
若用乙烯和氯气在适当的条件下反应制取三氯乙烷,这一过程中所发生的反应的类型及消耗氯气的量是(设乙烯为1 mol,反应产物中的有机物只有三氯乙烷)
A.取代反应,4 mol Cl2
B.加成反应,2 mol Cl2
C.加成反应、取代反应,3 mol Cl2
D.加成反应、取代反应,2 mol Cl2
 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源:2015-2016学年广东省高二下第一次段考文科化学试卷(解析版) 题型:选择题
下列物质中,从化学键的角度看,有一种与其他三种明显不同,这种物质是( )
A.NaOH B.CH4 C.SO2 D.H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省广州市南沙区高一下学期期末考试化学试卷(解析版) 题型:选择题
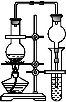
如图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是( )

A.50 mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46 mol
B.稀释该硫酸时应把水倒入硫酸中,边倒边搅拌
C.该硫酸试剂的物质的量浓度为18.4 mol/L
D.标准状况下2.7g Al与足量的该硫酸反应可得到H2 3.36L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一下学期期末考试化学试卷(解析版) 题型:填空题
如图表示4个碳原子相互结合的几种方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合。
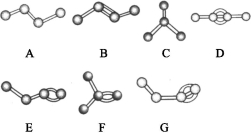
(1)图中属于烷烃的是 (填编号)。
(2)写出分子中碳原子数为2且与B互为同系物的有机物与水反应的化学方程式 ,该反应的反应类型为 。该反应生成的有机物在铜做催化剂的条件下与氧气反应的化学方程式为 。
(3)上图中与D互为同分异构体的是: 。(填编号)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列变化中,吸收的能量用于克服分子间作用力的是
A.加热氢氧化钠晶体使之熔化
B.电解水使之分解
C.碘单质受热升华
D.加热二氧化硅晶体使之熔化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是
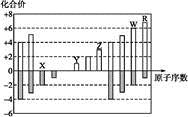
A. 离子原子半径: X2-> Y+>Z3+
B. 气态氢化物的沸点:X >R
C. 最高价氧化物的水化物的酸性:W>R
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二下学期期末考试化学试卷(解析版) 题型:实验题
用菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2)制备MnSO4·H2O的工艺流程如下:
Ⅰ.向菱锰矿中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量MnO2,过滤;
Ⅲ.调节滤液pH=a,过滤;
Ⅳ.浓缩、结晶、分离、干燥得到产品;
Ⅴ.检验产品纯度。
(1)步骤Ⅰ中,滤渣的主要成分是 。
(2)将MnO2氧化Fe2+的离子方程式补充完整:
 MnO2 +
MnO2 + Fe2++
Fe2++ =
= Mn2+ +
Mn2+ +  Fe3+ +
Fe3+ +
(3)与选用Cl2作为氧化剂相比,MnO2的优势主要在于:原料来源广、成本低、可避免环境污染、 。
(4)已知:生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 | 7.6 |
完全沉淀时 | 4.7 | 8.3 | 2.8 | 10.2 |
注:金属离子的起始浓度为0.1mol/L
步骤Ⅲ中a的取值范围是 。
(5)步骤Ⅴ,通过测定产品中锰元素的质量分数来判断产品纯度。
已知一定条件下,MnO4-与Mn2+反应生成MnO2 。取x g产品配成溶液,用0.1mol/L KMnO4溶液滴定,消耗KMnO4溶液y mL,产品中锰元素的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
已知,I2(aq)+I﹣(aq) I3﹣(aq).某I2、KI溶液中,c(I3﹣)与温度(T)的关系如图所示(曲上任何一点都表示平衡状态).下列说法正确的是
I3﹣(aq).某I2、KI溶液中,c(I3﹣)与温度(T)的关系如图所示(曲上任何一点都表示平衡状态).下列说法正确的是
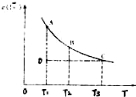
A.反应I2(aq)+I﹣(aq) I3﹣(aq)△H>0
I3﹣(aq)△H>0
B.状态A的c (I2)比状态D的小
C.A点对应的反应速率大于C点对应的反应速率
D.其他条件不变,向溶液中加入KI固体,平衡由C点移动到D点
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆四十二中高一下期中化学试卷(解析版) 题型:选择题
元素性质呈周期性变化的决定因素是( )
A. 元素原子半径大小呈周期性变化
B. 元素相对原子质量依次递增
C. 元素原子最外层电子排布呈周期性变化
D. 元素的最高正化合价呈周期性变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com