
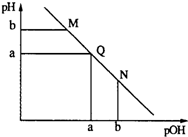
| A. | M点和N点溶液中H2O的电离程度相同 | |
| B. | Q点溶液中,c(NH4+)+c(OH-)=c(Cl-)+c(H+) | |
| C. | M点溶液的导电性大于Q点溶液的导电性 | |
| D. | N点溶液加水稀释,$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$变小 |
分析 碱溶液中pOH越大、pH越小,说明溶液中氢氧根离子浓度越小,氢离子浓度越大,碱性越弱、酸性越强,随着盐酸的加入,发生中和反应,溶液氢氧根离子的浓度逐渐减小,则溶液pH逐渐减小,pOH逐渐增大,结合弱电解质的电离解答该题.
解答 解:A.由于M点的OH-浓度等于N点的H+浓度,对水的电离程度抑制能力相同,所以两点水电离程度相同,故A正确;
B.Q点时pH=pOH,说明c(OH-)=c(H+),溶液呈中性,电荷守恒为:c(NH4+)+c(H+)=c(Cl-)+c(OH-),则c(NH4+)=c(Cl-),所以c(NH4+)+c(OH-)=c(Cl-)+c(H+),故B正确;
C.M点溶液中主要溶质为一水合氨,为弱电解质,在溶液中部分电离,溶液中离子浓度较小,Q点溶液中主要为氯化铵,为强电解质,溶液中离子浓度较多,所以M点的导电能力小于Q点,故C错误;
D.N点溶液加水稀释,Ka=$\frac{c(N{{H}_{4}}^{+})×c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$,温度不变,Ka不变,加水稀释氢离子浓度减小,c(OH-)增大,所以$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$变小,故D正确;
故选C.
点评 本题考查酸碱中和的定性判断和计算,侧重于弱电解质的电离的考查,注意弱电解质的电离特点,把握pOH的含义,题目难度中等.


科目:高中化学 来源: 题型:解答题

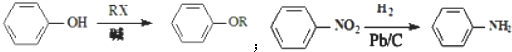

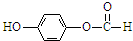 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| 甲 | C | 0.2 | pH=7 |
| 乙 | 0.2 | 0.1 | pH=a |
| 丙 | 0.2 | 0.2 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 盐酸的物质的量浓度为1mol/L | |
| B. | P点时恰好完全反应,溶液呈中性 | |
| C. | 曲线a是盐酸滴定氢氧化钠的滴定曲线 | |
| D. | 酚酞不能用作本实验的指示剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
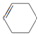 ).其中既能使酸性KMnO4溶液褪色,又能与溴水反应使溴水褪色的是( )
).其中既能使酸性KMnO4溶液褪色,又能与溴水反应使溴水褪色的是( )| A. | ②④⑤⑧ | B. | ②③⑤⑧ | C. | ②④⑤⑦ | D. | ②④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某烷烃命名为3-甲基-5-乙基己烷 | |
| B. | 用溴的CCl4溶液可鉴别己烷、2,4-己二烯和甲苯 | |
| C. | 酸性条件下CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 乙醇脱水制乙烯;溴乙烷消去制乙烯两者反应类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 分子式 | C8H10 | C3H5Cl | C4H8O2 | C4H9ClO |
| 限定条件 | 芳香烃 | 能发生加成反应 | 能与氢氧化钠溶液反应 | 能与钠反应 |
| A. | ③②①④ | B. | ②③①④ | C. | ③①②④ | D. | ②①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第IA族元素铯的同位素137Cs比133Cs多4个质子 | |
| B. | 溴元素的原子序数与氯元素的原子序数差为8 | |
| C. | 卤素元素的阴离子由上到下还原性依次减弱 | |
| D. | 117号元素位于元素周期表中第七周期、第VIIA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
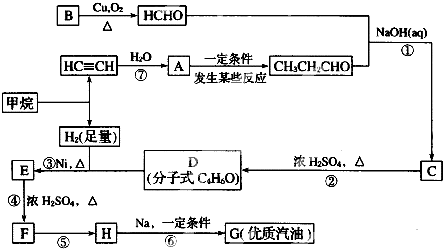
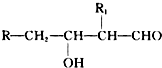
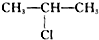
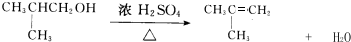 ;H→G
;H→G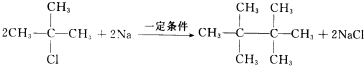 .
.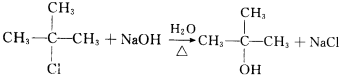 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com