
| A. | Ba(OH)2═Ba2++2OH- | B. | NaHSO4═Na++HSO4? | ||
| C. | CO32-+2H2O?H2CO3+2OH- | D. | Fe3++3H2O?Fe(OH)3↓+3H+ |
分析 A.氢氧化钡为强电解质完全电离;
B.硫酸氢钠为强电解质,在水溶液中完全电离;
C.碳酸根离子为多元弱酸根离子,分步水解,以第一步为主;
D.三价铁离子水解生成氢氧化铁和水,水解产生氢氧化铁少量,不标注沉淀符号.
解答 解:A.氢氧化钡为强电解质完全电离,电离方程式:Ba(OH)2=Ba2++2OH-,故A正确;
B.硫酸氢钠为强电解质,在水溶液中完全电离,电离方程式:NaHSO4=Na++H++SO42-,故B错误;
C.碳酸根离子水解方程式:CO32-+H2O?HCO3-+OH-,故C错误;
D.三价铁离子水解离子方程式:Fe3++3H2O?Fe(OH)3+3H+,故D错误;
故选:A.
点评 本题考查了电解质电离方程式、盐类水解离子方程式的书写,明确电解质强弱及电离方式,熟悉盐类水解规律是解题关键,题目难度不大.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:推断题
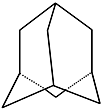 金刚烷的结构如图所示,它可看作是由四个等同的六元环组成的空间构型.
金刚烷的结构如图所示,它可看作是由四个等同的六元环组成的空间构型.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 现使用酸碱中和滴定法测定市售白醋(CH3COOH)的总酸量(g/100mL).
现使用酸碱中和滴定法测定市售白醋(CH3COOH)的总酸量(g/100mL).| 滴定次数 | 1 | 2 | 3 | 4 |
| V(样品) (mL) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) (mL) | 15.95 | 15.00 | 15.05 | 14.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 正极反应式:Ag+Cl--e-=AgCl | |
| B. | 每生成1mol Na2Mn5O10转移2mol电子 | |
| C. | Na+不断向“水”电池的负极移动 | |
| D. | 若用阳离子交换膜,当电路中转移0.2mole-,负极区将减少0.4mol离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:1 | B. | 2:1:2 | C. | 4:22:7 | D. | 8:11:14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(s,单斜)═S(s,正交)△H3=+0.33 kJ•mol-1 | |
| B. | 正交硫比单斜硫稳定 | |
| C. | 相同物质的量的正交硫比单斜硫所含有的能量高 | |
| D. | ①式表示断裂1 mol O2中的共价键所吸收的能量比形成1 mol SO2中的共价键所放出的能量多297.16 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com