
ĪŖŃŠ¾æ½šŹōøÆŹ“µÄĢõ¼žŗĶĖŁĀŹ£¬Ä³æĪĶāŠ”×éѧɜÓĆ½šŹōĖæ½«Čżøł“óŠ”ĻąĶ¬µÄĢś¶¤·Ö±š¹Ģ¶ØŌŚĶ¼Ź¾µÄČżøö×°ÖĆÖŠ£¬ŌŁ·ÅÖĆÓŚ²£Į§ÖÓÕÖĄļ±£“ęĻąĶ¬µÄŅ»¶ĪŹ±¼ä”£ĻĀĮŠ¶ŌŹµŃé½įŹųŹ±ĻÖĻóµÄĆčŹö²»ÕżČ·µÄŹĒ (””””)”£

A£®×°ÖĆ¢ń×ó²ąµÄŅŗĆęŅ»¶Ø»įĻĀ½µ
B£®×ó²ąŅŗĆę×°ÖĆ¢ń±Č×°ÖĆ¢ņµÄµĶ
C£®×°ÖĆ¢ņÖŠµÄĢś¶¤øÆŹ“×īŃĻÖŲ
D£®×°ÖĆ¢óÖŠµÄĢś¶¤¼øŗõĆ»±»øÆŹ“
½āĪö””ÓŠ¹Ų½šŹōøÆŹ“µÄĢāŠĶ£¬ŅŖĒóøćĒ彚ŹōøÆŹ“µÄÖ÷ŅŖŌŅņ(µē»ÆѧøÆŹ“)£¬
ŌĖÓĆŌµē³ŲŌĄķ½ųŠŠĒ”µ±µÄ·ÖĪö£¬Ķ¬Ź±ÕĘĪÕ½šŹō·Ą»¤µÄ»ł±¾·½·Ø£ŗøı佚Źō
ÄŚ²æ½į¹¹(ČēÖĘ³ÉŗĻ½š)”¢Ķæ±£»¤²ćŗĶµē»Æѧ±£»¤·Ø”£¢ņÖŠĢś¶¤ÓėĶĖæĻąĮ¬£¬
½šŹō»īĘĆŠŌĻą²ī½Ļ“ó£¬ĒŅÓƻӷ¢ŠŌŃĪĖį£¬Ņņ“Ė×°ÖĆ¢ņÖŠµÄĢś¶¤øÆŹ“×īŃĻÖŲ£¬
CĻīÕżČ·£»¢ńÖŠĖäČ»Ņ²ÓĆĮĖŃĪĖį£¬µ«Ģś¶¤ÓėĢśĖæĻąĮ¬£¬øÆŹ“²»¼°¢ņ£»ÓÉÓŚ¾ł
·¢ÉśĮĖ2H£«£«2e£===H2”ü£¬¢ńŗĶ¢ņ¾łÉś³ÉĮĖĘųĢ壬ŅŗĆę¶¼»įĻĀ½µ£¬×ó²ąŅŗĆę
×°ÖĆ¢ņ±Č×°ÖĆ¢ńµÄµĶ£¬AĻīÕżČ·£¬BĻī“ķĪ󣻢óÖŠĖäČ»Ģś¶¤⇒Ņ²ÓėĶĖæĻąĮ¬£¬
µ«ÓÉÓŚĖł×°ŹŌ¼ĮĪŖ²»»Ó·¢ŠŌĮņĖį£¬Ņņ“ĖĢś¶¤¼øŗõĆ»±»øÆŹ“£¬DŃ”ĻīÕżČ·”£
“š°ø””B



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ (””””)”£
A£®ÖŹĮæŹżŹĒŌ×ÓŗĖÄŚÖŹ×ÓÖŹĮæÓėÖŠ×ÓÖŹĮæÖ®ŗĶ
B£®¾ßÓŠĻąĶ¬ÖŹ×ÓŹżµÄĪ¢Į££¬Ęä»ÆѧŠŌÖŹŅ»¶ØĻąĶ¬
C£®×īĶā²ćÓŠ5øöµē×ÓµÄŌ×Ó¶¼ŹĒ·Ē½šŹōŌ×Ó
D£®×īĶā²ćÓŠ8øöµē×ÓµÄĪ¢Į££¬²»Ņ»¶ØŹĒĻ”ÓŠĘųĢåµÄŌ×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷×éÓŠ»śĪļ£¬ĪŽĀŪŅŌŗĪÖÖĪļÖŹµÄĮæµÄ±ČĄż»ģŗĻ£¬Ö»ŅŖ×ÜĪļÖŹµÄĮæŅ»¶Ø£¬ŌņĶźČ«Č¼ÉÕĻūŗÄŃõĘųµÄĮæĪŖŅ»ŗć¶ØÖµµÄŹĒ(””””)
A£®C3H6ŗĶC3H8 B£®C2H6ŗĶC2H4O2
C£®C5H10ŗĶC6H6 D£®C2H6ŗĶC3H8
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¾Ż±ØµĄ£¬ŗŗ½Į÷ÓņŌŁ“Ī·¢Éś”°Ė®»Ŗ”±ĻÖĻ󣬽ĆęÉĻÓŠ“óĮæĀĢÉ«ĘÆø”Īļ£¬ĄąĖĘÓŚŗ£ĆęÉĻµÄ”°ŗģ³±”±£¬Č”Ė®Ńł·ÖĪö£ŗĀĢŌåŗ¬Įæ±ČÕż³£ĒéæöĻĀĘ«øßŗܶą£¬ŗ¬ŃõĮæĆ÷ĻŌĘ«µĶ£¬»ė×Ē¶ČŌö¼Ó”£Ōģ³Éŗŗ½”°Ė®»Ŗ”±×īæÉÄܵÄŌŅņŹĒ(””””)”£
A£®Ė®ĶĮĮ÷Ź§
B£®ÓŠ¶¾µÄ·ĻĖ®“óĮæÅÅČėŗŗ½
C£®Éś»ī·ĻĖ®“óĮæÅÅČėŗŗ½£¬Ź¹Ė®ÖŹø»ÓŖŃų»Æ
D£®ŗŗ½Į÷ÓņÅ©ŅµÉś²śÖŠ³¤ĘŚŹ¹ÓĆÅ©Ņ©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĒéæöĻĀ£¬²»Ņ×·¢Éśµē»ÆѧøÆŹ“µÄŹĒ (””””)”£
A£®øÖĢśŌŚ³±ŹŖµÄæÕĘųÖŠ
B£®øÖĢśŌŚÓźĖ®ÖŠ
C£®Ķ±ŅŌŚµŲĻĀĖ®ÖŠ
D£®²»ŠāøÖŌŚ³±ŹŖµÄæÕĘųÖŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪŖĮĖ·ĄÖ¹øÖĢśŠāŹ“£¬ĻĀĮŠ·Ą»¤·½·ØÖŠÕżČ·µÄŹĒ (””””)”£
A£®ŌŚ¾«ĆܵÄĢśÖĘŅĒĘ÷ÉĻĆÉĻĶ¶¤Ōö¼ÓĆĄ¹ŪŠŌ
B£®ŌŚÅÅ·Åŗ£Ė®µÄøÖĢś·§ĆÅÉĻÓƵ¼ĻßĮ¬½ÓŅ»æéŹÆÄ«£¬Ņ»Ķ¬½žČėŗ£Ė®ÖŠ
C£®ŌŚµŲĻĀŹäÓĶµÄÖżĢś¹ÜÉĻ°ü¹üŅ»²ćøßĆܶČĖÜĮĻ
D£®ŌŚŗ£ĀÖĻĻÉĻÓĆĢśĖæĻµ×”Ķ°å½žŌŚŗ£Ė®Ąļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
25 ”ꏱ£¬pH£½3µÄŃĪĖįa L·Ö±šÓėĻĀĮŠČżÖÖČÜŅŗ³ä·Ö»ģŗĻŗó£¬ČÜŅŗ¾ł³ŹÖŠŠŌ£ŗ¢Łc(NH3”¤H2O)£½10£3 mol”¤L£1µÄ°±Ė®b L£¬¢Śc(OH£)£½10£3 mol”¤L£1µÄ°±Ė®c L£¬¢Ūc(OH£)£½10£3 mol”¤L£1µÄBa(OH)2ČÜŅŗd L”£ŹŌÅŠ¶Ļa”¢b”¢c”¢dµÄŹżĮæ“󊔹ŲĻµĪŖ(””””)
A£®a£½b>c>d B£®b>a£½d>c C£®b>a>d>c D£®c>a£½d>b
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪļÖŹŌŚĖ®ČÜŅŗÖŠæÉÄÜ“ęŌŚµēĄėĘ½ŗā”¢ŃĪµÄĖ®½āĘ½ŗā»ņ³ĮµķČܽāĘ½ŗā£¬ĖüĆĒ¶¼æÉæ“×÷»ÆŃ§Ę½ŗāµÄŅ»ÖÖ”£Ēėøł¾ŻĖłŃ§»ÆѧÖŖŹ¶»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)AĪŖ0.1 mol”¤L£1µÄ(NH4)2SO4ČÜŅŗ£¬ŌŚøĆČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ
________________________________________________________________________ӣ
(2)BĪŖ0.1 mol”¤L£1µÄNaHCO3ČÜŅŗ£¬NaHCO3ŌŚøĆČÜŅŗÖŠ“ęŌŚµÄĘ½ŗāÓŠ(ÓĆĄė×Ó·½³ĢŹ½±ķ
Ź¾)________________________________________________________________________
________________________________________________________________________ӣ
(3)CĪŖ0.1 mol”¤L£1µÄ(NH4)2Fe(SO4)2ČÜŅŗ£¬ÓėĶ¬ÅØ¶ČµÄ(NH4)2SO4ČÜŅŗÖŠĻą±Č½Ļ______(ĢīČÜÖŹµÄ»ÆѧŹ½)ČÜŅŗÖŠNH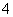 µÄÅضČøü“ó£¬ĘäŌŅņŹĒ
µÄÅضČøü“ó£¬ĘäŌŅņŹĒ
________________________________________________________________________
________________________________________________________________________ӣ
(4)DĪŖŗ¬ÓŠ×ćĮæAgCl¹ĢĢåµÄ±„ŗĶČÜŅŗ£¬AgClŌŚČÜŅŗÖŠ“ęŌŚČēĻĀĘ½ŗā£ŗAgCl(s)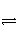
 Ag£«(aq)£«Cl£(aq)
Ag£«(aq)£«Cl£(aq)
ŌŚ25 ”ꏱ£¬AgClµÄKsp£½1.8”Į10£10mol2”¤L£2”£ĻÖ½«×ćĮæAgCl·Ö±š·ÅČėĻĀĮŠŅŗĢåÖŠ£ŗ¢Ł100 mLÕōĮóĖ®””¢Ś100 mL 0.3 mol”¤L£1 AgNO3ČÜŅŗ””¢Ū100 mL 0.1 mol”¤L£1 MgCl2ČÜŅŗ³ä·Ö½Į°čŗóĄäČ“µ½ĻąĶ¬ĪĀ¶Č£¬Ag£«ÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ______(ĢīŠņŗÅ)£¬“ĖŹ±ČÜŅŗ¢ŚÖŠCl£ĪļÖŹµÄĮæÅضČĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ»ÆѧŹµŃ黳±¾²Ł×÷ÕżČ·µÄŹĒ
A£®ÓĆŹÖÖ±½ÓÄĆČ”ķĄĀė
B£®ÓĆ×ģ“µĆš¾Ę¾«µĘ
C£®ÓĆ½ą¾»µÄ²£Į§°ōÕŗČ”“ż²āŅŗµĪŌŚpHŹŌÖ½ÉĻ²āpH
D£®ÅäÖĘČÜŅŗŹ±ŃöŹÓ¶ĮĮæĶ²ÄŚŅŗĢåĢå»ż
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com