
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[3,3]庚烷(![]() )是其中的一种。下列关于该化合物的说法不正确的是( )
)是其中的一种。下列关于该化合物的说法不正确的是( )
A. 与环庚烯互为同分异构体B. 二氯代物共有8种(不含立体异构)
C. 所有碳原子不可能处在同一平面D. 1mol该化合物含有18mol共价键
【答案】D
【解析】
A、该有机物的分子式为C7H12,与环庚烯的分子式相同,其结构不同,故互为同分异构体,故A不选;
B、![]() 有2种不同位置的H原子,若二氯代物中两个Cl原子位于同一个C原子上,有2种同分异构体,若位于不同C原子上,在一个四元环上,有2种不同位置;若位于两个四元环上,可能有4种不同结构,因此二氯代物共有2+2+4=8种,故B不选;
有2种不同位置的H原子,若二氯代物中两个Cl原子位于同一个C原子上,有2种同分异构体,若位于不同C原子上,在一个四元环上,有2种不同位置;若位于两个四元环上,可能有4种不同结构,因此二氯代物共有2+2+4=8种,故B不选;
C、在螺[3,3]庚烷(![]() )分子中的C原子都是饱和C原子,由于与C原子连接的原子构成的是四面体结构,最多有三个原子处于同一平面上,因此不可能所有碳原子处在同一平面上,故C不选;
)分子中的C原子都是饱和C原子,由于与C原子连接的原子构成的是四面体结构,最多有三个原子处于同一平面上,因此不可能所有碳原子处在同一平面上,故C不选;
螺[3,3]庚烷分子式是C7H12,1个分子中含有8个C—C键,含有12个C—H,所以一个分子中含有20个共价键,则1mol该化合物中含有20mol共价键,故D选;


科目:高中化学 来源: 题型:
【题目】下列方程式不正确的是
A.NaHCO3在水中的电离方程式:NaHCO3 = Na++HCO![]()
B.氯化镁溶液与氨水反应的离子方程式:Mg2++2OH-= Mg(OH)2↓
C.Cl2与水反应的离子方程式:Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
D.醋酸钠水解的离子方程式CH3COO-+H2O![]() CH3COOH+OH-
CH3COOH+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C物质为烃类,在标准状况下的密度为1.16g/L,F物质具有水果香味,G物质不能水解。转化关系如图所示,省略了反应条件。
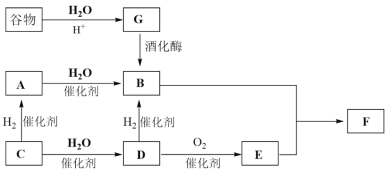
请回答下列问题:
(1)写出G的分子式:____________________。
(2)D中官能团的名称是__________________________。 C→A的反应类型____________
(3)请写出反应B+E→F的化学方程式:______________________。
(4)下列有关说法正确的是_____________________________。
A.C物质燃烧时,易产生大量黑烟 B.物质B和甘油(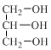 )互为同系物
)互为同系物
C.一定条件下,A可被直接氧化为D D.用NaOH溶液可以区分B、D、F
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。2017年5月9日,中国公布113号、115号、117号和118号四种元素的中文名称。其中118号元素的原子符号为![]() Og,中文名称为“
Og,中文名称为“![]() ”下列说法不正确的是
”下列说法不正确的是
A. 质子数为118B. 中子数为176
C. 核外电子数为118D. 质量数为412
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,改变某醋酸溶液的pH,溶液中c(CH3COO-)与c(CH3COOH)之和始终为0.1mol·L-1,溶液中H+、OH-、CH3COO-及CH3COOH浓度的常用对数值(lgc)与pH的关系如图所示。下列说法错误的是( )
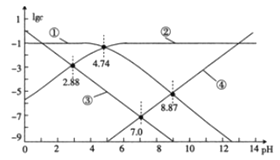
A.图中③表示lgc(H+)与pH的关系曲线
B.0.1mol·L-1CH3COOH溶液的pH约为2.88
C.lgK(CH3COOH)=4.74
D.向0.10mol·L-1醋酸钠溶液中加入0.1mol醋酸钠固体,水的电离程度变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】线型PAA(![]() )具有高吸水性,网状PAA在抗压性、吸水性等方面优于线型PAA。网状PAA的制备方法是:将丙烯酸用NaOH中和,加入少量交联剂a,再引发聚合。其部分结构片段如下:
)具有高吸水性,网状PAA在抗压性、吸水性等方面优于线型PAA。网状PAA的制备方法是:将丙烯酸用NaOH中和,加入少量交联剂a,再引发聚合。其部分结构片段如下:

下列说法不正确的是( )
A. 线型PAA的单体不存在顺反异构现象
B. 交联剂a的结构简式是![]()
C. 形成网状结构的过程发生了加聚反应
D. PAA的高吸水性与—COONa有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)在①苯 ②乙醇③甲苯 ④氯乙烷 ⑤![]() ⑥
⑥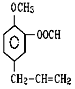 ⑦
⑦![]() 七种物质中(填编号)
七种物质中(填编号)
能和金属钠反应放出H2的有_________________常温能与NaOH溶液反应的有___________
常温下能与溴水反应的有____________________能使酸性KMnO4溶液褪色的有__________
(2)某有机物结构简式如图所示,则用足量的Na、NaOH、NaHCO3、浓溴水分别与等物质的量的该有机物反应时,消耗Na、NaOH、NaHCO3和Br2的物质的量之比为__________.

(3)A、B、C 三种醇同足量的金属钠完全反应,在相同条件下产生相同体积的氢气,消耗这三种醇的物质的量之比为2:6:3,则A、B、C 三种醇分子中含羟基数目之比是______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应KMnO4+FeSO4+H2SO4→MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是( )

A. 石墨b是原电池的负极,发生氧化反应
B. 甲烧杯中的电极反应式:MnO4-+5e-+8H+===Mn2++4H2O
C. 电池工作时,盐桥中的阴阳离子分别向乙甲烧杯中移动,保持溶液中的电荷平衡
D. 忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸钠(NaH2PO2)是有机合成的常用还原剂,一般制备方法是将黄磷(P4)和过量烧碱溶液混合、加热,生成次磷酸钠和PH3,PH3是一种无色、有毒且能自燃的气体。实验装置如图所示:
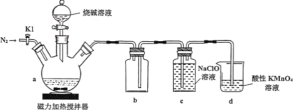
回答下列问题:
(1)在a中加入黄磷、活性炭粉末,打开K1,通入N2一段时间,关闭K1,打开磁力加热搅拌器,滴加烧碱溶液。
①仪器a的名称是______,已知NaH2PO2能与盐酸反应但不能与NaOH溶液反应,则次磷酸(H3PO2)是_______元弱酸。
②反应开始时,首先打开K1,通入N2一段时间,其目的是________。
③为了尽可能避免PH3造成的空气污染,拆卸装置前还要进行的一项操作是_________,a中反应的化学方程式为_______。
(2)装置c中生成NaH2PO2和NaCl,相关物质溶解度(S)如下,通过______的方法可分离出NaH2PO2固体。

(3)产品纯度测定:
取产品m g配成250mL溶液,取25mL于锥形瓶中,然后用0.01 mol/L KMnO4标准溶液滴定至终点(氧化产物是PO43-),达到滴定终点时消耗V1 mL KMnO4标准溶液,产品纯度为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com