
����Ŀ��X��Y��Z��M��G��������Ԫ�ط������������ڣ���ԭ��������������X��Zͬ���壬���γ����ӻ�����ZX��Y��Mͬ���壬���γ�MY2��MY3���ַ��ӡ�������ѧ�����ش��������⣺
��1��G�����ӵĽṹʾ��ͼΪ____��Y��Z��M�����ӵİ뾶�ɴ�С��˳��Ϊ____�������ӷ��ű�ʾ����
��2������Ԫ�ص�����������Ӧ��ˮ����������ǿ����___���ѧʽ����Y��M�ļ��⻯��е�ϸߵ���____���ѧʽ������ɸ����ʵķ��ӵĿռ�ṹΪ_____��
��3��Y��G�ĵ��ʻ���Ԫ��֮���γɵĻ��������ˮ����������______��д���֣��ѧʽ����
��4��Z��Y����Ԫ�صĵ����ڼ��������¿ɷ�����Ӧ������ĵ���ʽΪ______��
��5��M�ĵ�����������������Ӧˮ���ﷴӦ�Ļ�ѧ����ʽΪ______��
���𰸡�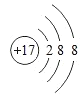 S2��>O2��>Na+ HClO4 H2O V�� Cl2��O3��ClO2����д���֣�
S2��>O2��>Na+ HClO4 H2O V�� Cl2��O3��ClO2����д���֣� ![]() S��2H2SO4(Ũ)
S��2H2SO4(Ũ)![]() 3SO2����2H2O
3SO2����2H2O
��������
X��Y��Z��M��G��������Ԫ�ط������������ڣ���ԭ������������������X��HԪ�أ�X��Zͬ���壬���γ����ӻ�����ZX����Zԭ����������Yԭ������������Z��NaԪ�أ�Y��Mͬ���壬���γ�MY2��MY3���ַ��ӣ�����Y��OԪ�أ�M��SԪ�أ�G�Ƕ���������Ԫ�أ�����G��ClԪ�أ����Ԫ���������Լ�Ԫ�ص����ʽ��д��⡣
�ɷ�����֪��X��HԪ�أ�Y��OԪ�أ�Z��NaԪ�أ�M��SԪ�أ�G��ClԪ�ء�
��1���ɷ�����֪��G��ClԪ�أ������Ӻ�����3�����Ӳ㣬�������8�����ӣ��������ӵĽṹʾ��ͼΪ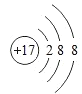 ��Y��Z��M�����ӷֱ�ΪO2-��Na+��S2-�����Ӳ���Խ�࣬���Ӱ뾶Խ������ͬ��������Ų������ӣ��˵����Խ�����Ӱ뾶ԽС���������Ӱ뾶�ɴ�С��˳��Ϊ��S2��>O2��>Na+���ʴ�Ϊ��
��Y��Z��M�����ӷֱ�ΪO2-��Na+��S2-�����Ӳ���Խ�࣬���Ӱ뾶Խ������ͬ��������Ų������ӣ��˵����Խ�����Ӱ뾶ԽС���������Ӱ뾶�ɴ�С��˳��Ϊ��S2��>O2��>Na+���ʴ�Ϊ�� ��S2��>O2��>Na+��
��S2��>O2��>Na+��
��2���ǽ�����Ԫ�صķǽ�����Խǿ������Ӧ����ۺ����������Խǿ���⼸��Ԫ�طǽ�������ǿ����ClԪ�أ�������ۺ������������ǿ���Ǹ�����HClO4��Y��M�ļ��⻯��ֱ�ΪH2O��H2S��ͬ��Ԫ���γɵ��⻯��ṹ���ƣ����ڽṹ���Ƶ����ʣ�һ������£���Է�������Խ���Ӽ���������Խ�����ʵ��۷е��Խ�ߣ�����������ˮ����֮���������������˷���֮�������ã����Էе�H2O��H2S��ˮ���ӵĿռ�ṹΪV�Σ��ʴ�Ϊ��HClO4��H2O��V�Ρ�
��3��Y�ĵ���O3��G�ĵ���Cl2����Ԫ��֮���γɵĻ�����ΪClO2������ˮ���������ʴ�Ϊ��Cl2��O3��ClO2����д���֣���
��4��O��Na����Ԫ�صĵ����ڼ��������¿ɷ�����Ӧ���ɹ������ƣ����������������������������֮���γ����Ӽ�����������������ԭ��֮���γɹ��ۼ��������ʽΪΪ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��5��SԪ�ص�����������Ӧˮ����ΪH2SO4��S������Ũ���ᷴӦ�Ļ�ѧ����ʽΪS��2H2SO4(Ũ)![]() 3SO2����2H2O���ʴ�Ϊ��S��2H2SO4(Ũ)
3SO2����2H2O���ʴ�Ϊ��S��2H2SO4(Ũ)![]() 3SO2����2H2O��
3SO2����2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����84������Һ���ճ�������ʹ�ù㷺��������Һ��ɫ����Ư�����ã�������Ч�ɷ����������ʵ�һ�֣�����������( )
A.Ca(ClO)2B.Na2O2C.H2O2D.NaClO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��װ���ܴﵽ��ӦĿ�ĵ��ǣ� ��
A | B | C | D | |
ʵ��װ�� |
|
|
|
|
Ŀ�� | ��֤Fe��ϡ���ᷴӦ���� | �ⶨ�к��� | �Ʊ������NH3 | ����I2��NH4Cl |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ��е�VIIA��Ԫ�صĵ��ʼ��仯�������;�㷺��
��1������Ϊ�ȡ��塢��Ԫ�طǽ�����(ԭ�ӵõ�������)�ݱ���ɵ��ж�������____(�����)��
a��Cl2��Br2��I2���۵� b��Cl2��Br2��I2��������
c��HCl��HBr��HI�����ȶ��� d��HCl��HBr��HI������
��2����Ԫ�ؿ�Ԥ����״���״�����ҹ��г��ϵ�ʳ�ξ����˵⣨KIO3������ͬѧ����ʳ���Ƿ�ӵ���������£�
![]()
������ƷΪ�ӵ�ʳ�Σ�������ӦΪ_____���˷�����KI��������_____��
����ͬѧȡ��NaCl����Ʒ������ʵ�飬Ҳ���������Ե�����ԭ����____��
�۱�ͬѧ����µļ���ӵ�ʳ�εķ������������£�
![]()
�˷�����һ���漰��Ӧ�����ӷ���ʽΪ____��
��3����֪��Ӧ2HBr(g) = H2(g) + Br2(g) ��H= +102 kJ��mol��1��
��1molH2(g)��1molBr2(g)�����л�ѧ������ʱ�ֱ���Ҫ����436kJ��200kJ����������1molHBr(g)�����л�ѧ������ʱ�����յ�����Ϊ___kJ��
��ij�¶��£������Ϊ2L���ܱ�������ͨ��amol HBr���壬10min����Br2������Ũ��Ϊbmol/L����˶�ʱ������(HBr)=____��
��4��һ����������ˮ��Һ��1 mol Cl����ClOx��(x��1��2��3��4)������(kJ)��Դ�С��ͼ��ʾ��

B��A��C��Ӧ���Ȼ�ѧ����ʽΪ____(�����ӷ��ű�ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����Ȼ�ѧ����ʽ��
��H2(g)+1/2O2(g)��H2O(l) ��H =��285.8 kJ/mol
��H2(g)+1/2O2(g)��H2O(g) ��H =��241.8 kJ/mol
��C(s)+1/2O2(g)��CO(g) ��H =��110.5 kJ/mol
��C(s)+O2(g)��CO2(g) ��H =��393.5 kJ/mol
�ش��������⣺
��1��H2��ȼ������H��_______��C��ȼ����Ϊ__________��
��2��ȼ��1 g H2����Һ̬ˮ���ų�������Ϊ_________��
��3����֪CO��ȼ����Ϊ283.0 kJ/mol������CO��H2��CO2��ɵĻ������116.8 L(��״��)����ȫȼ�պ�ų�������Ϊ867.9 kJ��������18 gҺ̬ˮ������������H2Ϊ_________L��CO�ڻ�������е��������ԼΪ_________(��ȷ��С�����һλ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ�ÿ������ռ����岢��֤�仯ѧ���ʣ����ж�Ӧ��ϵ��ȫ��ȷ����(����)
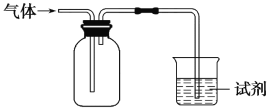
ѡ�� | ���� | �Լ� | ���� | ���� |
A | NO | ��ɫʯ����Һ | ��Һ��� | NO��ˮ��Ӧ�������� |
B | Cl2 | ����KI��Һ | ��Һ���� | Cl2�������� |
C | SO2 | Ʒ����Һ | ��Һ��ɫ | SO2��ǿ������ |
D | NH3 | MgCl2��Һ | ������ɫ���� | NH3�м��� |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���������ȷ���ǣ� ��
A.��ˮ�������Ȼ�̼�;ƾ��Ļ����
B.�������ʱ������ֹͣ���ȣ��ر�����ˮ
C.����һ�����ʵ���Ũ�ȵ�������Һʱ������Ͳ��ȡһ�������Ũ���ᵹ���ձ��������� ��ˮϴ����Ͳ2��3�Σ�����ϴ��Һһ�������ձ���ϡ��
D.�����ڳ���ֽ�ϳ�ȡ��NaOH�������ձ����ܽ⣬����ȴ����ת��������ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ͽ�1 mol AB(g)�����еĻ�ѧ��ʹ��ֱ�������̬Aԭ�Ӻ���̬Bԭ�������յ�������ΪA��B���ļ��ܡ��±��г���һЩ��ѧ���ļ���E��
��ѧ�� | H��H | Cl��Cl | O===O | C��Cl | C��H | O��H | H��Cl |
E/kJ��mol��1 | 436 | 247 | x | 330 | 413 | 463 | 431 |
��ش��������⣺
��ͼ��ʾij��Ӧ�������仯��ϵ����˷�ӦΪ________(����ȡ����ȡ�)��Ӧ�����Ц�H��______________(�ú���a��b�Ĺ�ϵʽ��ʾ)��

��ͼʾ�б�ʾ��Ӧ H2(g)��O2(g)===H2O(g) ��H����241.8 kJ��mol��1����b��________kJ��mol��1��x��__________��
(3)��ʷ�����á��ؿ���������������һ��������CuCl2����������450 �����ÿ����е��������Ȼ��ⷴӦ����������Ӧ�Ļ�ѧ����ʽΪ___________________________________���������¶Ⱥ�ѹǿ�Է�Ӧ�ȵ�Ӱ�죬���������е��й����ݣ����㵱��Ӧ����1 mol����ת��ʱ����Ӧ�������仯Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��鷴Ӧ�У����ڿ��淴Ӧ��һ���ǣ� ��
A. 2H2O![]() 2H2��+O2����2H2+O2
2H2��+O2����2H2+O2![]() 2H2O
2H2O
B. NH3+CO2+H2O=NH4HCO3��NH4HCO3![]() NH3��+H2O��+CO2��
NH3��+H2O��+CO2��
C. H2+I2![]() 2HI��2HI
2HI��2HI![]() H2��+I2��
H2��+I2��
D. 2Ag+Br2![]() 2AgBr��2AgBr
2AgBr��2AgBr![]() 2Ag+Br2
2Ag+Br2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com