
”¾ĢāÄæ”æŃŠ¾æ¼õÉŁCO2ÅÅ·ÅŹĒŅ»ĻīÖŲŅŖæĪĢā”£CO2¾“߻ƼÓĒāæÉŅŌÉś³ÉµĶĢ¼ÓŠ»śĪļ£¬Ö÷ŅŖÓŠŅŌĻĀ·“Ó¦£ŗ
·“Ó¦¢ń£ŗCO2(g)£«3H2(g)![]() CH3OH(g)£«H2O(g) ”÷H1£½£49.6 kJ/mol
CH3OH(g)£«H2O(g) ”÷H1£½£49.6 kJ/mol
·“Ó¦¢ņ£ŗCH3OCH3(g)£«H2O(g)![]() 2CH3OH(g) ”÷H2£½£«23.4 kJ/mol
2CH3OH(g) ”÷H2£½£«23.4 kJ/mol
·“Ó¦¢ó£ŗ2CO2(g)£«6H2(g)![]() CH3OCH3(g)£«3H2O(g) ”÷H3
CH3OCH3(g)£«3H2O(g) ”÷H3
£Ø1£©”÷H3£½____kJ/mol”£
£Ø2£©ŗćĪĀŗćČŻĢõ¼žĻĀ£¬ŌŚĆܱÕČŻĘ÷ÖŠĶØČėµČĪļÖŹµÄĮæµÄCO2ŗĶH2£¬·¢Éś·“Ó¦I”£ĻĀĮŠĆčŹöÄÜĖµĆ÷·“Ó¦I“ļµ½Ę½ŗāדĢ¬µÄŹĒ___£ØĢīŠņŗÅ£©”£
A£®·“Ó¦ĢåĻµ×ÜŃ¹Ēæ±£³Ö²»±ä
B£®ČŻĘ÷ÄŚµÄ»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
C£®Ė®·Ö×ÓÖŠ¶ĻĮŃ2NAøöH-O¼ü£¬Ķ¬Ź±Ēā·Ö×ÓÖŠ¶ĻĮŃ3NAøöH-H¼ü
D£®CH3OHŗĶH2OµÄÅضČÖ®±Č±£³Ö²»±ä
£Ø3£©·“Ó¦IIŌŚÄ³ĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżĪŖ0.25£¬“ĖĪĀ¶ČĻĀ£¬ŌŚĆܱÕČŻĘ÷ÖŠ¼ÓČėµČĪļÖŹµÄĮæµÄCH3OCH3(g)ŗĶH2O(g)£¬·“Ó¦µ½Ä³Ź±æĢ²āµĆø÷×é·ÖÅضČČēĻĀ£ŗ
ĪļÖŹ | CH3OCH3(g) | H2O(g) | CH3OH(g) |
ÅضČ/mol”¤L£1 | 1.8 | 1.8 | 0.4 |
“ĖŹ±vÕż___vÄę£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©£¬µ±·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬»ģŗĻĘųĢåÖŠCH3OHĢå»ż·ÖŹż(CH3OH)% £½___%”£
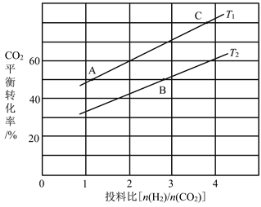
£Ø4£©ŌŚÄ³Ń¹ĒæĻĀ£¬·“Ó¦IIIŌŚ²»Ķ¬ĪĀ¶Č”¢²»Ķ¬Ķ¶ĮĻ±ČŹ±£¬CO2µÄĘ½ŗā×Ŗ»ÆĀŹČēĶ¼ĖłŹ¾”£T1ĪĀ¶ČĻĀ£¬½«6mol CO2ŗĶ12mol H2³äČė2 LµÄĆܱÕČŻĘ÷ÖŠ£¬5minŗó·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬Ōņ0”«5minÄŚµÄĘ½¾ł·“Ó¦ĖŁĀŹv(CH3OCH3)£½____£»KA”¢KB”¢KCČżÕßÖ®¼äµÄ“󊔹ŲĻµĪŖ____”£
£Ø5£©ŗćŃ¹ĻĀ½«CO2ŗĶH2°“Ģå»ż±Č1£ŗ3»ģŗĻ£¬ŌŚ²»Ķ¬“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ó¦IŗĶ·“Ó¦III£¬ŌŚĻąĶ¬µÄŹ±¼ä¶ĪÄŚCH3OHµÄŃ”ŌńŠŌŗĶ²śĀŹĖęĪĀ¶ČµÄ±ä»ÆČēĶ¼”£ĘäÖŠ£ŗCH3OHµÄŃ”ŌńŠŌ£½![]() ”Į100%
”Į100%
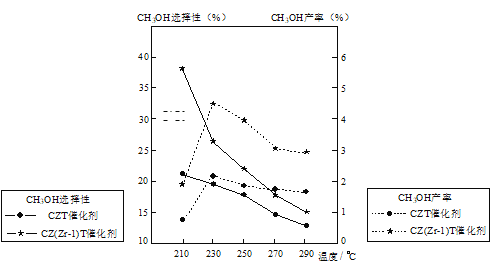
¢ŁĪĀ¶ČøßÓŚ230”ę£¬CH3OH²śĀŹĖęĪĀ¶ČÉżø߶ųĻĀ½µµÄŌŅņŹĒ_____”£
¢ŚŌŚÉĻŹöĢõ¼žĻĀŗĻ³É¼×“¼µÄ¹¤ŅµĢõ¼žŹĒ____”£
p>A£®210”ę B£®230”ę C£®“߻ƼĮCZT D£®“߻ƼĮCZ(Zr£1)T”¾“š°ø”æ£122.6 AC £¾ 20 0.18mol”¤L1”¤min1 KA£½KC£¾KB ·“Ó¦IµÄ”÷H£¼0ĪĀ¶ČÉżøߣ¬Ź¹CO2×Ŗ»ÆĪŖCH3OHµÄĘ½ŗā×Ŗ»ÆĀŹĻĀ½µ BD
”¾½āĪö”æ
£Ø1£©øł¾ŻøĒĖ¹¶ØĀÉŅŌ¼°ČČ»Æѧ·½³ĢŹ½½ųŠŠ¼ĘĖć£»
£Ø2£©øł¾Ż»ÆŃ§Ę½ŗāדĢ¬µÄÅŠ¶Ļ±źÖ¾½ųŠŠÅŠ¶Ļ£»
£Ø3£©øł¾ŻÅضČÉĢŗĶ»ÆŃ§Ę½ŗā³£ŹżµÄ“󊔹ŲĻµÅŠ¶Ļ·“Ó¦½ųŠŠµÄ·½Ļņ£»ÉčĪ“ÖŖŹżĄūÓĆ»ÆŃ§Ę½ŗā³£ŹżĮŠ³öČż¶ĪŹ½½ā·½³Ģ£¬½ų¶ų¼ĘĖćĢå»ż·ÖŹż£»
£Ø4£©øł¾ŻĶ¼ĻńČ·¶ØCO2µÄĘ½ŗā×Ŗ»ÆĀŹ£¬½ų¶ų¼ĘĖćCH3OCH3µÄÉś³ÉĮ棬ŌŁĄūÓĆ»Æѧ·“Ó¦ĖŁĀŹµÄ¼ĘĖć¹«Ź½¼ĘĖćv(CH3OCH3)£»øł¾Ż»ÆŃ§Ę½ŗā³£ŹżÖ»ÓėĪĀ¶ČÓŠ¹Ų£¬ĪĀ¶Č²»±ä£¬»ÆŃ§Ę½ŗā³£Źż²»±ä£¬µĆ³öKA£½KC£¬ŌŁøł¾ŻøĆ·“Ó¦ĪŖÕżĻņ·ÅČȵķ“Ó¦£¬½µĪĀĘ½ŗāÄęĻņŅĘ¶Æ£¬½įŗĻĶ¼ĻńÅŠ¶ĻT1”¢T2µÄ“󊔹ŲĻµ£¬“Ó¶ųµĆ³öKA”¢KC”¢KBČżÕߵĹŲĻµ£»
£Ø5£©·“Ó¦IµÄ”÷H£¼0£¬ÉżĪĀĘ½ŗāÄęĻņŅĘ¶Æ£¬CO2×Ŗ»Æ×Ŗ»ÆĀŹ½µµĶ£¬CH3OH²śĀŹĻĀ½µ£¬ŌŁ½įŗĻĶ¼ĻńÅŠ¶ĻŗĻ³É¼×“¼µÄ¹¤ŅµĢõ¼ž”£
£Ø1£©øł¾ŻøĒĖ¹¶ØĀÉÖŖ£¬·“Ó¦III=·“Ó¦¢ń”Į2-·“Ó¦¢ņ£¬Ņņ“Ė£¬”÷H3=”÷H1”Į2-”÷H2=£49.6 kJ/mol”Į2-23.4 kJ/mol=-122.6 kJ/mol£»
¹Ź“š°øĪŖ£ŗ£122.6£»
£Ø2£©·“Ó¦Ģõ¼žĪŖŗćĪĀŗćČŻ£¬·“Ó¦I£ŗCO2(g)£«3H2(g)![]() CH3OH(g)£«H2O(g)ĪŖ·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæ¼õÉŁµÄ·“Ó¦£¬
CH3OH(g)£«H2O(g)ĪŖ·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæ¼õÉŁµÄ·“Ó¦£¬
A. øĆ·“Ó¦ĪŖ·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæ¼õÉŁµÄ·“Ó¦£¬Ėę×Å·“Ó¦µÄ½ųŠŠĘųĢåĪļÖŹµÄĮæ¼õÉŁ£¬ĢåĻµ×ÜŃ¹Ēæ¼õŠ”£¬Ņņ“Ėµ±·“Ó¦ĢåĻµ×ÜŃ¹Ēæ±£³Ö²»±äŹ±ÄÜĖµĆ÷·“Ó¦I“ļµ½Ę½ŗāדĢ¬£¬AĻīÕżČ·£»
B. øł¾ŻÖŹĮæŹŲŗć¶ØĀÉÖŖ»ģŗĻĘųĢåµÄ×ÜÖŹĮæ²»±ä£¬ČŻĘ÷ČŻ»żŅ²²»±ä£¬ŌņĖę×Å·“Ó¦µÄ½ųŠŠ£¬ČŻĘ÷ÄŚµÄ»ģŗĻĘųĢåµÄĆܶȏ¼ÖÕ±£³Ö²»±ä£¬Ņņ“Ėµ±·“ČŻĘ÷ÄŚµÄ»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±äŹ±²»ÄÜĖµĆ÷·“Ó¦I“ļµ½Ę½ŗāד£¬BĻī“ķĪó£»
C. µ±Ė®·Ö×ÓÖŠ¶ĻĮŃ2NAøöH£O¼üŹ±»įÓŠ3NAøöH£H¼üŠĪ³É£¬¼“Éś³É3molĒā·Ö×Ó£¬ČōĶ¬Ź±Ēā·Ö×ÓÖŠ¶ĻĮŃ3NAøöH£H¼ü£¬¼“ĻūŗÄ3molĒā·Ö×Ó£¬ŌņĒāĘųµÄĪļÖŹµÄĮæ±£³Ö²»±ä£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬Ņņ“ĖĖ®·Ö×ÓÖŠ¶ĻĮŃ2NAøöH£O¼ü£¬Ķ¬Ź±Ēā·Ö×ÓÖŠ¶ĻĮŃ3NAøöH£H¼üÄÜĖµĆ÷·“Ó¦I“ļµ½Ę½ŗāד£¬CĻīÕżČ·£»
D. ·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±ø÷ĪļÖŹµÄĪļÖŹµÄĮæÅØ¶Č±£³Ö²»±ä£¬µ«CH3OHŗĶH2OµÄÅضČÖ®±ČŹ¼ÖÕµČÓŚ1:1£¬Ņņ“ĖCH3OHŗĶH2OµÄÅضČÖ®±Č±£³Ö²»±ä²»ÄÜĖµĆ÷·“Ó¦I“ļµ½Ę½ŗāד£¬DĻīÕżČ·£»
¹Ź“š°øĪŖ£ŗAC£»
£Ø3£©“ĖæĢ·“Ó¦µÄÅضČÉĢ![]() £¬Ņņ“Ė·“Ó¦ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬vÕż>vÄę£»
£¬Ņņ“Ė·“Ó¦ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬vÕż>vÄę£»
ÉčĘšŹ¼Ź±CH3OCH3ŗĶH2OµÄĪļÖŹµÄĮæ¾łĪŖa mol£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬CH3OCH3µÄ×Ŗ»ÆĮæĪŖx mol£¬ŌņæÉĮŠ³öČż¶ĪŹ½£ŗ
CH3OCH3(g) £« H2O(g)![]() 2CH3OH(g)
2CH3OH(g)
ĘšŹ¼£Ømol£© a mol a mol 0
×Ŗ»Æ£Ømol£© x mol x mol 2x mol
Ę½ŗā£Ømol£© (a-x)mol (a-x)mol 2x mol
Ōņ»ÆŃ§Ę½ŗā³£Źż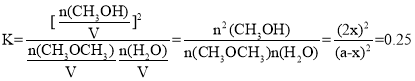 £¬½āµĆ£ŗx=0.2a£¬Ōņ»ģŗĻĘųĢåÖŠCH3OHµÄĪļÖŹµÄĮæĪŖ0.4a£¬»ģŗĻĘųĢå×ÜĪļÖŹµÄĮæ²»±äČŌĪŖ2a£¬Ņņ“Ė»ģŗĻĘųĢåÖŠCH3OHĢå»ż·ÖŹż
£¬½āµĆ£ŗx=0.2a£¬Ōņ»ģŗĻĘųĢåÖŠCH3OHµÄĪļÖŹµÄĮæĪŖ0.4a£¬»ģŗĻĘųĢå×ÜĪļÖŹµÄĮæ²»±äČŌĪŖ2a£¬Ņņ“Ė»ģŗĻĘųĢåÖŠCH3OHĢå»ż·ÖŹż![]() £»
£»
¹Ź“š°øĪŖ£ŗ£¾£»20£»
£Ø4£©ÓÉĶ¼æÉÖŖ£¬ŌŚT1ĪĀ¶ČĻĀ£¬½«6 molCO2ŗĶ12molH2³äČė2 LµÄĆܱÕČŻĘ÷ÖŠŹ±£¬CO2µÄĘ½ŗā×Ŗ»ÆĀŹĪŖ60%£¬Ņņ“ĖCO2µÄ×Ŗ»ÆĮæĪŖ6 mol”Į60%=3.6£¬ŌņÉś³ÉCH3OCH3µÄĪļÖŹµÄĮæĪŖ1.8mol£¬![]() £»
£»
»ÆŃ§Ę½ŗā³£ŹżÖ»ÓėĪĀ¶ČÓŠ¹Ų£¬ĪĀ¶Č²»±ä£¬»ÆŃ§Ę½ŗā³£Źż²»±ä£¬ŌņKA£½KC£¬ÓÉĶ¼ĻńæÉÖŖ£¬µ±Ķ¶ĮĻ±ČĻąĶ¬Ź±£¬T1ĪĀ¶ČĻĀµÄĘ½ŗā×Ŗ»ÆĀŹ½Ļ“ó£¬øĆ·“Ó¦ĪŖÕżĻņ·ÅČȵķ“Ó¦£¬½µĪĀĘ½ŗāÕżĻņŅĘ¶Æ£¬»ÆŃ§Ę½ŗā³£ŹżŌö“ó£¬Ņņ“ĖT1<T2£¬KA£½KC£¾KB£»
¹Ź“š°øĪŖ£ŗ0.18mol”¤L1”¤min1£»KA£½KC£¾KB£»
£Ø5£©¢Ł·“Ó¦IµÄ”÷H£¼0£¬ŌŚĻąĶ¬µÄŹ±¼ä¶ĪÄŚ·“Ó¦£¬230”ę·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬ÉżĪĀĘ½ŗāÄęĻņŅĘ¶Æ£¬CO2×Ŗ»Æ×Ŗ»ÆĀŹ½µµĶ£¬CH3OH²śĀŹĻĀ½µ£»
¹Ź“š°øĪŖ£ŗ·“Ó¦IµÄ”÷H£¼0ĪĀ¶ČÉżøߣ¬Ź¹CO2×Ŗ»ÆĪŖCH3OHµÄĘ½ŗā×Ŗ»ÆĀŹĻĀ½µ£»
¢ŚÓÉĶ¼ĻńæÉÖŖŌŚ230”ęĻĀCH3OHµÄ×Ŗ»ÆĀŹ×īøߣ¬“߻ƼĮCZ(Zr£1)T¶ŌCH3OHµÄŃ”ŌńŠŌ×īŗĆ£¬Ņņ“ĖŗĻ³É¼×“¼µÄ¹¤ŅµĢõ¼žŹĒ230”ę£¬“߻ƼĮCZ(Zr£1)T”£
¹Ź“š°øĪŖ£ŗBD”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀ±×åŌŖĖŲ°üĄØF”¢Cl”¢BrµČŌŖĖŲ”£
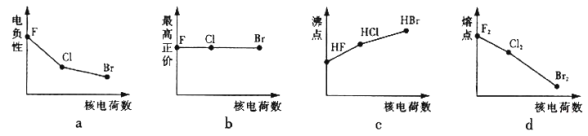
£Ø1£©ĻĀĮŠĒśĻß±ķŹ¾Ā±×åŌŖĖŲijÖÖŠŌÖŹĖęŗĖµēŗÉŹżµÄ±ä»ÆĒ÷ŹĘ£¬ÕżČ·µÄŹĒ_______”£
£Ø2£©ŌŚ²ā¶ØHFµÄĻą¶Ō·Ö×ÓÖŹĮæŹ±£¬ŹµŃé²ā¶ØÖµŅ»°ćøßÓŚĄķĀŪÖµµÄÖ÷ŅŖŌŅņŹĒ______________”£
£Ø3£©BCl3ŗĶNCl3ÖŠŠÄŌ×ÓµÄŌӻƷ½Ź½ŹĒ·ńĻąĶ¬_____________£ØĢī ŹĒ »ņ ·ń£©”£µŚŅ»µēĄėÄܽéÓŚB”¢NÖ®¼äµÄµŚ¶žÖÜĘŚŌŖĖŲÓŠ_______ÖÖ”£
£Ø4£©īī£ØRh£©ÓėµāŹōÓŚĶ¬ÖÜĘŚŌŖĖŲ”£īīµÄijÅäŗĻĪļµÄ»ÆѧŹ½ĪŖCsRh(SO4)2£¬øĆĪļÖŹŅ×ČÜÓŚĖ®£¬ĻņĘäĖ®ČÜŅŗÖŠ¼ÓČėŅ»¶ØÅØ¶ČµÄBaCl2ČÜŅŗ£¬ĪŽ³ĮµķÉś³É£¬øĆŃĪČÜÓŚĖ®µÄµēĄė·½³ĢŹ½ĪŖ___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A. ±ź×¼×“æöĻĀ£¬22.4L H2Oŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ1 NA
B. ³£ĪĀ³£Ń¹ĻĀ,1.06g Na2CO3ŗ¬ÓŠµÄNa+Ąė×ÓŹżĪŖ0.02 NA
C. ³£ĪĀ³£Ń¹ĻĀ£¬1 NA øöCO2·Ö×ÓÕ¼ÓŠµÄĢå»żĪŖ22.4L
D. ĪļÖŹµÄĮæÅضČĪŖ0.5mol/LµÄMgCl2ČÜŅŗÖŠ£¬ŗ¬ÓŠCl- øöŹżĪŖ1 NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŹµŃéŹŅŠčŅŖ1.500 mol”¤L£1ĮņĖįČÜŅŗ450 mL”£øł¾ŻČÜŅŗµÄÅäÖĘĒéæö»Ų“šĻĀĮŠĪŹĢā£ŗ
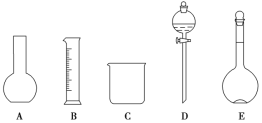
£Ø1£©ČēĶ¼ĖłŹ¾µÄŅĒĘ÷ÖŠÅäÖĘČÜŅŗæĻ¶Ø²»ŠčŅŖµÄŹĒ______(ĢīŠņŗÅ)£¬ÅäÖĘÉĻŹöČÜŅŗ»¹ŠčÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒ________(ĢīŅĒĘ÷Ćū³Ę)”£
£Ø2£©ĻÖÓĆÖŹĮæ·ÖŹżĪŖ98%”¢ĆܶČĪŖ1.84 g”¤cm£3µÄÅØĮņĖįĄ“ÅäÖĘ450 mL 1.50 mol”¤L£1µÄĻ”ĮņĖį”£¼ĘĖćĖłŠčÅØĮņĖįµÄĢå»żĪŖ________ mL (±£Įō1Ī»Š”Źż)£¬ĻÖÓŠ ¢Ł10 mL ¢Ś25 mL”” ¢Ū50 mL ¢Ü100 mLĖÄÖÖ¹ęøńµÄĮæĶ²£¬×īŗĆŃ”ÓƵÄĮæĶ²ŹĒ________(Ģī“śŗÅ)”£
£Ø3£©ÅäÖĘŹ±£¬Ņ»°ćæÉ·ÖĪŖŅŌĻĀ¼øøö²½Öč£ŗ
¢ŁĮæČ”””¢Ś¼ĘĖć””¢ŪĻ”ŹĶ””¢ÜŅ”ŌČ””¢Ż×ŖŅĘ””¢ŽĻ“µÓ””¢ß¶ØČŻ””¢ąĄäČ“
ĘäÕżČ·µÄ²Ł×÷Ė³ŠņĪŖ£ŗ¢Ś”ś¢Ł”ś¢Ū”ś___”ś_____”ś_____”ś______”ś¢Ü(ĢīŠņŗÅ)”£
£Ø4£©ŌŚÅäÖĘ¹ż³ĢÖŠ£¬ĻĀĮŠ²Ł×÷ÖŠ»įµ¼ÖĀĖłÅäÖʵÄČÜŅŗÅضČĘ«øßµÄÓŠ________”£
¢ŁÓĆĮæĶ²ĮæČ”ÅØĮņĖįŹ±ŗņ£¬ø©ŹÓæĢ¶ČĻß
¢ŚĻ“µÓĮæČ”ÅØĮņĖįŗóµÄĮæĶ²£¬²¢½«Ļ“µÓŅŗ×ŖŅʵ½ČŻĮæĘæÖŠ
¢Ū×ŖŅĘĒ°£¬ČŻĮæĘæÖŠŗ¬ÓŠÉŁĮæÕōĮóĖ®
¢Ü¶ØČŻŹ±£¬ø©ŹÓæĢ¶ČĻß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³ŃłĘ·Ö÷ŅŖŗ¬KClŗĶÉŁĮæMgCl2”¢CaCl2”¢MgSO4µČ£¬ŠčŅŖ·ÖĄėĢį“æµĆµ½KCl”£
£Ø1£©ŹµŃéŹŅ²ÉÓĆ³Įµķ·Ø²ā¶Øѳʷ֊MgSO4µÄÖŹĮæ·ÖŹż”£²Ł×÷²½ÖčČēĻĀ£ŗ
¢ŁČ”10gѳʷČÜÓŚĖ®ÖŠ£¬¼ÓČė×ćĮæµÄBaCl2ČÜŅŗ£¬³ä·Ö½Į°č·“Ó¦£»¢Ś½«ĖłµĆ»ģŗĻĪļ¹żĀĖ”¢Ļ“µÓ”£¢Ū½«³ĮµķĮ¬Ķ¬ĀĖÖ½Č”³ö·ÅČėŪįŪöÖŠ×ĘÉÕÖĮŗćÖŲ£ØĀĖÖ½ĶźČ«×Ŗ»Æ³ÉCO2ŗĶĖ®£¬³Įµķ²»·Ö½ā£©¢ÜĄäČ“ŗó³ĘĮæĖłµĆ³ĮµķÖŹĮæĪŖ0.466g”£
ÅŠ¶Ļ³ĮµķŹĒ·ńĻ“µÓøɾ»µÄ·½·ØŹĒ_______________£»ŃłĘ·ÖŠMgSO4µÄÖŹĮæ·ÖŹżĪŖ________”£
£Ø2£©ĻÖÓŠ¼øÖÖŹŌ¼Į£ŗ¢ŁŃĪĖį£»¢ŚK2CO3£»¢ŪNa2CO3£»¢ÜNaOH£»¢ŻKOH£»¢ŽBa(OH)2£»¢ßBaCl2£»ĪŖÓŠŠ§³żČ„ѳʷ֊µÄŌÓÖŹ£¬¼ÓČėµÄŹŌ¼Į¼°Ė³ŠņŗĻĄķµÄŹĒ____________£¬
A£®¢ß¢Ū¢Ü B£®¢ß¢Ż¢Ś C£®¢Ś¢Ž D£®¢Ż¢Ś¢ß
¹żĀĖ³żČ„³Įµķŗ󻹊čŅŖ¼ÓČėµÄŹŌ¼ĮĪŖ_________ (ĢīŠņŗÅ)£¬Č»ŗó½ųŠŠÕō·¢½į¾§”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄų”¢īÜ”¢īŃ”¢ĶµČŌŖĖŲ³£ÓĆ×÷Öʱøļ®Ąė×Óµē³ŲµÄÕż¼«²ÄĮĻ»ņøߊ§“߻ƼĮ”£NA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬ĒėĢīŠ“ĻĀĮŠæÕ°×”£
£Ø1£©»łĢ¬CoŌ×ӵĵē×ÓÅŲ¼Ź½ĪŖ___”£
£Ø2£©ÄųÓėCOÉś³ÉµÄÅäŗĻĪļNi(CO)4ÖŠ£¬Ņ×Ģį¹©¹Āµē×Ó¶ŌµÄ³É¼üŌ×ÓŹĒ___£ØĢīŌŖĖŲĆū³Ę£©£»1 molNi(CO)4ÖŠŗ¬ÓŠµÄ¦Ņ¼üŹżÄæĪŖ__£»Š“³öÓėCO»„ĪŖµČµē×ÓĢåµÄŅ»ÖÖŅõĄė×ӵĻÆѧŹ½_____”£
£Ø3£©Ti(BH4)2ŹĒŅ»ÖÖ“¢Ēā²ÄĮĻ”£BH4-µÄæռ乹ŠĶŹĒ____£¬BŌ×ÓµÄŌӻƷ½Ź½__”£ÓėīŃĶ¬ÖÜĘŚµÄµŚ¢ņB×åŗĶ¢óA×åĮ½ÖÖŌŖĖŲÖŠµŚŅ»µēĄėÄܽĻ“óµÄŹĒ___£ØŠ“ŌŖĖŲ·ūŗÅ£©£¬ŌŅņŹĒ____”£
£Ø4£©CuFeS2µÄ¾§°ūČēĶ¼ĖłŹ¾£¬¾§°ū²ĪŹż·Ö±šĪŖanm”¢bnm”¢cnm£»CuFeS2µÄ¾§°ūÖŠĆæøöCuŌ×ÓÓė___øöSŌ×ÓĻąĮ¬£¬¾§ĢåĆÜ¶Č¦Ń£½___g”¤cm3£ØĮŠ³ö¼ĘĖć±ķ“ļŹ½£©”£

ŅŌ¾§°ū²ĪŹżĪŖµ„Ī»³¤¶Č½ØĮ¢µÄ×ų±źĻµæÉŅŌ±ķŹ¾¾§°ūÖŠø÷Ō×ÓµÄĪ»ÖĆ£¬³Ę×÷Ō×Ó·ÖŹż×ų±ź£¬ĄżČēĶ¼ÖŠŌ×Ó2ŗĶ3µÄ×ų±ź·Ö±šĪŖ£Ø0£¬1£¬![]() £©”¢£Ø
£©”¢£Ø![]() £¬
£¬![]() £¬0£©£¬ŌņŌ×Ó1µÄ×ų±źĪŖ___”£
£¬0£©£¬ŌņŌ×Ó1µÄ×ų±źĪŖ___”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼×°·(CH3NH2)ŹĒŅ»ÖÖŅ»ŌŖČõ¼ī£¬ĘäµēĄė·½³ĢŹ½ĪŖ£ŗCH3NH2 + H2O ![]() CH3NH3+ + OH£”£³£ĪĀĻĀ£¬Ļņ20.0 mL 0.10 mol/LµÄ¼×°·ČÜŅŗÖŠµĪ¼ÓVmL0.10mol/LµÄĻ”ŃĪĖį£¬»ģŗĻČÜŅŗµÄpHÓėĻą¹ŲĪ¢Į£ÅØ¶ČµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ
CH3NH3+ + OH£”£³£ĪĀĻĀ£¬Ļņ20.0 mL 0.10 mol/LµÄ¼×°·ČÜŅŗÖŠµĪ¼ÓVmL0.10mol/LµÄĻ”ŃĪĖį£¬»ģŗĻČÜŅŗµÄpHÓėĻą¹ŲĪ¢Į£ÅØ¶ČµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ
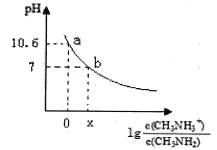
A. bµć¶ŌÓ¦¼ÓČėŃĪĖįµÄĢå»żV<20.00mL
B. ³£ĪĀĻĀ£¬øł¾ŻaµćæÉÖŖ¼×°·µÄµēĄėĘ½ŗā³£ŹżKb=10 -3£®4
C. bµćæÉÄÜ“ęŌŚ¹ŲĻµ£ŗc(Cl£) > c(CH3NH3+) > c(H+) = c(OH£)
D. V=20.00mLŹ±£¬ČÜŅŗ³ŹČõĖįŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŗćĪĀ”¢ČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠĶØČė1 mol XŗĶ2 mol Y£¬·¢Éś·“Ó¦£ŗX(g)£«2Y(g)![]() M(g)””¦¤H£½£a kJ/mol(a>0)£¬5 minÄ©²āµĆMµÄĪļÖŹµÄĮæĪŖ0£®4 mol”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
M(g)””¦¤H£½£a kJ/mol(a>0)£¬5 minÄ©²āµĆMµÄĪļÖŹµÄĮæĪŖ0£®4 mol”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. 0”«5 min£¬YµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0£®08 mol”¤L£1”¤min£1
B. µ±ČŻĘ÷ÖŠ»ģŗĻĘųĢåĆÜ¶Č²»±äŹ±“ļµ½Ę½ŗāדĢ¬
C. Ę½ŗāŗóÉżøßĪĀ¶Č£¬XµÄ·“Ó¦ĖŁĀŹ½µµĶ
D. µ½“ļĘ½ŗāדĢ¬Ź±£¬·“Ó¦·Å³öµÄČČĮæĪŖa kJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹµÄ×Ŗ»ÆŌŚøų¶ØĢõ¼žĻĀÄÜŹµĻֵďĒ
A. Na![]() Na2O
Na2O![]() Na2CO3
Na2CO3
B. Al![]() Al2O3
Al2O3![]() Al(OH)3
Al(OH)3
C. Fe(OH)2![]() Fe(OH)3
Fe(OH)3![]() Fe2O3
Fe2O3
D. Na2CO3(aq)![]() NaHCO3
NaHCO3![]() CO2
CO2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com