
 ĄķĀŪÉĻČĪŗĪ×Ō·¢µÄŃõ»Æ»¹Ō·“Ó¦¶¼æÉŅŌÉč¼Ę³ÉŌµē³Ų£®ĻÖŹ¹ÓĆŠæµē¼«”¢Ķµē¼«”¢³Č×Ó£ØĖįŠŌ½éÖŹ£©Éč¼ĘČēĶ¼ĖłŹ¾µÄĖ®¹ūµē³Ų£®
ĄķĀŪÉĻČĪŗĪ×Ō·¢µÄŃõ»Æ»¹Ō·“Ó¦¶¼æÉŅŌÉč¼Ę³ÉŌµē³Ų£®ĻÖŹ¹ÓĆŠæµē¼«”¢Ķµē¼«”¢³Č×Ó£ØĖįŠŌ½éÖŹ£©Éč¼ĘČēĶ¼ĖłŹ¾µÄĖ®¹ūµē³Ų£®·ÖĪö £Ø1£©ŠæĪŖøŗ¼«£¬±»Ńõ»ÆÉś³ÉŠæĄė×Ó£»
£Ø2£©¢Ł×é³ÉĖ®¹ūµē³Ųøŗ¼«µÄ½šŹōŠŌ“óÓŚÕż¼«¼“æÉ£¬Õż¼«ÉĻĒāĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£»
¢ŚČō×é³É¼īŠŌµē³Ų£¬Ōņøŗ¼«²ÄĮĻŹĒAl£¬Õż¼«²ÄĮĻŹĒÄܵ¼µēµÄĪļÖŹ¼“æÉ£®
½ā“š ½ā£ŗ£Ø1£©»īĘĆ½šŹōZn×÷Ōµē³ŲµÄøŗ¼«£¬·¢ÉśŃõ»Æ·“Ó¦£¬µē¼«·½³ĢŹ½ĪŖ£¬¹Ź“š°øĪŖ£ŗŠæ»ņZn£»Zn-2e-=Zn2+£»
£Ø2£©¢ŁĖįŠŌĖ®¹ūµē³ŲÖŠ£¬øŗ¼«ÄÜŗĶĖį·“Ó¦£¬Ōņøŗ¼«²ÄĮĻæÉŅŌŹĒĆ¾»ņĀĮ£¬Õż¼«ÉĻĒāĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£¬µē¼«·“Ó¦Ź½ĪŖ2H++2e-=H2”ü£¬
¹Ź“š°øĪŖ£ŗAB£»2H++2e-=H2”ü£»
¢ŚČō×é³É¼īŠŌµē³Ų£¬Ōņøŗ¼«²ÄĮĻŹĒAl£¬Õż¼«²ÄĮĻŹĒÄܵ¼µēµÄĪļÖŹ¼“æÉ£¬ĖłŅŌÕż¼«æÉŅŌŹĒĆ¾”¢Ķ»ņĢ¼°ō£¬¼ŁÉčĖ®¹ūµÄ¼īŠŌ½ĻĒ棬µē³ŲµÄøŗ¼«·“Ó¦Ź½ĪŖ
¹Ź“š°øĪŖ£ŗABD£»Al-3e-+4OH-=AlO2-+2H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌµē³ŲŌĄķÕżøŗ¼«µÄÅŠ¶Ļ¼°µē¼«·“Ó¦Ź½µÄŹéŠ“£¬øł¾ŻČÜŅŗÖŠµē¼«²ÄĮĻµĆŹ§µē×ÓµÄÄŃŅ׳Ģ¶ČČ·¶ØÕżøŗ¼«£¬×¢Ņā²»ÄÜøł¾Ż½šŹōµÄ»ī¶ÆŠŌĒæČõÅŠ¶ĻÕżøŗ¼«£¬ĪŖŅדķµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
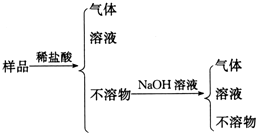
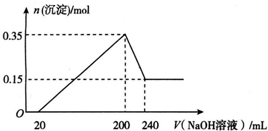 ½«Ņ»¶ØÖŹĮæµÄĆ¾ŗĶĀĮ»ģŗĻĪļĶ¶Čė200 mLĻ”ĮņĖįÖŠ£¬¹ĢĢåČ«²æČܽāŗó£¬ĻņĖłµĆČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓė¼ÓČėµÄNaOHČÜŅŗĢå»żµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£®ŌņĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
½«Ņ»¶ØÖŹĮæµÄĆ¾ŗĶĀĮ»ģŗĻĪļĶ¶Čė200 mLĻ”ĮņĖįÖŠ£¬¹ĢĢåČ«²æČܽāŗó£¬ĻņĖłµĆČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓė¼ÓČėµÄNaOHČÜŅŗĢå»żµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£®ŌņĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | Ć¾ŗĶĀĮµÄ×ÜÖŹĮæĪŖ9 g | |
| B£® | ×ī³õ20 mL NaOHČÜŅŗÓĆÓŚÖŠŗĶ¹żĮæµÄĻ”ĮņĖį | |
| C£® | ĒāŃõ»ÆÄĘČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ5 mol•L-1 | |
| D£® | Éś³ÉµÄĒāĘųŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ11.2 L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

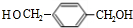 £®ÉĻŹö·“Ó¦ÖŠŹōÓŚČ”“ś·“Ó¦µÄŹĒ¢Ł¢Ś£ØĢīŹż×ÖŠņŗÅ£©£®
£®ÉĻŹö·“Ó¦ÖŠŹōÓŚČ”“ś·“Ó¦µÄŹĒ¢Ł¢Ś£ØĢīŹż×ÖŠņŗÅ£©£® +2NaOH$”ś_{”÷}^{H_{2}O}$
+2NaOH$”ś_{”÷}^{H_{2}O}$ +2NaCl£»
+2NaCl£» +O2$”ś_{”÷}^{Cu}$
+O2$”ś_{”÷}^{Cu}$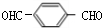 +2H2O£®
+2H2O£® £®
£®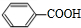 £®
£®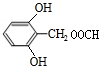 »ņ
»ņ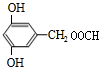 £ØŠ“³öŅ»ÖÖ£©£®
£ØŠ“³öŅ»ÖÖ£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
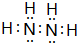 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¾ĆÖĆŌŚæÕĘųÖŠµÄNaOHČÜŅŗ£¬¼ÓŃĪĖįŹ±ÓŠĘųĢå²śÉś | |
| B£® | 50 mL 12 mol•L-1µÄÅØŃĪĖįÓė×ćĮæµÄMnO2·“Ó¦£¬Éś³É0.15 mol Cl2 | |
| C£® | ŌŚ³£ĪĀĻĀ£¬ÅØH2SO4²»ÓėCu·“Ó¦£¬ŹĒŅņĪŖĶ±»¶Ū»Æ | |
| D£® | CO2ĶØČėÅصÄCaCl2ČÜŅŗÖŠ²śÉś°×É«³Įµķ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ĻīÄæ | ČŪµć/”ćC | ĆܶČ/ £Øg•cm-3£© | Ó²¶Č£Ø½šøÕ ŹÆĪŖ10£© | µ¼µēŠŌ £ØŅųĪŖ100£© |
| ijŗĻ½š | 2 500 | 3.00 | 7.4 | 2.3 |
| Ģś | 1 535 | 7.86 | 4.5 | 17 |
| A£® | µ¼Ļß | B£® | ĆÅ“°æņ | C£® | ĀÆ¾ß | D£® | ·É»śĶāæĒ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Al”¢Cu”¢Mg”¢Si | B£® | Al”¢Mg”¢Si”¢Zn | C£® | Al”¢Fe”¢C”¢Cu | D£® | Al”¢Si”¢Zn”¢Na |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
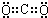 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com