
| A. | 液氨气化 | B. | 钠与水反应 | C. | 碳酸钙分解 | D. | 化学键的断裂 |
分析 放出热量的过程可以是放热反应,也可以是放热的物理过程;
常见的放热反应有:绝大多数的化合反应、所有的燃烧、金属和水或酸的反应、酸碱中和反应、铝热反应;
常见的放热的物理过程有:浓硫酸用水稀释;氢氧化钠固体溶于水;物质由气态→液态→固态,据此进行分析.
解答 解:A.液态物质具有能量小于气态,则液氨气化吸收热量,故A错误;
B.钠与水反应生成氢氧化钠和氢气,该反应为放热反应,故B正确;
C.碳酸钙在高温下分解生成氧化钙和二氧化碳,该反应为吸热反应,故C错误;
D.化学键旧键断裂需要吸收热量,故D错误;
故选B.
点评 本题考查了反应热与焓变的应用,题目难度不大,明确常见化学反应与能量变化的关系为解答关键,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
| HClO | HSCN | H2CO3 |
| K=3.2×10-8 | K=0.13 | K1=4.3×10-7 K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用装置来制备.
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用装置来制备.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +HCl
+HCl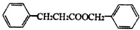 ;检验M中官能团的试剂是银氨溶液或新制备氢氧化铜浊液.
;检验M中官能团的试剂是银氨溶液或新制备氢氧化铜浊液.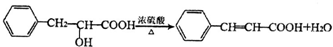 ,
, .
.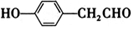 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯分子中无碳碳双键,苯不能发生加成反应 | |
| B. | 甲烷能与氯水发生取代反应 | |
| C. | 乙醇在一定条件下能被氧化成乙醛 | |
| D. | 乙烯和苯均能与溴水反应而使其褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
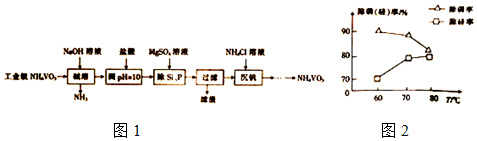
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
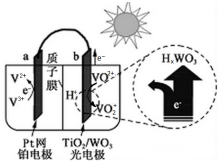
| A. | 光照时,太阳能主要转化为电能 | |
| B. | 光照时,b极的电极反应式为VO2+-e-+H2O═VO2++2H+ | |
| C. | 光照时,每转移5 mol电子,有5mol H+由b极区向a极区迁移 | |
| D. | 夜间,a极的电极反应式为V3++e-═V2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯甲酸和苯甲酸钠都是食品防腐剂 | |
| B. | 食用花生油和汽油都属于酯 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 毛发、鸡蛋清都不能发生水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com