
 Ni(CO)4(g)
Ni(CO)4(g)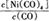 减小,则?H 0(填“>”或“<”)。
减小,则?H 0(填“>”或“<”)。
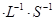 。
。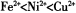 )
)
 Ni2++S。
Ni2++S。 Ni(CO)4(g),当温度升高时,
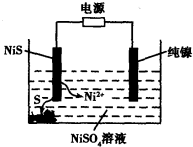
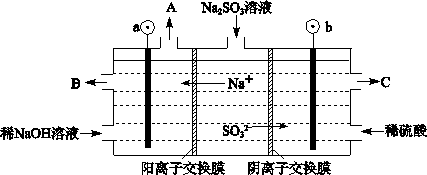
Ni(CO)4(g),当温度升高时,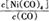 减小,说明平衡逆向移动,升高温度平衡向吸热反应方向移动,则该反应的逆向吸热,正向为放热反应,?H<0;②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,a.随着反应的进行,容器内气体的质量增大,物质的量减小,等压条件下容器体积减小,密度逐渐增大,达平衡时密度不变,与图像不符,错误;b.随着反应的减小,反应物的浓度逐渐减小,正反应速率逐渐减小,达平衡时正反应速率不变,与图像符合,正确;c.?H不随反应的进行而变化,不能作为平衡标志,错误;d.CO的转化率随反应的进行不断增大,达平衡时CO的转化率不变,与图像相符,正确,选bd;若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,影响平衡常数的外界因素为温度,温度不变,平衡常数不变;根据公式v=△n/V△t将题给数据代入计算得v(Ni(CO)4)=0.2mol﹒L—1﹒S—1,则0—3s内的平均反应速率v(CO)=0.8mol﹒L—1﹒S—1。③要提高上述反应中CO的转化率,同时增大反应速率,可采取的措施为增大CO的浓度或增大压强。(2)迁移教材知识铜的电解精炼作答。以NiSO4溶液为电解质溶液进行粗镍(含Fe、Zn、Cu、Pt、Au等杂质)的电解精炼, a.电解过程中,电能转化为化学能,错误;b.粗镍作阳极,发生氧化反应,错误;c.精炼过程中比镍活泼的金属Fe、Zn以离子形式进入电解质溶液,活泼性比镍弱的金属Cu、Pt、Au进入阳极泥,正确;d.粗镍精炼时通过的电量与阴极析出镍的质量成正比,正确,选cd;(3) 根据题意知,电解时,硫化镍中的硫元素以单质形态沉积在某电极附近,硫元素的化合价由—2价升高为0价,发生氧化反应,作电解池的阳极,与电源的正极相接。阳极的电极反应式为NiS—2e-
减小,说明平衡逆向移动,升高温度平衡向吸热反应方向移动,则该反应的逆向吸热,正向为放热反应,?H<0;②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,a.随着反应的进行,容器内气体的质量增大,物质的量减小,等压条件下容器体积减小,密度逐渐增大,达平衡时密度不变,与图像不符,错误;b.随着反应的减小,反应物的浓度逐渐减小,正反应速率逐渐减小,达平衡时正反应速率不变,与图像符合,正确;c.?H不随反应的进行而变化,不能作为平衡标志,错误;d.CO的转化率随反应的进行不断增大,达平衡时CO的转化率不变,与图像相符,正确,选bd;若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,影响平衡常数的外界因素为温度,温度不变,平衡常数不变;根据公式v=△n/V△t将题给数据代入计算得v(Ni(CO)4)=0.2mol﹒L—1﹒S—1,则0—3s内的平均反应速率v(CO)=0.8mol﹒L—1﹒S—1。③要提高上述反应中CO的转化率,同时增大反应速率,可采取的措施为增大CO的浓度或增大压强。(2)迁移教材知识铜的电解精炼作答。以NiSO4溶液为电解质溶液进行粗镍(含Fe、Zn、Cu、Pt、Au等杂质)的电解精炼, a.电解过程中,电能转化为化学能,错误;b.粗镍作阳极,发生氧化反应,错误;c.精炼过程中比镍活泼的金属Fe、Zn以离子形式进入电解质溶液,活泼性比镍弱的金属Cu、Pt、Au进入阳极泥,正确;d.粗镍精炼时通过的电量与阴极析出镍的质量成正比,正确,选cd;(3) 根据题意知,电解时,硫化镍中的硫元素以单质形态沉积在某电极附近,硫元素的化合价由—2价升高为0价,发生氧化反应,作电解池的阳极,与电源的正极相接。阳极的电极反应式为NiS—2e- Ni2++S。
Ni2++S。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.v(O2)=0.01mol·L-1·s-1 | B.v(NO)="0.008" mol·L-1·s-1 |
| C.v(H2O)="0.003" mol·L-1·s-1 | D.v(NH3)="0.004" mol·L-1·s-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.压缩体积,增大压强 | B.降低温度 | C.充入大量的氮气 | D.仅增加SO2的浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g) △H=-196kJ/mol,提高反应中SO2的转化率,是减少SO2排放的有效措施。
2SO3(g) △H=-196kJ/mol,提高反应中SO2的转化率,是减少SO2排放的有效措施。| A.SO2、O2、SO3三者的浓度之比为2∶1∶2 | B.容器内气体的压强不变 |
| C.容器内混合气体的密度保持不变 | D.SO3的物质的量不再变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是
30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是 | A.V(O2)=0.01mol·L-1·s-1 | B.V(NO)=0.08mol·L-1·s-1 |
| C.V(H2O)=0.01mol·L-1·s-1 | D.V(NH3)=0.002mol·L-1·s-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
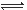 2Z(g),下列说法正确的是 ( )
2Z(g),下列说法正确的是 ( )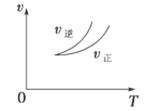
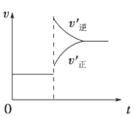
| A.左上图说明正反应为吸热反应 |
| B.反应达平衡后,增大压强气体密度将减小 |
| C.右上图可表示升高温度使平衡向逆反应方向移动 |
| D.右上图虚线可表示使用催化剂后引发的反应速率变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 的硝酸反应的化学方程式:______________________.
的硝酸反应的化学方程式:______________________.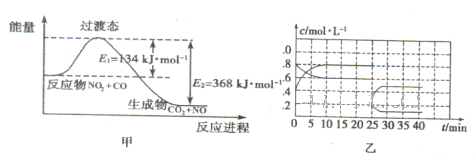
 N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。| A.加入催化剂 | B.缩小容器体积 | C.降低温度 | D.再加入一定量的NO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C来说,下列反应速率最快的是:( )
2C来说,下列反应速率最快的是:( ) 查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

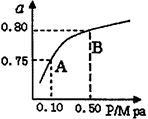
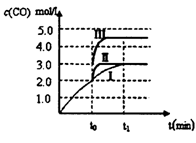
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com