
分析 (1)含有碳碳不饱和键、醛基的有机物能和溴发生反应,含有碳碳不饱和键、醛基、连接苯环的碳原子上含有氢原子的苯的同系物都能与酸性高锰酸钾溶液氧化;
(2)苯、甲苯和溴水不反应,但在溴化铁作催化剂条件下能与液溴反应;
(3)含有碳碳双键的烯烃能与溴水及酸性高锰酸钾溶液反应;
(4)连接苯环的碳原子上含有氢原子的苯的同系物都能与酸性高锰酸钾溶液氧化.
解答 解:(1)含有碳碳不饱和键、醛基的有机物能和溴发生反应,含有碳碳不饱和键、醛基、连接苯环的碳原子上含有氢原子的苯的同系物都能与酸性高锰酸钾溶液氧化,所以己烷和苯都不与溴水和酸性高锰酸钾溶液反应,故答案为:己烷和苯;
(2)苯、甲苯和溴水不反应,但在溴化铁作催化剂条件下能与液溴反应,发生的反应为取代反应,故答案为:苯、甲苯;取代;
(3)含有碳碳双键的烯烃能与溴水及酸性高锰酸钾溶液反应,所以己烯能与溴水和酸性高锰酸钾溶液反应,前者是加成反应、后者是氧化反应,故答案为:己烯;加成反应;氧化反应;
(4)连接苯环的碳原子上含有氢原子的苯的同系物都能与酸性高锰酸钾溶液氧化,甲苯和溴水不反应,但能和酸性高锰酸钾溶液反应而使酸性高锰酸钾溶液褪色,故答案为:甲苯.
点评 本题考查有机物结构和性质,为高频考点,明确官能团和性质关系是解本题关键,注意:并不是所有的苯的同系物都能被酸性高锰酸钾溶液氧化,为易错点.


科目:高中化学 来源: 题型:填空题
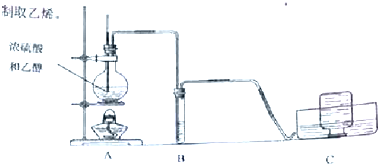
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、CuSO4•5H2O、苛性钾 | B. | 硫酸、空气、纯碱 | ||
| C. | 硝酸、食盐水、烧碱 | D. | 氧化铁、胆矾、熟石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个自发反应,反应物的总能量必须高于生成物的总能量 | |
| B. | 在等温条件下,化学反应的热效应称为焓变 | |
| C. | 化学反应中,发生能量变化的根本原因是化学键的断裂与形成 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
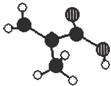 北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )
北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )| A. | 该产品的名称是甲基丙酸 | |
| B. | 该产品与硬脂酸互为同系物 | |
| C. | 四个黑球一定在同一个平面上 | |
| D. | 一定条件下,可以与乙二醇发生酯化反应,也可与氯化氢发生加成反应且产物只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com