
����Ŀ��1��2����������������Ϳ����������Ӽ���������������ɫҺ�壬�е�131.4�棬�۵�9.79�棬������ˮ�������ڴ����ѡ���ͪ���л��ܼ�����ʵ���п�����ͼ9��ʾװ���Ʊ�1��2���������飮���з�Һ©������ƿa��װ���Ҵ���Ũ����Ļ��Һ���Թ�d��װ��Ũ�壨���渲������ˮ��������д���пհף�
��1����ƿaҪ���¶�Ѹ�����ߵ�170�淢����Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ���÷�Ӧ����Ϊ ��
��2��д���Ʊ�1��2����������Ļ�ѧ����ʽ ��
��3����ȫƿb���Է�ֹ�����������Լ��ʵ�����ʱ�Թ�d�Ƿ�����������д����������ʱƿb�е����� ��
��4������c��NaOH��Һ����������eװ����NaOH��Һ�������� ��
��5��ijѧ������ʵ��ʱ��ʹ��һ������Һ�壬����ȫ����ɫʱ���������Ҵ���Ũ������Һ����������������³������࣬���װ�õ�������û�����⣬�Է�������ܵ�ԭ������2�㣩 �� 
���𰸡�
��1��CH3CH2OH ![]() CH2=CH2��+H2O����ȥ��Ӧ
CH2=CH2��+H2O����ȥ��Ӧ
��2��CH2=CH2+Br2��CH2BrCH2Br
��3��b��ˮ����½�,�������е�ˮ��������,�������
��4��������ϩ�����к��е�CO2��SO2��������������HBr��Br2������,��ֹ������Ⱦ
��5������ϩ���ٹ���,δ��ȫ�����ӳɷ�Ӧ����ʵ�������,��ϩ��Ũ����Ļ��Һû��Ѹ�ٴﵽ170��,��������Ӧ��������
���������⣺��1���Ҵ���170��ʱ������ȥ��Ӧ������ϩ���¶ȱ�����170�棬��Ӧ����ʽ��CH3CH2OH ![]() CH2=CH2��+H2O��
CH2=CH2��+H2O��
���Դ��ǣ�CH3CH2OH ![]() CH2=CH2��+H2O����ȥ��Ӧ����2����ϩ��Һ�巢���ӳɷ�Ӧ����1��2���������黯ѧ����ʽΪ��CH2=CH2+Br2��CH2BrCH2Br��
CH2=CH2��+H2O����ȥ��Ӧ����2����ϩ��Һ�巢���ӳɷ�Ӧ����1��2���������黯ѧ����ʽΪ��CH2=CH2+Br2��CH2BrCH2Br��
���Դ��ǣ�CH2=CH2+Br2��CH2BrCH2Br����3���Թ�d��������ʱ��b��ѹǿ�������ᵼ��b��ˮ���½����������е�ˮ�����������������
���Դ��ǣ�b��ˮ����½����������е�ˮ���������������������4��װ��c������������Һ������������ϩ�����к��е�CO2��SO2�����������÷�Ӧ��ʣ����廯�⼰��Ӧ�������嵥�ʵ��ж�������Ⱦ������Ӧ�ý���β�����գ�����װ��e������������Һ������������HBr��Br2�����壬��ֹ������Ⱦ��
���Դ��ǣ�������ϩ�����к��е�CO2��SO2��������������HBr��Br2�����壬��ֹ������Ⱦ����5������ȫ����ɫʱ���������Ҵ���Ũ������Һ����������������³��������ԭ���������ϩ��������ͨ��Һ�壩�ٶȹ��죬���´���ϩû�к��巢����Ӧ������ʵ������У��Ҵ���Ũ����Ļ��Һû��Ѹ�ٴﵽ170��ᵼ�¸���Ӧ�ķ�������������ɣ�
���Դ��ǣ�����ϩ���ٹ��죬δ��ȫ�����ӳɷ�Ӧ����ʵ������У���ϩ��Ũ����Ļ��Һû��Ѹ�ٴﵽ170�棬��������Ӧ�������ѣ�


 �ľ�ͼ���ʱ�ȷ�ϵ�д�
�ľ�ͼ���ʱ�ȷ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1mol/L��NaOH��Һ�ζ���ͬŨ�ȵ�һԪ����HA20mL���ζ���������Һ��pH��ζ�����(�ζ�����= ![]() ) �ı仯������ͼ��ʾ(�����к���ЧӦ),����˵������ȷ����
) �ı仯������ͼ��ʾ(�����к���ЧӦ),����˵������ȷ����
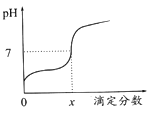
A. HA��Һ��ˮϡ�ͺ���Һ��c(HA)/c(A-)��ֵ����
B. ���ζ�����Ϊ1ʱ����Һ��ˮ�ĵ���̶����
C. ���ζ���������1ʱ����Һ������Ũ�ȹ�ϵһ����c(Na+)>c(A-)>c(OH-)> c(H+)
D. ���ζ�����Ϊxʱ��HA�ĵ��볣��ΪKHA=(10-7x)/(1-x)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�������ʵ�ת����ϵ��ijЩ��Ӧ���������ֲ�������ȥ����A��GΪ�ճ������еij���������B��C��E��I��JΪ���壬����CΪ����ɫ���壬MΪ���ɫ���塣
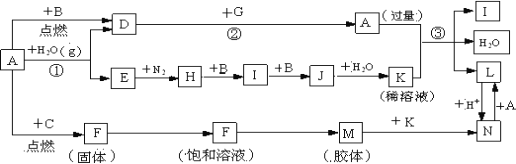
��1����֪AΪ��26��Ԫ�أ���д��AԪ�������ڱ��е�λ��__________��
��2��D��G��Ӧ�Ļ�ѧ����ʽ____________________��ʵ���������÷�Ӧ�IJ���___________��
��3����Ӧ�����ӷ���ʽ__________________________��
��4��H��I�Ļ�ѧ����ʽ_______________��
��5���ֽ�һ�Թ�J���嵹����ˮ����һ��ʱ���ˮ������������������ʹˮ���������Թܣ�Ӧ���Թ���ͨ��һ����__________��������Ļ�ѧʽ������ʱ�Թ�����Һ��Ũ��Ϊ________mol/L�������������״�����㣩��������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧʵ���Ҳ����ķ�Һ�к���Fe3+��Cu2+��Ba2+��Cl���������ӣ���������з����Է�Һ���д������Ի��ս������Ʊ��Ȼ������Ȼ������壮 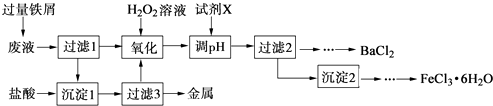
��1������1�к��еĽ��������� ��
��2������ʱ����H2O2��Һ������Ӧ�����ӷ���ʽΪ ��
��3�����������У�������Ϊ�Լ�X������ ��������ĸ����
A.BaCl2
B.BaCO3
C.NaOH
D.Ba��OH��2
��4���������2ϴ���Ƿ���ȫ�ķ����� ��
��5���Ʊ��Ȼ�������������豣�������������Ŀ���� ��
��6���ɹ���2�õ�����Һ�Ʊ�BaCl2��ʵ���������Ϊ����ȴ�ᾧ����ϴ�ӡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ֲ��֦Ҷ��ȡ�ľ����к��мס������ֳɷ֣� ![]()
��1���������Ը��������Һ��������к���̼̼˫���������Ƿ����������С������С����� ����д����һ����ͬʱ��������3��������ͬ���칹��Ľṹ��ʽ ��
a����������������ͬ��ȡ����
b������Br2��CCl4��Һ�����ӳɷ�Ӧ
c����FeCl3��Һ������ɫ
��2���ɼ�ת��Ϊ�ҵĹ���Ϊ������ȥ�ز���� 
�����ķ�Ӧ����Ϊ �� Y�Ľṹ��ʽ �� ��Ʋ�����Ŀ���� ��
��3��1mol�������� mol H2�����ӳɷ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£������Ϊ2L���ܱ������г���1mol A��b mol B���壬�������·�Ӧ��A��g��+B��g��2C��g����5min��Ӧ�ﵽƽ��ʱn��A��Ϊ0.4mol���ڷ�Ӧ��������ϵ���¶ȳ������ߣ�ʵ���û��������C�ĺ������¶ȵĹ�ϵ����ͼ��ʾ������������ȷ���ǣ������� 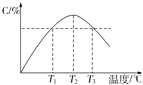
A.0��5 min��C���ʵ�ƽ����Ӧ����Ϊ0.04 molL��1min��1
B.ͼ���¶�T1ʱ������Ӧ���ʵ����¶�T3ʱ������Ӧ����
C.�÷�Ӧ�¶�T2ʱ��ƽ�ⳣ�������¶�T3ʱ��ƽ�ⳣ��
D.ͼ��T2ʱ����ֻ����ѹǿ���������淴Ӧ���ʲ��ı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������ʵ���̶ȵ��������������=���ѵ���ĵ���ʵ����ʵ���/ԭ���ܵ����ʵ�������100%����ȡ20mL pH=3�� CH3COOH��Һ������0.2molL��1�İ�ˮ�������Һ�����Ա仯��ͼ������백ˮǰCH3COOH�ĵ����Ϊ�������� 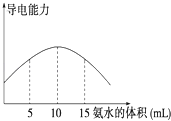
A.0.5%
B.1.5%
C.0.1%
D.1%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�������ữ�IJ��ᣨH2C2O4����Һ����KMnO4��Һ��Ӧ��ij��ѧС���о����֣�����MnSO4�ɶԸ÷�Ӧ������ã�Ϊ��һ���о��й����ضԸ÷�Ӧ���ʵ�Ӱ�죬̽�����£�
��1�������£�̽����ͬ�ij�ʼpH�Ͳ�����ҺŨ�ȶԷ�Ӧ���ʵ�Ӱ�죬�������ʵ�飬��A= �� C= �� E=
ʵ���� | �¶� | ��ʼpH | 0.1mol/L������Һ���/mL | 0.01mol/LKMnO4 | ����ˮ���/mL | �������ݣ����Һ��ɫʱ��/s�� |
�� | ���� | 1 | 20 | 50 | 30 | t1 |
�� | ���� | A | B | C | 30 | t2 |
�� | ���� | 2 | 40 | D | E | t3 |
��2���÷�Ӧ�����ӷ���ʽ ��
��3����t1��t2 �� �����ʵ��ٺ͢ڵõ��Ľ����� ��
��4��С��ͬѧ����ÿ��ʵ�鷴Ӧ������ʱ��ı仯������ͼ������t1��t2ʱ�������ʱ�����Ҫԭ������ǣ�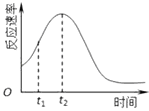
������ ��
��5����ѧС���õζ����ⶨKMnO4��Һ���ʵ���Ũ�ȣ�ȡag���ᾧ�壨H2C2O42H2O��Ħ������126g/mol������ˮ���250mL��Һ��ȡ25.00mL��Һ������ƿ�У���������ϡH2SO4�ữ������KMnO4��Һ�ζ����յ㣬�ظ��ζ����Σ�ƽ������KMnO4��ҺVmL���ζ������յ�������ǣ���ʵ��������Ķ��������������������ƣ�����KMnO4��Һ�����ʵ���Ũ��Ϊmol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������գ�
��1���������и��仯���������������ؼ���
��NH4NO3��ը��2NH4NO3��s���T2N2��g��+4H2O��g��+O2��g��
��ˮú��ת����CO��g��+H2O��g���TCO2��g��+H2��g��
�۳��������ɣ�3O2��g���T2O3��g��
��2�����淴ӦA��g��+B��g��2C��g���ڲ�ͬ�¶��¾���һ��ʱ�䣬�������C������������¶ȵĹ�ϵ��ͼ��ʾ��
����T1��T2�仯ʱ������Ӧ�����淴Ӧ���ʣ����������������=������
����T3��T4�仯ʱ������Ӧ�����淴Ӧ���ʣ����������������=������
�۷�Ӧ���¶��´ﵽƽ��
�ܴ˷�Ӧ������ӦΪ�ȷ�Ӧ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com