
NA代表阿伏加德罗常数,下列说法错误的是
A.标准状况下,22.4 L NO和22.4 L O2的混合, 混合气体中含有的氧原子数为3NA
B.0.012 kg 13C中,含中子数为7NA
C.25 ℃时,1 L pH=13的氢氧化钡溶液中含有0.1NA个氢氧根离子
D.在反应3SiO2+6C+2N2  Si3N4+6CO ,生成1 mol Si3N4时共转移12 NA电子
Si3N4+6CO ,生成1 mol Si3N4时共转移12 NA电子
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源:2014高考名师推荐化学--预测6 题型:选择题
下列有关化学用语表示正确的是
A 二氧化硅的分子式:SiO2
B质子数为53,中子数为78的碘原子:
C甲基的电子式:
D邻羟基苯甲酸的结构简式:
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测4 题型:填空题
合成口服抗菌药琥乙红霉素片的原料G、某种广泛应用于电子领域的高分子化合物I的合成路线如下:
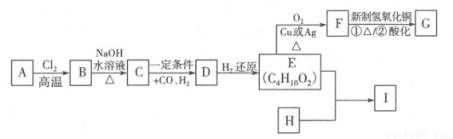
已知:① R—CH2—CH=CH2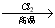 R—CHCl—CH=CH2
R—CHCl—CH=CH2
②R—CH2—CH=CH2 R—CH2CH2CH2CHO
R—CH2CH2CH2CHO
(1)C的结构简式是 ,E中的官能团的名称是 。
(2)写出A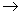 B的反应方程式 ,该反应类型是 。
B的反应方程式 ,该反应类型是 。
(3)H的分子式为C8H6O4,能与碳酸钠溶液反应放出气体,其一氯取代物只有一种,试写出E+H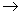 I的反应方程式 。
I的反应方程式 。
(4)关于G的说法中错误的是 (填序号)。
a.1 mol G最多可与2 mol NaHCO3反应
b.G可发生消去反应
c.1 mol G最多可与2 mol H2发生加成反应
d.1 mol G在一定条件下可与2 mol乙醇发生取代反应
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:简答题
下图为某套实验装置示意图,其中加热装置和部分药品等均已经省略(装置①和装置②为气体发生装置)。

(1)甲同学用此装置(在A、B间增加一盛有浓硫酸的洗气瓶)制备NO2并验
证其性质。装置①用于实验室制备NH3,用装置②制备过量O2。装置①中发生
反应的化学方程式是 。B处冰水冷却的U型管中有红棕色气
体生成且越接近U型管底部颜色越浅,请解释原因 。
(2)乙同学用此套装置合成SO3,B处冰水冷却的U型管中有固体出现。C中
若盛放酸性K2Cr2O7溶液,则在C中发生的氧化还原反应的离子方程式是 (生成物中Cr以Cr3+形式存在);现欲制得纯净干燥的SO3,若C中盛放NaOH溶液,则此装置中存在明显不足,应如何改进 (从下面给出的实验装置中选择字母标号补充或替换,并用简要文字说明补充和替换的位置)。

(3)丙同学拟验证NO能被氨气还原并测算其转化率(装置①、装置②分别制
NO和NH3),将上述装置A、B、C分别换成下列⑤、⑥、⑦。

请回答:装置⑦的作用可能是 ;若进入装置⑤的NO共22.4L(已折算为标准状况,下同),氨气过量,最后收集到标准状况下11.2LN2,则NO的转化率是 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:选择题
下列各组离子一定能大量共存的是
A.加入铝粉有氢气产生的溶液中Na+ 、K+ 、SO42-、Cl- 、HCO3-
B.含有大量硝酸根离子的溶液中H+ 、Fe2+ 、SO42-、Cl-
、SO42-、Cl-
C.常温下,c(H+)/c(OH-) = 1×10-10 的溶液中NH4+ 、K+ 、Ca2+ 、Cl-
D. 常温下pH=1的溶液中:MnO4-、NO3-、SO42-、Na+、Fe3+
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:选择题
维生素A1、B2的结构简式分别如图所示:
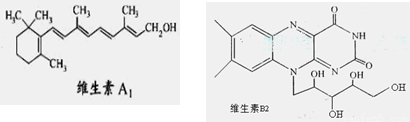
已知:
下列说法正确的是
A.1mol维生素A1最多与溴水中的4molBr2发生加成反应
B.维生素A1的分子式为C19H30O,是一种易溶于水的高分子。
C.维生素B2在酸性条件下彻底水解后得到的有机物,其分子内发生酯化得多种酯
D.用-C4H9取代维生素B2苯环上的一个H原子,最多可得4种同分异构体
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测2 题型:选择题
下列反应的离子方程式正确的是
A.Na2CO3溶液与NaHSO4溶液反应:CO32--+2H+=CO2↑+H2O
B.向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓
C.碘化钾溶液中滴入稀硫酸酸化的双氧水反应:2I-+H2O2+2H+=H2O+I2
D.海水制取溴时用纯碱吸收吹出的溴:3Br2+3H2O=5Br-+BrO3-+6H+
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测17 题型:选择题
关于下列各图的叙述中不正确的是

A.已知CO的燃烧热为283 kJ/mol,2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ/mol,则图甲表示CO和H2O(g)生成CO2和H2的能量变化
B.某温度下,pH=11的NH3·H2O和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+ 、NH3·H2O与NH3三种微粒的平衡浓度之和为0.05 mol·L-1
C.在常温下,X2(g)和H2反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐降低,且X2与H2反应的剧烈程度逐渐减弱
D.图乙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中, 的变化情况
的变化情况
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测15 题型:选择题
常温下,关于1L pH=3的H2SO4溶液说法正确的是
A、与等体积pH=11氨水混合后所得溶液pH小于7
B、与等浓度的CH3COONa溶液混合后所得溶液pH一定小于7
C、与pH=3的CH3COOH溶液混合后所得溶液pH小于3
D、与10L Ba(OH)2溶液恰好完全反应,则Ba(OH)2溶液的pH一定等于10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com