
100 g炭粉燃烧所得气体中,CO占2/3、CO2占1/3,且C(s)+1/2O2(g)===CO(g) ΔH=-110.35 kJ/mol,CO(g)+1/2O2(g)===CO2(g) ΔH=-282.57 kJ/mol,与这些炭粉完全燃烧相比损失的热量是( )
A.784.92 kJ B.2 489.44 kJ
C.1 569.83 kJ D.3 274.3 kJ
科目:高中化学 来源: 题型:
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):
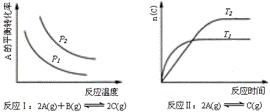

根据以上规律判断,上列结论正确的是( )
A.反应Ⅰ:△H>0,P2>P1 B.反应Ⅱ:△H>0,T1>T2
C.反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1 D.反应Ⅳ:△H<0,T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
高锰酸钾(KMnO4)和过氧化氢(H2O2)是两种典型的氧化剂。
(1)H2O2的结构式为________________。
(2)下列物质中能使酸性KMnO4溶液褪色的是________(填选项字母)。
A.臭碱(Na2S) B.小苏打(NaHCO3)
C.水玻璃(Na2SiO3) D.酒精(C2H5OH)
(3)高锰酸钾、双氧水、活性炭常用于饮用水的处理,但三者联合作用时必须有先后顺序。
①在稀硫酸中,KMnO4和H2O2能发生氧化还原反应:
氧化反应:H2O2-2e-―→2H++O2↑
还原反应:MnO +5e-+8H+―→Mn2++4H2O
+5e-+8H+―→Mn2++4H2O
写出该氧化还原反应的离子方程式_____________________________
____________________________________________________________。
②在处理饮用水时,活性炭应在高锰酸钾反应结束后投加,否则会发生反应:KMnO4+C+H2O―→MnO2+X+K2CO3(未配平),其中X的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铜是重要的工业原材料,现有Cu、Cu2O组成的混合物,某研究性学习小组为了探究其组成情况,取35.2 g混合物加入0.5 L 3.4 mol/L的稀硝酸,固体物质完全反应,生成4.48 L(标准状况)的NO。向所得溶液中加入a L 2.0 mol/L的NaOH溶液,恰好使溶液中的Cu2+沉淀完全。
(1)Cu2O与稀硝酸反应的化学方程式为________________。
(2)混合物中,n(Cu)=________;n(Cu2O)=________。
(3)所加NaOH溶液的体积a L=________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关能量的判断或表示方法正确的是( )
A.由C(s,石墨)===C(s,金刚石)
ΔH=+1.9 kJ·mol-1,可知:石墨比金刚石更稳定
B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多
C.由H+(aq)+OH-(aq)===H2O(l)
ΔH=-57.3 kJ·mol-1,可知:含1 mol CH3COOH的溶液与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ
D.2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的 热化学方程式为2H2(g)+O2(g)===2H2O(l) ΔH=-285.8 kJ·mol-1
热化学方程式为2H2(g)+O2(g)===2H2O(l) ΔH=-285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池反应原理为:Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l),下列说法正确的是( )
2PbSO4(s)+2H2O(l),下列说法正确的是( )
A.放电时,负极的电极反应式为:Pb-2e-===Pb2+
B.放电时 ,正极得电子的物质是PbO2
,正极得电子的物质是PbO2
C.充电时,电解质溶液中硫酸浓度减小
D.充电时,阴极的电极反应式为PbSO4-2e-+2H2O===PbO2+4H++SO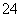
查看答案和解析>>
科目:高中化学 来源: 题型:
请仔细观察下列五种装置的构造示意图,完成下列问题:
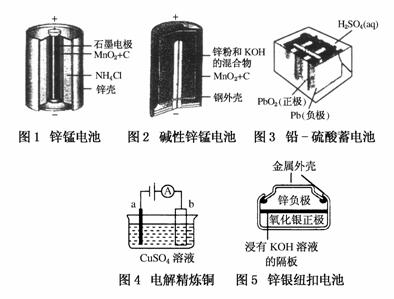
(1)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2,则负极的电极反 应式______________________。
应式______________________。
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是______________________________。
(3)铅-硫酸蓄电池放电过程中,H2SO4浓度______(填“变大”“变小”或“不变”),充电时阴极的电极反应式为____________________________。
(4)电解精炼铜时,a极是________(填“纯铜”或“粗铜”)。锌银纽扣电池在工作过程中________(填物质名称)被还原。
查看答案和解析>>
科目:高中化学 来源: 题型:
LiNi0.25Co0.75O2是锂离子电池的一种高性能的二元正极活性材料,其制备原理可表示为4Ni0.25Co0.75(OH)2+4LiOH+O2===4LiNi0.25Co0.75O2+6H2O(已知Ni与Co的化合价均有+2和+3)。下列说法不正确的是( )
A.Ni0.25Co0.75(OH)2中Ni的化合价是+2
B.LiNi0.25Co0.75O2中Co的化合价是+3
C.该反应中LiOH是还原剂
D.该反应中O2是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质应用和组成的说法正确的是( )
A.P2O5可用于干燥Cl2和NH3
B.“可燃冰”主要成分是甲烷和水
C.CCl4可用于鉴别溴水和碘水
D.Si和SiO2都用于制造光导纤维
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com