
用如图所示装置处理含NO3—的酸性工业废水,某电极反应式为2NO3—+12H++10e-=N2+6H2O,则下列说法错误的是
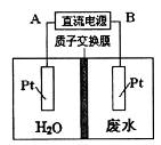
A.电源正极为A,电解过程中有气体放出
B.电解时H+从质子交换膜左侧向右侧移动
C.电解过程中,右侧电解液pH保持不变
D.电解池一侧生成5.6g N2,另一侧溶液质量减少l8g
C
【解析】
试题分析:A、根据示意图可知该装置为电解装置,右侧为含NO3—的酸性工业废水,发生的电极反应为:2NO3—+12H++10e-=N2+6H2O,为阴极,生成氮气,则B电极为电源的负极,A为电源正极,正确;B、电解时,电解质溶液中阳离子向阴极移动,所以电解时H+从质子交换膜左侧向右侧移动,正确;C、右侧发生的电极反应为:2NO3—+12H++10e-=N2+6H2O,消耗H+,pH增大,错误;D、右侧电极反应为:2NO3—+12H++10e-=N2+6H2O,n(N2)=5.6g÷28g/mol=0.2mol,则电子转移2mol,左侧发生电极反应为:4OH?—4e?=2H2O+O2↑,溶液减少的质量为O2的质量和移动到右侧的H+质量和,m(O2)=2mol×1/4×32g/mol=16g,m(H+)=2mol×1g/mol=2g,所以左侧溶液减少18g,正确。
考点:本题考查电解原理及应用。


科目:高中化学 来源:2015届山东省泰安市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式正确的是
A.用食醋除去暖水瓶中的水垢:2CH3COOH+CaCO3═Ca2++2CH3COO-+CO2↑+H2O
B.碳酸氢铵溶液中加入足量氢氧化钡溶液:NH4++HCO3—+2OH—═CO32-+NH3 H2O+H2O
H2O+H2O
C.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2
D.Ca(HCO3)2溶液中加入少量的NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+ CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第二次检测化学试试卷(解析版) 题型:选择题
还原2.4×10-3 mol [XO(OH)3]+ 到X元素的低价态时,消耗0.2mol·L—1的Na2SO3溶液30 mL,则X元素反应后的价态是
A.-1 B.+1 C.0 D.-2
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三第一次学情调查化学试卷(解析版) 题型:填空题
(12分)运用化学反应原理研究元素及其化合物的反应有重要意义。
工业合成氨过程中,N2和H2反应生成NH3:N2(g)+3H2(g) 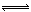 2NH3(g)。混合体系中NH3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2NH3(g)。混合体系中NH3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
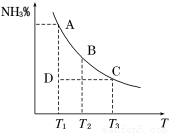
(1)N2(g)+3H2(g) 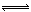 2NH3(g)的ΔH________0(填“>”或“<”)。
2NH3(g)的ΔH________0(填“>”或“<”)。
(2)若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡_______移动(填“向左”、“向右”或“不移动”) 。
(3)若温度为T1时,反应进行到状态D时,v正_____v逆(填“>”、“<”或“=”)。
(4)在体积为5 L的恒温、恒容密闭容器中,起始时投入2 mol N2、3 mol H2,经过10 s达到平衡,测得平衡时NH3的物质的量为0.8 mol。
①达平衡时N2的转化率=________。
②容器中反应的逆反应速率随时间变化的关系如图。
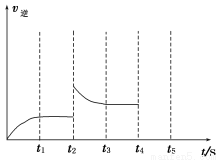
t2时改变了某一种条件,改变的条件可能是__________、____________________(填写两项)。
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三第一次学情调查化学试卷(解析版) 题型:选择题
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型,NiMH中的M表示储氢金属或合金,该电池在充电过程中的总反应方程式是Ni(OH)2+M===NiOOH+MH。已知:6NiOOH+NH3+H2O+OH-===6Ni(OH)2+NO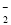 ,下列说法正确的是( )
,下列说法正确的是( )
A.NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-===Ni(OH)2+OH-
B.充电过程中OH-从阳极向阴极迁移
C.充电过程中阴极的电极反应式:H2O+M+e-===MH+OH-,H2O中的H被M还原
D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三第一次学情调查化学试卷(解析版) 题型:选择题
反应:L(s)+aG(g) bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。
bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。
据此可判断

A.上述反应是放热反应 B.上述反应是吸热反应
C.a>b D.无法判断a,b大小
查看答案和解析>>
科目:高中化学 来源:2015届山东省文登市高三上学期11月月考化学试卷(B卷)(解析版) 题型:选择题
硫酸、盐酸和硝酸与烧碱和纯碱并称为工业上的“三酸两碱”。下列说法正确的是
A.等质量的铝与足量的烧碱和盐酸反应生成氢气的质量相同
B.等质量的铜与足量的浓硫酸和浓硝酸反应生成气体的物质的量相同
C.相同物质的量的烧碱和纯碱与足量盐酸反应,消耗盐酸的体积相同
D.相同质量的硫与足量烧碱、浓硫酸、浓硝酸反应,转移电子数相同
查看答案和解析>>
科目:高中化学 来源:2015届山东省德州市高三期中考试化学试卷(解析版) 题型:实验题
(14分)MnO2是一种重要的催化剂。某研究性学习小组设计了将粗MnO2(含有较多MnO和MnCO3)样品转化为纯MnO2的实验,其流程如下:
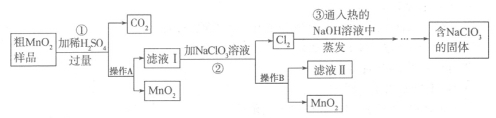
(1)检验操作A所得的MnO2是否洗涤干净的方法是 。
(2)第②步反应的离子反应方程式为 。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、 、 、玻璃棒。
(4)上述流程中可用于循环使用的物质是 (填化学式)。
(5)MnO2不仅可作催化剂还可作氧化剂,写出1个用二氧化锰作氧化剂的化学反应方程式 。
(6)若粗MnO2样品的质量为24.28g,第①步反应后,经过滤得到18.35g MnO2,并收集到0.672 LCO2(标准状况下),则样品中所含的MnO质量为 g。
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次模拟考试试卷(解析版) 题型:实验题
(14分)下图是实验室中制备气体或验证气体性质的装置图
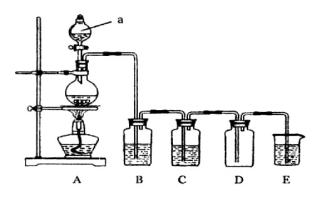
(1)写出用A制取氯气的化学方程式_________________________________________。
(2)利用上图装置制备纯净的氯气,并证明氧化性:Cl2>Fe3+
则装置B中的溶液的作用是___________________________________;
装置D中加的最佳试剂是(填序号)___________:
供选试剂:a.浓H2SO4 b.FeCl2溶液 c.KSCN与FeCl2的混合溶液 d.无水氯化钙
(3)在上图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置同时完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
证明SO2具氧化性和漂白性:B中为少量Na2S溶液、C中加品红溶液,D中应加入足量的__________(填溶液名称),E中加入___________溶液(填化学式)。
(4)证明碳元素的非金属性比硅元素的强的现象为______________________;
实验2不严谨之处应如何改进________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com