
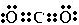 ,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.
,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.| 共价键 | H-H | H-F | H-Cl | H-Br | H-O | H-S | H-N | H-P |
| 键长(pm) | 74 | 92 | 127 | 141 | 98 | 135 | 101 | 321 |
| 键能(kJ/mol) | 436 | 568 | 432 | 368 | 464 | 364 | 391 | 142 |
分析 (1)根据蛋白质、脂肪、碳水化合物和核酸的组成元素判断;核外有几个电子就有几种运动状态不同的电子;第二周期单质熔点最高的元素为C;
(2)葡萄糖在人体内完全氧化成二氧化碳和液态水,结合热化学方程式的要求书写;
(3)二氧化碳电子式为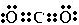 ,不同原子间是极性键;
,不同原子间是极性键;
(4)根据元素周期律的递变规律判断粒子半径、金属性、晶体的熔点以及氢化物的还原性强弱;
(5)同主族元素原子与相同其他原子形成的化合物中,键长越长,键能越小.
解答 解:(1)蛋白质由C、H、O、N元素组成,脂肪由C、H、O元素组成,碳水化合物由C、H、O元素组成,核酸由C、H、O、N、P等元素组成,N的原子序数为7,最外层电子为5,则有5种运动状态不同的电子;与它同周期,且单质熔点最高的元素为C,位于周期表第二周期IVA族,
故答案为:N;5;第二周期IVA族;
(2)葡萄糖在人体内完全氧化成二氧化碳和液态水,反应的热化学方程式:C6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l)△H=-2804 kJ•mol-1,
故答案为:C6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l)△H=-2804 kJ•mol-1;
(3)二氧化碳为含有极性键的非极性分子,电子式为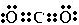 ,故答案为:
,故答案为: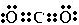 ;极性;
;极性;
(4)a.核外电子排布相同时,核电核数越大,半径越小,则有Na+<O2-,故a错误;
b.金属性:Ca>Mg,则Ca与水反应较Mg剧烈,故b错误;
C.SiO2为原子晶体,熔点最高,故c错误;
D.元素的非金属性:P<S<Cl<F,元素的非金属性越强,对应的单质的氧化性越强,其氢化物的还原性越弱,所以还原性:PH3>H2S>HCl>HF,故d正确,
故答案为:d;
(5)由表中数据可知,同主族元素原子与相同其他原子形成共价键时,原子半径越大,键长越长,键能越小,或同类分子中,键长越小,键能越大,
故答案为:同类分子中(同主族元素原子与相同其他原子等合理均可),键长越小,键能越大.
点评 本题考查较为综合,涉及多方面知识,题目难度中等,把握元素周期律的递变规律是解题的关键,注意基础知识的积累.


科目:高中化学 来源: 题型:选择题
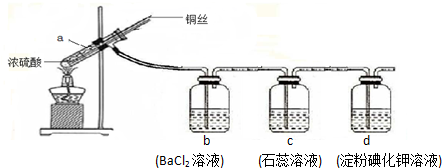
| A. | a装置中有白色固体 | B. | b装置中产生白色沉淀 | ||
| C. | c装置中溶液先变红后褪色 | D. | d装置中溶液变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
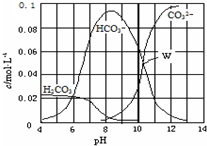
| A. | W点所示的溶液:c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) | |
| B. | pH=4的溶液:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1 mol•L-1 | |
| C. | 向pH=8的溶液中通入CO2至pH=7所得的溶液:c(Na+)>c(Cl-)+c(HCO3-)+c(H2CO3) | |
| D. | pH=11的溶液:c(Na+)+2c(H2CO3)>2c(Cl-)+2c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol/L的CH3COOH溶液与0.1 mol/L CH3COOH溶液中c(H+)之比为2:1 | |
| B. | 0.1 mol/L NaHCO3溶液中,c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | 0.1 mol/L 的NaHA溶液,其pH=4,则c(HA-)>c(A2-)>c(H2A) | |
| D. | 只含Na+、CH3COO-、H+、OH-的酸性溶液中,c(H+)>c(CH3COO-)>c(Na+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 弱碱的浓度大于强酸的浓度 | |
| B. | 原氨水中有1%的含氮微粒为NH4+ | |
| C. | 反应后的溶液呈酸性 | |
| D. | 混合溶液中c(NH4+)+c(NH3•H2O)+c(NH3)=5×10-4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16.5g | B. | 85g•mol-1 | C. | 65 g | D. | 55g•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com