
【题目】研究人员采用双极膜将酸-碱电解液隔离,实现MnO2/Mn2+和Zn/![]() 的两个溶解/沉积电极氧化还原反应,研制出新型高比能液流电池,其放电过程原理示意图如下:
的两个溶解/沉积电极氧化还原反应,研制出新型高比能液流电池,其放电过程原理示意图如下:
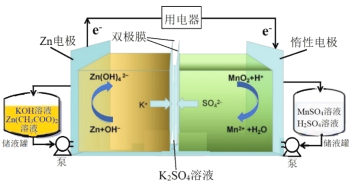
下列说法不正确的是
A.放电过程中,总反应方程式为Zn+MnO2+4OH-+4H+===![]() +Mn2++2H2O
+Mn2++2H2O
B.放电过程中,当1molZn参与反应时,理论上有4molK+发生迁移
C.充电过程中,阴极的电极反应为![]() +2e-===Zn+4OH-
+2e-===Zn+4OH-
D.充电过程中,右侧池中溶液pH逐渐减小
【答案】B
【解析】
根据电池示意图,左侧Zn失去电子与溶液中的OH-反应生成![]() ,为负极反应,右侧MnO2得电子与溶液中的H+反应生成Mn2+和水;电解过程中,右侧的Mn2+失去电子与水反应生成MnO2和H+,电极方程式与原电池的正极方程式相反,左侧
,为负极反应,右侧MnO2得电子与溶液中的H+反应生成Mn2+和水;电解过程中,右侧的Mn2+失去电子与水反应生成MnO2和H+,电极方程式与原电池的正极方程式相反,左侧![]() 得电子生成Zn和OH-,电极方程式与原电池的负极方程式相反,据此分析。
得电子生成Zn和OH-,电极方程式与原电池的负极方程式相反,据此分析。
A.放电过程中负极的电极反应式为Zn-2e-+4OH-=![]() ,正极的电极方程式为MnO2+2e-+4H+=Mn2++2H2O,总反应为Zn+MnO2+4OH-+4H+===
,正极的电极方程式为MnO2+2e-+4H+=Mn2++2H2O,总反应为Zn+MnO2+4OH-+4H+===![]() +Mn2++2H2O,A正确;
+Mn2++2H2O,A正确;
B.放电过程中每消耗1mol Zn会生成1mol ![]() ,即每消耗4mol负电荷生成2mol负电荷,电解质中减少2mol负电荷,因此有2mol K+发生迁移,B错误;
,即每消耗4mol负电荷生成2mol负电荷,电解质中减少2mol负电荷,因此有2mol K+发生迁移,B错误;
C.根据分析,充电过程中阴极的电极方程式与放电过程中负极的电极方程式相反,阴极的电极方程式为![]() +2e-===Zn+4OH-,C正确;
+2e-===Zn+4OH-,C正确;
D.充电过程中右侧Mn2+不断失去电子并结合水生成MnO2,同时生成大量H+,因此,右侧pH不断减小,D正确;
故选B。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】根据如图所示转化关系,判断A、B、C、D各是什么物质,写出有关的化学方程式:
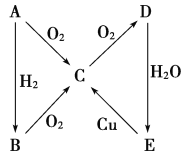
(1)当A为气体单质时,A是________,B是__________,C是________,D是________,E是________,E→C的化学方程式:_________________________________________________。
(2)当A为固体单质时,A是________,B是________,C是________,D是________,E是________,E→C的化学方程式是_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列十种物质:①H2O,②Cu,③NO,④Fe2O3,⑤稀硫酸,⑥氢氧化钡,⑦饱和FeCl3溶液,⑧氨水,⑨稀硝酸,⑩硫酸铝。根据上述提供的物质,回答下列问题:
(1)属于纯净物的是__________(填序号),属于电解质的是__________(填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH===H2O,则该反应的化学方程式为___________________________________________________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为________________________________________________________。
(4)实验室配制245 mL 0.5 mol/L的硫酸铝溶液,从配制好的溶液中取出100 mL,其中含有的![]() 的数目为_______(设NA为阿伏加德罗常数的值)。
的数目为_______(设NA为阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要制备纯净的氯化钾。现含有少量K2SO4的氯化钾样品,按照如图所示的实验方案进行提纯。

(1)检验加入BaCl2溶液后![]() 是否沉淀完全的操作为____________________________。
是否沉淀完全的操作为____________________________。
(2)若用硝酸钡来代替氯化钡,请判断是否可行,并说明理由:_____________________。
(3)某同学认为该实验方案中加适量氯化钡溶液不容易控制,应加入过量氯化钡溶液,他的思路如下:

请写出①②③④⑤溶质或沉淀的化学式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,有下列物质:①8gCH4、②6.02×1023个HCl分子、③2mol O2。按由小到大的顺序填写下列空白(填写序号):
(1)摩尔质量____________________。
(2)物质的量____________________。
(3)分子数目____________________。
(4)原子数目____________________。
(5)质量____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究金属钠的性质,实验如下:
实验装置 | 实验方案 | |
液体a | 现象 | |
| 蒸馏水 | I.钠浮在水面,剧烈反应,有少量白雾 |
0.1 mol·L-1盐酸 | II.钠浮在液面,反应比Ⅰ剧烈,有白雾产生 | |
浓盐酸 | III.钠浮在液面,反应比Ⅰ缓慢,产生大量白雾,烧杯底部有白色固体 | |
下列说法不正确的是
A.II中反应的离子方程式为2Na + 2H+ === 2Na+ + H2↑
B.对比I、II、III可知,随着c(H+) 增大,反应的剧烈程度增大
C.实验I、II、III均有白雾产生,说明Na与水或酸反应均放出大量热
D.推测III中浓盐酸的c(Cl-)以及生成的NaCl固体对反应剧烈程度有影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥运吉祥物福娃外材料为纯羊毛,内充物为无毒的聚酯纤维
![]() 。
。
下列说法中正确的是( )
A.羊毛与聚酯纤维的化学成分相同
B.聚酯纤维和羊毛在一定条件下均能水解
C.纯羊毛为纯净物
D.羊毛与聚酯纤维不能用燃烧法区别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下的一密闭容器中事先放入1.56g过氧化钠,然后再通入乙烷与氧气的混合气体,用电火花引爆,直至反应完全为止,恢复到原温度,容器内压强近似为零。
(1)相同条件下,通入的气体氧气和乙烷的体积比是多少?_____
(2)通入氧气的质量最大应是多少?_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 NaOH溶液滴定NH4HSO4溶液 ,混合溶液的相对导电能力变化曲线如图所示,已知: Kb(NH3 H2O) =10-5,下列叙述正确的是
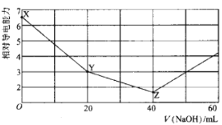
A.X→Y 过程中发生反应的离子方程式为:![]() +OH-= NH3 H2O
+OH-= NH3 H2O
B.Y点满足:c(![]() ) +c(Na+) =2c(
) +c(Na+) =2c(![]() )
)
C.水的电离程度:X>Y>Z
D.若Z点溶液pH=1l,则此时溶液中氨水浓度约为0.1 molL-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com