
| A. | 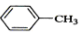 +Cl2$\stackrel{光照}{→}$ +Cl2$\stackrel{光照}{→}$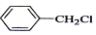 +HCl +HCl | |
| B. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O | |
| C. | ClCH2CH=CH2+NaOH→HOCH2CH=CH2+NaCl | |
| D. | 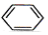 +HONO2$\stackrel{浓硫酸}{→}$ +HONO2$\stackrel{浓硫酸}{→}$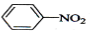 +H2O +H2O |
分析 A.甲基上H被Cl取代;
B.-OH转化为-CHO;
C.-Cl转化为-OH;
D.苯环上H被硝基取代.
解答 解:A. +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl为取代反应,故A不选;
+HCl为取代反应,故A不选;
B.2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O为氧化反应,故B选;
C.ClCH2CH=CH2+NaOH→HOCH2CH=CH2+NaCl为水解反应,属于取代反应,故C不选;
D. +HONO2$\stackrel{浓硫酸}{→}$
+HONO2$\stackrel{浓硫酸}{→}$ +H2O为取代反应,故D不选;
+H2O为取代反应,故D不选;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机反应类型的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 60 mL 0.03 mol•L-1HCl溶液 | B. | 60 mL 0.04 mol•L-1KCl溶液 | ||
| C. | 20 mL 0.03 mol•L-1CaCl2溶液 | D. | 50 mL 0.05 mol•L-1AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液(FeCl2):通入适量Cl2 | |
| B. | Fe2O3固体(Al2O3):加入烧碱溶液,过滤 | |
| C. | Cl2气体(HCl):通过NaOH溶液洗气后干燥 | |
| D. | Na2CO3固体(NaHCO3):加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molH2O所含质子数为8NA | |
| B. | 1摩尔氦气所含的原子数为2NA | |
| C. | 在标准状况下1L水所含分子数为$\frac{1}{22.4}$NA | |
| D. | 0.5molaL与足量盐酸反应转移的电子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
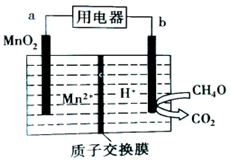
| A. | a极为正极,发生还原反应 | |
| B. | b极的电极反应为CH4O-6e-+H2O=CO2+6H+ | |
| C. | 电子从b极流出经用电器流向a极 | |
| D. | 放电时H+由质子交换膜左侧移向右侧 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
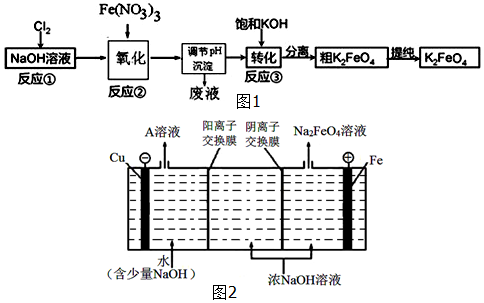
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
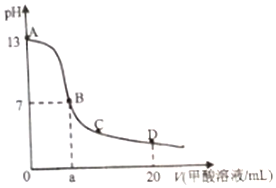 在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )
在15mL0.lmol•L-1KOH溶液中逐滴加入0.2mol•L-1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( )| A. | 在B点:c(K+)=c(HCOO-)>c(OH-)=c(H+),且a=7.5 | |
| B. | 在A、B间任意一点,c(HCOO-)>c(K+)>c(OH-)>c(H+) | |
| C. | 在D点:c(HCOO-)+c(HCOOH)>2c(K+) | |
| D. | B→C段:水的电离程度先增大后减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com