
【题目】叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和N3-。试回答下列问题:
(1)下列有关说法正确的是___(填序号)。
A.HN3中含有5个σ键
B.HN3中的三个氮原子均采用sp2杂化
C.HN3、HNO2、H2O、N2H4都是极性分子
D.N2H4沸点高达113.5℃,说明肼分子间可形成氢键
(2)叠氮酸根能与许多金属离子等形成配合物,如[Co(N3)(NH3)5]SO4,在该配合物中钴显___价;根据价层电子对互斥理论判断SO42-的空间构型为___。
(3)与N3-互为等电子体的分子有___(写两种即可)。
【答案】CD +3 正四面体形 CO2、CS2
【解析】
(1)A.根据HN3的分子结构可知,HN3分子中存在3个σ键,故A错误;
B.HN3分子中连接三键的氮原子为sp杂化,故B错误;
C.HN3、HNO2、H2O、N2H4分子的正、负电荷中心不重合,都是极性分子,故C正确;
D.N2H4为分子化合物,N元素电负性较高,能够形成分子间氢键,分子间氢键的存在会使物质的熔、沸点升高,故D正确;
故答案为:CD;
(2)[Co(N3)(NH3)5]SO4中![]() 带1个单位负电荷,NH3不带电荷,
带1个单位负电荷,NH3不带电荷,![]() 带2个单位负电荷,根据化合物中元素化合价的代数和等于零可知,[Co(N3)(NH3)5]SO4中钴显+3价;硫酸根离子中S原子的价层电子对数为
带2个单位负电荷,根据化合物中元素化合价的代数和等于零可知,[Co(N3)(NH3)5]SO4中钴显+3价;硫酸根离子中S原子的价层电子对数为![]() ,无孤电子对,故其空间构型为正四面体形;
,无孤电子对,故其空间构型为正四面体形;
(3)互为等电子体的粒子必须满足两个条件:①所含原子总数相等;②所含价电子总数相等,![]() 价电子总数为3×5+1=16,因此与
价电子总数为3×5+1=16,因此与![]() 互为等电子体的分子有CO2、CS2。
互为等电子体的分子有CO2、CS2。


科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10个电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(1)E元素原子基态电子排布式____________。
(2)F元素原子的价电子排布图________________。
(3)F、G元素对应的最高价含氧酸中酸性较强的分子式为__________________。
(4)离子半径D+______B3-,第一电离能B______C,电负性C______F(填“<”、“>”或“=”)。
(5)A、C形成的两种常见分子中,其中一种为绿色氧化剂的电子式为_________。
(6)基态G原子中,电子占据的最高能层符号是_______,该能层有________个能级,电子数是_____。该原子有_____种运动状态不同的电子,最高能级符号是_____,未成对电子数为________。
(7)与E同族有4个能层的元素符号为______,它的简化电子排布式为______,与该元素同周期且核电荷数小7的元素在周期表中的位置______________,该元素的价电子排布式为__________,_________满足构造原理(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:NH4+、Cl-、Mg2+、Ba2+、K+、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.04mol
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。
根据上述实验,以下推测正确的是
A.K+可能存在B.该溶液中含CO32-离子的浓度为0.2mol/L
C.Cl-一定不存在D.Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,10L密闭容器中加入5molSO2、4.5moLO2,经10min后反应达平衡时,有3molSO2发生了反应。试回答下列问题:
(1)O2的转化率为__。
(2)用SO2表示该反应的反应速率为__。
(3)平衡时容器内气体压强与反应前的压强之比为__。(最简整数比)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用CH4燃料电池(如图)作为电源,用Cu-Si合金作硅源电解制硅可以降低制硅成本,高温利用三层液熔盐进行电解精炼,下列说法不正确的是( )
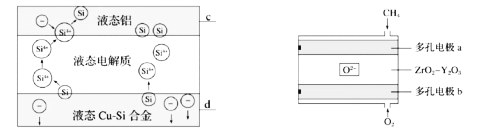
A.电极d与b相连,c与a相连
B.电解槽中,Si优先于Cu被氧化
C.a极的电极反应为CH4-8e-+8OH-=CO2+6H2O
D.相同时间下,通入CH4、O2的体积不同,会影响硅的提纯速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.羟基磷酸钙[Ca10(PO4)6(OH)2]具有优良的生物相容性和生物活性,它在口腔保健中具有重要作用,可以防止龋齿等,回答下列问题。
(1)Ca10(PO4)6(OH)2中,元素的电负性按由大到小的顺序依次是___。
(2)上述元素都能形成氢化物,其中PH3与同主族元素N形成的氢化物的键角关系是PH3___NH3(填“>”或“<”),PO43-离子空间构型是___。
(3)现已合成含钙的全氮阴离子盐,其中阴离子N5-为平面正五边形结构,N原子的杂化类型是___。
(4)碳酸钙的分解温度远高于碳酸镁,其原因是___。
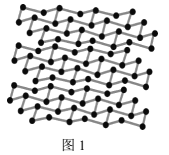
(5)黑磷是磷的一种同素异形体,与石墨烯类似,其晶体结构片段如图1所示:其中最小的环为6元环,每个环平均含有___个P原子。
Ⅱ.钴是人体不可或缺的微量元素之一。Co、Al、O形成的一种化合物钴蓝晶体结构如图2所示。
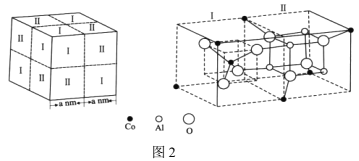
(6)基态Co原子的价电子排布式为___。该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为___,NA为阿伏加德罗常数的值,钴蓝晶体的密度为___ g·cm-3(列计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂是重要的营养物质.某天然油脂A可发生下列反应:
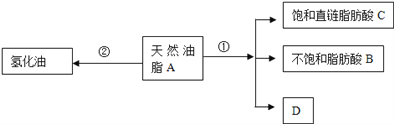
已知:A的分子式为C57H106O6.1mol该天然油脂A经反应①可得到1molD、1mol不饱和脂肪酸B和2mol直链饱和脂肪酸C.经测定B的相对分子质量为280,原子个数比为C:H:O=9:16:1;
(1)写出B的分子式:________________________;
(2)写出反应①的反应类型:____________;C的名称(或俗称)是_________;
(3)近日,电视媒体关于“氢化油危害堪比杀虫剂”的报道引发轩然大波,反应②为天然油脂的氢化过程.下列有关说法不正确的是_______________;
a.氢化油又称人造奶油,通常又叫硬化油.
b.植物油经过氢化处理后会产生副产品反式脂肪酸甘油酯,摄入过多的氢化油,容易堵塞血管而导致心脑血管疾病.
c.氢化油的制备原理是在加热植物油时,加入金属催化剂,通入氢气,使液态油脂变为半固态或固态油脂.
d.油脂的氢化与油脂的皂化都属于加成反应
(4)D和足量金属钠反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
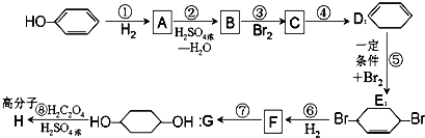
【题目】按以下步骤可从![]() 合成
合成![]() (部分试剂和反应条件已略去)。
(部分试剂和反应条件已略去)。
请回答下列问题:
(1)B,F的结构简式为:B___,F_______;
(2)反应①~⑦中属于消去反应的是(填代号)_______;
(3)根据反应![]() +Br2
+Br2![]()
![]() ,写出在同样条件下CH2=CHCH=CH2与等物质的量Br2发生加成反应的化学方程式:__;
,写出在同样条件下CH2=CHCH=CH2与等物质的量Br2发生加成反应的化学方程式:__;
(4)写出第④步C→![]() 的化学方程式(有机物写结构简式,注明反应条件)__;
的化学方程式(有机物写结构简式,注明反应条件)__;
(5)与4个不同的原子或原子团相连的碳原子称为手性碳原子;A﹣G这七种有机物分子中含有手性碳原子的是(填序号)__;
(6)核磁共振谱是测定有机物分子结构最有用的工具之一,在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目,例如:乙醛的结构式为:![]() ,其PMR谱中有2个信号峰,其强度之比为3:1,则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是__。
,其PMR谱中有2个信号峰,其强度之比为3:1,则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是__。
A ![]() B
B ![]() C
C ![]() D
D ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室经常利用KMnO4来检验产物或验证性质,图示为部分装置图,下列说法不正确的是
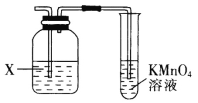
A.若X为NaOH溶液时,则KMnO4可用于溴乙烷发生消去反应的产物检验
B.若X为NaOH溶液时,则KMnO4可用于乙醇发生消去反应的产物检验
C.若X为CuSO4溶液时,则KMnO4可用于实验室制取乙炔时验证其性质
D.若X为溴水,则KMnO4可用于乙醛发生还原反应的产物检验
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com