
| A. | S O2 | B. | NaCl溶液 | C. | 熔融的 NaCl | D. | 铜丝 |
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:解答题
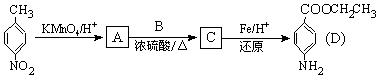
 、BCH3CH2OH、C
、BCH3CH2OH、C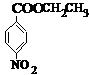 .
.
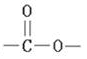
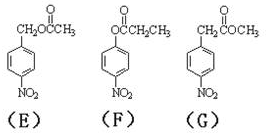
 .
.

 的流程图(无机试剂任选).合成路线流程图示如图:
的流程图(无机试剂任选).合成路线流程图示如图:
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH溶液与NaOH溶液反应:H++OH-═H2O | |
| B. | 碳酸氢钠溶液中加盐酸 CO32-+2H+═CO2和H2O | |
| C. | 氢氧化钠溶液中加硫酸镁 2OH-+Mg2+═Mg(OH)2 | |
| D. | 氢氧化钡溶液中加硫酸 OH-+H+═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③①②⑤ | B. | ④⑤③②① | C. | ④③②①⑤ | D. | ④②③①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A组 | B组 | C组 | D组 | |
| 分类标准 | 非金属单质 | 金属单质 | 金属氧化物 | 酸 |
| 不属于该类的物质 | Al | N2 | SO2 | NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜放入稀硫酸中:Cu+2H+═Cu2++H2↑ | |
| B. | 大理石溶于醋酸中:CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ | |
| C. | 金属铁溶于稀硫酸中:2Fe+6 H+═2 Fe3++3 H2↑ | |
| D. | 向硫酸溶液中加入氢氧化钡溶液:SO42++Ba2+═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| X | Y | ||
| Z | W | Q |
| A. | 阴离子的还原性:W2-<Q-<Y- | |
| B. | 常温下,X2与W的单质间化合反应不能自发进行 | |
| C. | ZX2是两性氧化物 | |
| D. | Y的氢化物可用来篆刻玻璃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com