
分析 (1)单质只有一种元素组成;氧化物含两种元素、其一为氧元素;由金属离子与酸根离子形成的化合物为盐(铵盐除外);在水溶液中或熔化状态下导电的化合物为电解质,而在水溶液和熔化状态下都不导电的化合物为非电解质;
(2)物质的量n=$\frac{V}{Vm}$;分子个数N=nNA;
(3)检验NaCl样品中是否含KCl,应鉴定钾元素的存在.
解答 解:(1)①二氧化碳(CO2)②碳酸钠(Na2CO3)③食盐水 ④钠(Na)中,单质是④;氧化物是①;盐类是②;属于电解质的是②;属于非电解质的是①,
故答案为:④;①;②;②;①;
(2)二氧化碳的物质的量n=$\frac{V}{Vm}$=$\frac{11.2L}{22.4L/mol}$=0.5mol;分子个数N=nNA=0.5mol×NA/mol=0.5NA个,故答案为:;
(3)检验NaCl样品中是否含KCl,应鉴定钾元素的存在,故应用焰色反应,故答案为:焰色反应.
点评 本题考查物质分类、物质的量的计算及物质检验,为高频考点,把握物质的组成、物质的量的基本计算公式、物质的性质为解答的关键,侧重分析与应用能力的考查,注意食盐水为混合物,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸化的淀粉溶液 | B. | 硫酸钠溶液 | C. | H2O2溶液 | D. | 氯水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
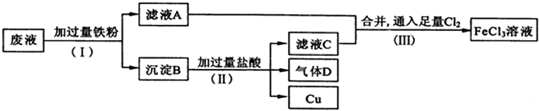
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1 mol•L-1的氨水中含有NH3•H2O分子数为0.1NA | |
| B. | 电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA | |
| C. | 标准状况下,2.24 L的二氯甲烷中含有的碳氯共价键的数目为0.2NA | |
| D. | 一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
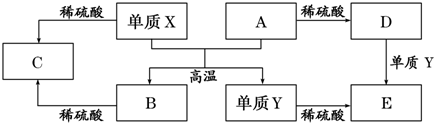
| A. | 单质Y在一定条件下能与水发生置换反应 | |
| B. | 向D溶液中滴加KSCN溶液,产生血红色沉淀 | |
| C. | X与A反应的化学方程式是 Al2O3+2Fe$\frac{\underline{\;高温\;}}{\;}$Fe2O3+2Al | |
| D. | 由于氧化物A和B均能与酸反应所以均是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某些金属、非金属元素化合时也能形成共价键 | |
| B. | 只有阴、阳离子间才能形成离子键 | |
| C. | 升温能加快钠与氧气反应生成氧化钠反应的速率 | |
| D. | FeCl2不能通过两种单质化合反应制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (10-8+10-10)mol/L | B. | (10-4+10-6)mol/L | C. | (10-8+10-9)mol/L | D. | 2×10-10mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com