
在容积为2 L的密闭容器中充入3mol气体A和2.5mol气体B,发生反应:3A(g)+B(g)xC(g)+2D(g)(正反应为吸热反应),5min时测得生成1mol D,C的平均反应速率v(C)=0.1mol·L-1·min-1,试求:
(1)方程式中C的化学计量数x=__________。
(2)5min内A的平均反应速率v(A)=__________。
(3)5min时B的转化率为__________。
(4)温度升高A的转化率________(填“增大”或“减小”或“不变”下同),压强增大B的转化率________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
已知氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白作用。为了探究SO2的漂白作用到底是SO2本身还是SO2与水作用的产物,某学习小组设计了如图装置来进行实验。请回答相关问题。
(1)制备SO2气体的反应方程式为: ;
发生装置的玻璃仪器名为 、 ;
(2)为了探究干燥的SO2能不能使品红褪色,某同学设计了如图所示实验装置,请指出实验装置图设计中的不合理之处。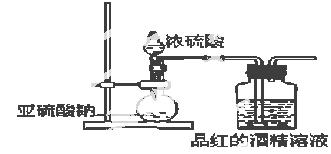
① ;② ;
(3)按照修改后的装置,实验中控制SO2以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色.这说明品红褪色的原因不是SO2直接导致。为此,SO2能使品红的水溶液褪色的可能微粒有(不考虑水及水电离出来的粒子) 。
(4)甲同学实验如下:取等量、相同浓度的品红水溶液于两支试管中,再分别加入少量Na2SO3固体和NaHSO3固体,两支试管中的品红都褪色,对此他得出结论:使品红褪色的微粒是HSO3-和SO32-,不是H2SO3。你认为他的结论是否正确 ,其理由是 。
(5)为了进一步探究,乙组同学做了如下实验:分别取相同浓度的品红水溶液各20ml于两只小烧杯中,再分别一次性加入20ml 0.1mol/L的Na2SO3溶液、20ml 0.1mol/L的NaHSO3溶液,发现加入Na2SO3溶液的品红褪色较快。
①微粒浓度与褪色快慢关系,请用“多”或“少”填写“ ”内容:
| 同浓度溶液 | SO32- | HSO3- | H2SO3 | 褪色速度 |
| Na2SO3溶液 | 多 | 少 | 少 | 快 |
| NaHSO3溶液 | 较上面_________ | 较上面_______ | 较上面_______ | 慢 |
②根据实验和分析,得出的结论是
查看答案和解析>>
科目:高中化学 来源: 题型:
某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3 个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
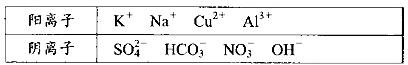
为了鉴别上述化台物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、c为紫色(透过蓝色钻玻璃);
④在各溶液中加入硝酸锁溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产
生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B________,D________。
(2)将含I mol A的溶液与含l molE的溶液反应后蒸于,仅得到一种化台物,该化合物的化学式为_____________.
(3)在A溶液中加入少量澄清石灰水,其离子方程式为________________。
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理_____________。
(5)若向含溶质lmol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为______________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列反应中:A2(g)+B2(g)2AB(g) ΔH<0当其达到平衡时,在下图所示的曲线中,符合勒夏特列原理的是( )
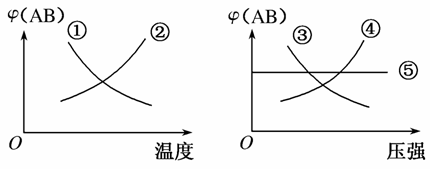
A.①② B.③④
C.① D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条下,在体积为2 L的密闭容器中,3mol X和3mol Y发生反应:
3X(g)+Y(g)2Z(g),经60 s达到平衡,生成0.4mol Z。下列说法正确的是( )
A.60 s内反应速率为v(X)=0.05mol/(L·s),X的转化率为80%
B.其他条件不变,将容器体积变为4 L,Z的平衡浓度变为原来的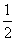
C.其他条件不变,若升高温度,X的体积分数增大,则该反应的ΔH>0
D.其他条件不变,若初始投入2mol X和2mol Y则物质Y的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2CH2===CH2+O2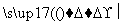 2CH3CHO。在下列反应中,其中有机反应物发生的反应类型与乙烯相同的是( )
2CH3CHO。在下列反应中,其中有机反应物发生的反应类型与乙烯相同的是( )
①乙醛转化为乙醇 ②苯酚置于空气中变红 ③乙醛的银镜反应 ④CH3CH2Br在NaOH醇溶液中加热 ⑤丙酮(CH3COCH3)与氢气生成2丙醇 ⑥甲苯使酸性高锰酸钾溶液褪色 ⑦乙酸乙酯碱性条件下水解
A.①⑤ B.①②⑥
C.②③⑥ D.除④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用锌粒与2mol/L硫酸溶液制取氢气,下列措施能增大化学反应速率的是()
A. 用锌粉代替锌粒
B. 改用更多的2mol/L硫酸溶液
C. 改用18mol/L硫酸溶液
D. 向该硫酸溶液中加入等体积的水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com