
【题目】化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用.
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7 , 其中1/3的Cu以罕见的Cu3+形式存在.Cu3+基态的核外电子排布式为
(2)磁性材料在生活和科学技术中应用广泛.研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性.下列物质适合做录音带磁粉原料的是(填选项字母).
A.V2O5
B.CrO2
C.PbO
D.ZnO
(3)屠呦呦因在抗疟药﹣﹣青蒿素(C15H22O5)研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人.青蒿素的结构简式如图l所示,碳原子的杂化方式为 . 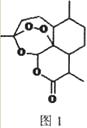
(4)“可燃冰因储量大”,污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示 
①“可燃冰”中分子间存在的2种作用力为
②H2O的键角大于CH4原因为
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有个碳原子.已知石墨的层间距为a pm,C﹣C键长为b pm,阿伏伽德罗常数的值为NA , 则石墨晶体的密度为g.cm﹣3(列出计算式). 
【答案】
(1)1s22s22p63s23p63d8
(2)B
(3)sp2、sp3
(4)氢键、范德华力;甲烷分子的杂化轨道中无孤电子对,而H2O分子有两对孤对电子,孤对电子与成键电子的排斥力大、键角小
(5)4;![]()
【解析】解:(1)Cu原子核外电子数为29,原子核外电子排布式为1s22s22p63s23p63d104s1 , 失去4s能级1个电子、3d能级2个电子形成Cu3+ , 基态Cu3+的核外电子排布式为1s22s22p63s23p63d8;所以答案是:1s22s22p63s23p63d8;
(2.)A.V2O5 中V5+的核外电子排布式为1s22s22p63s23p6 , 没有未成对电子,没有磁性;B.CrO2 中Cr4+的核外电子排布式为1s22s22p63s23p63d2 , 有未成对电子,具有磁性;C.PbO 中Pb处于IVA族,失去p能级2电子形成Pb2+ , 没有未成对电子,没有磁性;D.ZnO中Zn2+的核外电子排布式为1s22s22p63s23p63d10 , 没有未成对电子,具有磁性,CrO2适合作录音磁带磁粉原料,所以答案是:B;
(3.)青蒿素分子中酯基中C原子为形成3个σ键、其它碳原子形成4个σ键,均没有孤对电子,碳原子的杂化方式为 sp2、sp3 , 所以答案是:sp2、sp3;
(4.)①水分子之间形成氢键,分子之间还存在范德华力,所以答案是:氢键、范德华力;②H2O分子中O原子形成2个σ键、含有2对孤电子对,VSEPR模型为四面体形;甲烷分子的杂化轨道中无孤电子对,而H2O分子有两对孤对电子,孤对电子与成键电子的排斥力大、键角小,则键角H2O<CH4 ,
所以答案是:四面体形;<;甲烷分子的杂化轨道中无孤电子对,而H2O分子有两对孤对电子,孤对电子与成键电子的排斥力大、键角小;
(5.)根据均摊法,晶胞中C原子数目=1+8× ![]() +4×
+4× ![]() +2×
+2× ![]() =4,晶胞质量为
=4,晶胞质量为 ![]() g,C﹣C键长为b pm,则上、下底面为菱形,上底面棱长为b pm×
g,C﹣C键长为b pm,则上、下底面为菱形,上底面棱长为b pm× ![]() ×2=
×2= ![]() b pm,石墨的层间距为apm,则晶胞高为2a pm,则晶胞密度为
b pm,石墨的层间距为apm,则晶胞高为2a pm,则晶胞密度为 ![]() g÷{[2×
g÷{[2× ![]() ×
× ![]() b×10﹣10×
b×10﹣10× ![]() b×10﹣10×sin60°cm]×2a×10﹣10cm}=
b×10﹣10×sin60°cm]×2a×10﹣10cm}= ![]() g.cm﹣3 , 所以答案是:4;
g.cm﹣3 , 所以答案是:4; ![]() .
.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
【题目】乙烯发生的下列反应中,不属于加成反应的是 ( )
A. 与氢气反应生成乙烷
B. 与水反应生成乙醇
C. 与溴水反应使之褪色
D. 与氧气反应生成二氧化碳和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由C16O和C18O组成的混合气体与同温、同压下空气(平均相对分子质量为29)的密度相同,则下列关系正确的是( )
A.混合气体中C16O和C18O的分子数之比为14:15
B.混合气体中C16O和C18O的物质的量之比为1:1
C.混合气体中C16O和C18O的质量之比为15:14
D.混合气体中C16O和C18O的密度之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使石蕊试液变红的溶液中:I﹣、MnO4﹣、NO3﹣、Na+
B.含有大量Fe3+的溶液:NH4+、HCO3﹣、SO42﹣、AlO2﹣
C.水电离出C(H+)=1.0×10﹣12mol/L 的溶液:Cl﹣、Na+、ClO﹣、NH4+
D.澄清透明的溶液:Cu2+、Fe3+、SO42﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( ) 
A.洗气瓶中产生的沉淀是碳酸钡
B.从Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是亚硫酸钡
D.在Z导管口有红棕色气体出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了减少城市空气污染,要求使用无铅汽油,所谓无铅汽油是指( )
A.不用铅桶装的汽油
B.不含四乙基铅的汽油
C.不含Pb(NO3)2的汽油
D.不含氧化铅的汽油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定.请回答:
(1)氢氧燃料电池的能量转化主要形式是 , 在导线中电子流动方向为(用a、b表示).
(2)负极反应式为 .
(3)电极表面镀铂粉的原因为 .
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能.因此,大量安全储氢是关键技术之一.金属锂是一种重要的储氢材料,吸氢和放氢原理如下: I.2Li+H2 ![]() 2LiH
2LiH
Ⅱ.LiH+H2O═LiOH+H2↑
①反应I中的还原剂是 . 反应Ⅱ中的氧化剂是 .
②已知LiH固体密度为0.82g/cm3 . 用镁吸收224L(标准状况)H2 , 生成的LiH体积与被吸收的H2体积比为 .
③由②生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( ) 
A.由氯化钠制备纯碱的过程中,利用了物质溶解度的差异
B.用Cl2制备漂白粉时,是将Cl2通入澄清石灰水中
C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应
D.图示转化反应都是氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com