
| A. | Al2O3和稀盐酸 | B. | Al2O3和水 | C. | Al2(SO4)3和NaOH | D. | AlCl3和氨水 |
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:多选题
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50s的平均速率v(Cl2)=0.0016 mol•L-1•min-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol•L-1,则该反应的△H<0 | |
| C. | 温度为T时,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) | |
| D. | 温度为T时,起始时向容器中充入0.5 mol PCl3和0.5 mol Cl2,达到平衡时,PCl3的转化率小于80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2项 | B. | 3项 | C. | 4项 | D. | 5项 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题


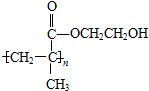 .
.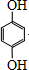 .
.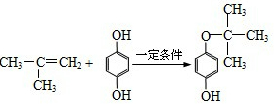 ,反应类型是加成反应.
,反应类型是加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol•L碳酸钠溶液中,阴离子数目小于0.1NA | |
| B. | 0.lmol铁粉与足量水蒸气反应生成的H2分子数目为0.1NA | |
| C. | 常温常压下,6g乙酸所含共价键数目为0.7NA | |
| D. | 1mol苯和苯甲酸的混合物完全燃烧时消耗O2的分子数为7.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验结论 |
| ①氯水+1mLCCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1mLCCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1mLCCl4,振荡,静置,观察四氯化碳层颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳分子的电子式为: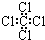 | |
| B. | C1-的结构示意图: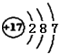 | |
| C. | 醋酸的电离方程式:CH3COOH+H2O?CH3COO-+H3O+ | |
| D. | 聚丙烯的结构简式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 产生气体的质量为0.3g | |
| B. | 合金中镁与铝的物质的量之比为1:2 | |
| C. | 溶液X中剩余NaOH的物质的量为0.2 mol | |
| D. | 向溶液X中通入足量C02,过滤,将沉淀充分灼烧得固体15.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+,HCO3-,Cl-,K+ | B. | K+,SO32-,ClO-,Na+ | ||
| C. | Fe2+,H+,SO42-,NO3- | D. | Fe3+,SCN-,Na+,CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com