
����Ŀ���״���һ�ֿ�������Դ����CO2�Ʊ��״��Ĺ��̿����漰�ķ�Ӧ���£���Ӧ��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H1=-49.58kJ��mol-1
CH3OH(g)+H2O(g) ��H1=-49.58kJ��mol-1
��Ӧ��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H2
CO(g)+H2O(g) ��H2
��Ӧ��CO(g)+2H2(g)![]() CH3OH(g) ��H3=-90.77kJ��mol-1
CH3OH(g) ��H3=-90.77kJ��mol-1
�ش��������⣺
��1����Ӧ��ġ�H2=______________��
��2����Ӧ���ܹ��Է����е�������__________ (��ϵ��¶ȡ����� �ϸ��¶ȡ����κ��¶ȡ�)
��3�����£������ܱ������У����ڷ�Ӧ������˵������˵���÷�Ӧ�ﵽ��ѧƽ��״̬����________��
A.���������ܶȲ��ٱ仯
B.��������ƽ����Է����������ٱ仯
C.CO2��H2��CH3OH��H2O�����ʵ���֮��Ϊ1��3��1��1
D.�״��İٷֺ������ٱ仯
��4�����ڷ�Ӧ��ͬ�¶ȶ�CO2��ת���ʼ�������Ч��Ӱ����ͼ��ʾ�������й�˵������ȷ����__________��

A.�����������䣬����ʹ�ô�������250��ʱCO2��ƽ��ת���ʿ���λ��M1
B.�¶ȵ���250��ʱ�����¶����״��IJ�������
C.M��ʱƽ�ⳣ����N��ʱƽ�ⳣ����
D.ʵ�ʷ�ӦӦ�������ڽϵ͵��¶��½��У������CO2��ת����
��5������1L�ܱ������г���3molH2��1molCO2������Ӧ��250��ʱ��Ӧ��ƽ�ⳣ��K=______����Ҫ��һ����״�����������ɲ�ȡ�Ĵ�ʩ��_________________��
��6����ͼ�ǵ��Na2CO3��Һ��װ��ͼ��

�����ĵ缫��ӦʽΪ________________
���𰸡�+41.19kJ��mol-1 �ϵ��¶� BD ABD 0.148(����![]() ) ����ѹǿ(�����¶�) 2H++2e-==H2����2H2O+2e-==H2��+2OH-
) ����ѹǿ(�����¶�) 2H++2e-==H2����2H2O+2e-==H2��+2OH-
��������
���⿼���˹���ɣ��Ȼ�ѧ��Ӧ������أ�ֻ��ʼ̬����̬�йأ���H2=��H1-��H3=+41.19kJ/mol����G==��H��T��S��TΪ�¶ȣ���G<0�����Է����У���Ӧ��H<0, ��S<0���ϵ��¶ȿ��Է����У�ƽ��״̬���жϣ�ͬһ���ʵ����淴Ӧ������ȣ���������=m/V����������������䣬�ܶ���ʼ���ղ��䣬������Ϊ�ж����ݣ�M=m/n���������䣬���ʵ������٣������ж����ݣ���Ӧ����������ƽ��ʱ�ı�����һ��Ϊ1��3��1��1�������ԣ�ֻҪƽ����״��İٷֺ������ٱ仯�����ԣ���ѧ��Ӧ������ѡ��Ҫ���Ƿ�Ӧʱ�IJ�������Ҫ���Ƿ�Ӧ�����ʣ�![]() ��250��ʱת����Ϊ50%������������ʧ���ӣ���Һ��Ϊˮ�ṩ������������ʧ���ӣ������������Ӻ������������������ƶ���������������ˮ�ṩ�������ӵõ��ӣ�����������
��250��ʱת����Ϊ50%������������ʧ���ӣ���Һ��Ϊˮ�ṩ������������ʧ���ӣ������������Ӻ������������������ƶ���������������ˮ�ṩ�������ӵõ��ӣ�����������
��1�����⿼���˹���ɣ��Ȼ�ѧ��Ӧ������أ�ֻ��ʼ̬����̬�йأ���H2=��H1-��H3=+41.19kJ/mol����2����G==��H��T��S��TΪ�¶ȣ���G<0�����Է����У���Ӧ��H<0, ��S<0���ϵ��¶ȿ��Է����У���3��ƽ��״̬���жϣ�ͬһ���ʵ����淴Ӧ������ȣ���������=m/V����������������䣬�ܶ���ʼ���ղ��䣬������Ϊ�ж����ݣ�M=m/n���������䣬���ʵ������٣������ж����ݣ���Ӧ����������ƽ��ʱ�ı�����һ��Ϊ1��3��1��1�������ԣ�ֻҪƽ����״��İٷֺ������ٱ仯�����ԣ���Ϊ��BD��(4)A.�����Է�Ӧ������Ӱ�죬��ƽ�������Ӱ�죬A����B.�÷�ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���������ߣ�B��ȷ��C.�����¶�ƽ�������ƶ�����ѧƽ�ⳣ����С��C����D. ʵ�ʷ�ӦӦ�������ڴ�Ч�����ʱ��D����ΪABD ��
(5) CO2 + 3H2![]() CH3OH + H2O 250��ʱת����Ϊ50%
CH3OH + H2O 250��ʱת����Ϊ50%
��ʼ����1 3
��Ӧ����0.5 1.5 0.5 0.5
ƽ�⣺ 0.5 1.5 0.5 0.5
![]() ��K=0.148����״����������Ϊ������ѹǿ(�����¶�)�� (6) ����������ʧ���ӣ���Һ��Ϊˮ�ṩ������������ʧ���ӣ������������Ӻ������������������ƶ���������������ˮ�ṩ�������ӵõ��ӣ�����������2H++2e-==H2����2H2O+2e-==H2��+2OH-
��K=0.148����״����������Ϊ������ѹǿ(�����¶�)�� (6) ����������ʧ���ӣ���Һ��Ϊˮ�ṩ������������ʧ���ӣ������������Ӻ������������������ƶ���������������ˮ�ṩ�������ӵõ��ӣ�����������2H++2e-==H2����2H2O+2e-==H2��+2OH-



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A(C11H8O4)��һ���������ʣ���NaOH��Һ�м��ȷ�Ӧ�����ữ�ɵõ�������B��C���ش��������⣺
��1��B�ķ���ʽΪC2H4O2��������ֻ��һ�������ţ�����NaHCO3��Һ��Ӧ�������������B�Ľṹ��ʽ��_________��д��B��NaHCO3��Һ��Ӧ�Ļ�ѧ����ʽ________��д�������ܷ���������Ӧ��B��ͬ���칹��Ľṹ��ʽ_________��________��
��2��C�Ƿ��㻯������б������л������Է�������Ϊ180����̼����������Ϊ60.0%�������������Ϊ4.4%������Ϊ������C�ķ���ʽ��_________������֪�����ԭ��������C��12��O��16��H��1��
��3����֪C�ı�����������ȡ����������һ��ȡ��������Ϊ��X����֧�����Һ�������������Ȼ�̼��Һ��1:1��ȫ��Ӧ�Ĺ������Լ���������̼��������Һ��Ӧ�ų�����Ĺ����ţ����ȡ�����ϵĺ��й�����������_________����������ȡ������ͬ��������Ϊ_______��������ͬ������ȡ�����ֱ�λ��ȡ��������X������λ�Ͷ�λ����C�Ľṹ��ʽ��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��![]() �ں��º����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
�ں��º����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
![]() ��λʱ��������n
��λʱ��������n![]() ��ͬʱ����2n
��ͬʱ����2n![]() ��
��
![]() ��λʱ��������n
��λʱ��������n![]() ��ͬʱ����2nmolNO��
��ͬʱ����2nmolNO��
![]() ����������ɫ���ٸı��״̬��
����������ɫ���ٸı��״̬��
![]() ���������
���������![]() ���䣻
���䣻
![]() ������������NO������������ȣ�
������������NO������������ȣ�
![]() ������ѹǿ����ʱ��仯���仯��
������ѹǿ����ʱ��仯���仯��
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������¶��£�0.1molN2(g)��0.3molH2(g)���ܱ������з�����Ӧ��N2(g)+3H2(g)![]() 2NH3(g) ��H=-akJ��mol-1(a>0)������˵����ȷ����
2NH3(g) ��H=-akJ��mol-1(a>0)������˵����ȷ����
A. �ﵽ��ѧƽ��״̬ʱ����Ӧ�ų�0.la kJ����
B. �ﵽ��ѧƽ��״̬ʱ��v��(NH3)��v��(N2)=2��1
C. n( N2)��n(H2)��n(NH3)=l��3��2ʱ��˵���÷�Ӧ�ﵽƽ��
D. ��С����������õ�����ʾ�ķ�Ӧ���ʣ�v��(N2)����v��(N2)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���Ӧ��N2(g��+3H2(g��![]() 2NH3(g����H=-92.4kJmol-1���ڷ�Ӧ�����У�����Ӧ���ʵı仯��ͼ������˵����ȷ��������
2NH3(g����H=-92.4kJmol-1���ڷ�Ӧ�����У�����Ӧ���ʵı仯��ͼ������˵����ȷ��������
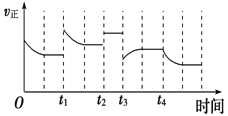
A. t1ʱ������������Ũ��
B. t2ʱʹ���˴���
C. t3ʱ������ѹǿ
D. t4ʱ�������¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������ӵ�ص��ܷ�ӦʽΪ2Li+FeS=Fe+Li2S��LiPF6��SO(CH3)2Ϊ����ʣ��øõ��Ϊ��Դ��⺬�����Է�ˮ���õ�����Ni��ʵ��װ����ͼ��ʾ������˵������ȷ����

A. �缫YΪLi
B. �������У�b��NaCl��Һ�����ʵ���Ũ�Ƚ����ϼ�С
C. X����ӦʽΪFeS+2Li++2e-=Fe+Li2S
D. ����ͼ��������Ĥȥ������a��b���Һϲ������ⷴӦ�ܷ���ʽ�����ı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�Fe(OH)3(s)��Cu(OH)2(s)�ֱ�����Һ�дﵽ�����ܽ�ƽ��ı���ҺpH������������Ũ�ȱ仯��ͼ��ʾ����ͼ�����������ж���ȷ����

A. [Ksp[Cu(OH)2]<Ksp[Fe(OH)3]
B. d���������Һ��Fe(OH)3�ѹ����͡�Cu(OH)2δ����
C. ������NH4Cl�����ʹ��Һ��a��䵽b��
D. b��c���������Fe(OH)3��Cu(OH)2�ܽ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ����
A.ú�Ϳ���ʯ�ͷ����ã�������ȼ�Ϻͱ�������������
B.���ۡ���֬�������ʶ���ˮ�⣬��ˮ����ﲻͬ
C.���顢�Ҵ������ᡢ�����������ܷ���ȡ����Ӧ
D.��ϩ�ͱ�����ʹ��ˮ��ɫ������ɫ��ԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п���㷺Ӧ����ҽҩ�����ũҵ��������ҵ��������п����Ҫ�ɷ�ΪZnO������ZnSiO3��FeCO3��CuO�ȣ�����ZnSO47H2O��һ��������ͼ��

��1�������IJ�����____________��
��2��������У���pHԼΪ5.1����Һ�м��������أ�����Fe(OH)3��MnO(OH)2���ֳ������÷�Ӧ�����ӷ���ʽΪ____________________________________��
��3��������У�����п�۵�������______________��
��4��ȡ28.70 g ZnSO47H2O��������ͬ�¶ȣ�ʣ�����������仯����ͼ��ʾ��ʵ������Ӧ����____________�����������ƣ�������Ʒ���������ݣ�100��ʱ������Ӧ�Ļ�ѧ����ʽΪ ______________________________��680��ʱ���ù���Ļ�ѧʽΪ__________������ĸ���ţ���
a��ZnO b��Zn3O(SO4)2 c��ZnSO4 d��ZnSO4H2O

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com