
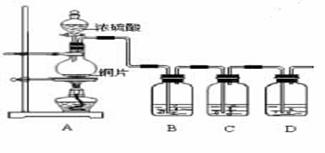
某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如下图所示的装置。
请回答下列问题。
(1)铜和浓硫酸反应的化学方程式为 。
(2)B瓶中盛有品红溶液,观察到品红溶液褪色,这是因为 SO2具有 。(填选项的字母,下同),C瓶中盛有新制的氯水,观察到氯水褪色,这是因为SO2具有 。
A.氧化性 B.还原性 C.漂白性
(3)D瓶中盛有NaOH溶液,作用是 。
(4)充分反应后,小组同学发现铜和硫酸都有剩余。若想使剩余的铜片溶解,可再加入(多选) (填选项的字母) 。。
A.HNO3 B.NaNO3 C.Fe2O3 D.Na2CO3
科目:高中化学 来源: 题型:
年来,许多专家对石灰氮重新进行了深入研究,这也使得石灰氮这一古老的肥料又焕发了新的活力。石灰氮是由Ca、N、C等三种元素组成的盐,其含钙、氮的质量分数分别为50 %、35%。石灰氮完全水解后的产物是固体A和气体B,其中B是制取氮肥的主要原料。固体A在高温下分解生成D和气体C。B的催化氧化产物为E和F,F继续氧化后的产物G遇到E生成一种工业强酸。将G和F的混合物溶解在接近零度的水中,即生成亚硝酸的水溶液,该反应可表示如下G+F+H2O=2HNO2(已配平)。请回答下列问题:
%、35%。石灰氮完全水解后的产物是固体A和气体B,其中B是制取氮肥的主要原料。固体A在高温下分解生成D和气体C。B的催化氧化产物为E和F,F继续氧化后的产物G遇到E生成一种工业强酸。将G和F的混合物溶解在接近零度的水中,即生成亚硝酸的水溶液,该反应可表示如下G+F+H2O=2HNO2(已配平)。请回答下列问题:
(1)石灰氮的化学式为 。
(2)足量B和C与饱和氯 化钠溶液的反应是化工生产中生产某种重要化工产品的重要反应,试写出其化学方程式
化钠溶液的反应是化工生产中生产某种重要化工产品的重要反应,试写出其化学方程式  。
。
(3)亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸,很不稳定,通常在室温下立即分解。在酸性条件下,当NaNO2与KI按物质的量1:1恰好完全反应,且I— 被氧化为I2时,含氮产物为 (填化学式)。要得到稳定HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质中不适合使用是 (填序号)。
a、磷酸 b、二氧化碳 c、稀硫酸 d、二氧化硫 e、次氯酸
(4)工业废水中的NO2— 可用铝粉除去。已知此反应体系中包含Al、NaAlO2、NaNO2、NaOH、NH3、H2O六种物质。写出上述反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
乙醇、乙酸都是有机化工重要的基础原料。
(1).空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为 。
(2).浓硫酸催化下,乙酸和乙醇生成乙酸乙酯
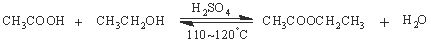
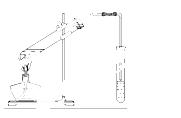
某化学兴趣小组的同学用以下装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、 3mL乙醇、2mL乙酸,其具体操作是 。
3mL乙醇、2mL乙酸,其具体操作是 。
②小试管中装的是浓Na2CO3溶液,导气管不插入液面下是为了防止 。
③相关物质的部分性质:
| 乙醇 | 乙酸 | 乙酸乙酯 | |
| 沸点 | 78.0℃ | 117.9℃ | 77.5℃ |
| 水溶性 | 易溶 | 易溶 | 难溶 |
根据上表数据有同学提出可用水替代小试管中的Na2CO3溶液,你认为可行吗?说明理由: 。④分离小试管中的乙酸乙酯应使用的仪器名称是 ;
⑤分离时,乙酸 乙酯应该从仪器 (填“下口放” 或“上口倒出”)。
乙酯应该从仪器 (填“下口放” 或“上口倒出”)。
⑥兴趣小组多次试验后,测出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如下表:
| 实验序号 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| a | 2 | 2 | 1.33 |
| b | 3 | 2 | 1.57 |
| c | 4 | 2 | X |
| d | 5 | 2 | 1.76 |
| e | 2 | 3 | 1.55 |
表中数据X的范围是 ;实验a与实验e探究的目的是
查看答案和解析>>
科目:高中化学 来源: 题型:
在生活、生产及化学研究中,人们经常需要根据不同原子、分子或离子的某些特征反应对物质进行区别、检验等。下列说法正确的是
A.用KOH溶液可以将NH4Cl、NaBr、CuSO4、FeCl3区别开
B.C、CuO、Fe三种物质的粉末都是黑色的,用稀盐酸不能将它们区别开
C.某溶液中加入稀盐酸有无色气体产生,该气体能使澄清石灰水变浑浊,则此溶液中一定含有CO32¯
D.可以用BaCl2溶液和稀硝酸检验Na2SO3是否变质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分类或归类正确的是( )
①铝热剂、纯净矿泉水、冰水混合物均为混合物
②NaOH、HD、IBr均为化合物
③明矾、烧碱、硫酸均为强电解质
④C60、金刚石、石墨均为碳的同素异形体
⑤碘酒、淀粉溶液、水雾、纳米材料均为胶体.
A.①②③④⑤ B. ③④⑤ C. ②④⑤ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液既能溶解Al(OH)3,又能溶解Al,但不能溶解Fe,在该溶液中可以大量共存的离子组是( )
|
| A. | K+、Na+、HCO | B. | Na+、SO |
|
| C. | NH | D. | H+、K+、Cl﹣、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
某强碱性溶液中可能含有K+、NH4+、Al3+、AlO2﹣、SO42﹣、SiO32﹣、CO32﹣、Cl﹣中的某几种离子,现进行如下实验:
①取少量溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成.
②另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
(1)原溶液中肯定存在的离子是 肯定不存在的离子是
(2)已知一定量的原溶液中慢慢滴入5mL 0.2mol/L盐酸时,产生的沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g,则原溶液中是否含有Cl﹣?(通过列式说明) .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的分离或鉴别正确的是
A.除去混在氯化钠固体中的氯化铵或单质碘均可用加热升华的方法
B.若FeCl2溶液中含有I-杂质,可用过量的Cl2氧化后进行萃取分液
C.从海水中提取溴,一般是向浓缩后的海水中通入Cl2,再鼓入热空气或水蒸汽将溴分离出来
D.鉴别固体Na2CO3和NaHCO3,可以分别配成溶液,再加入澄清石灰水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com