
【题目】Ⅰ.氯化亚铜(![]() )是一种重要的化工产品,常用作有机合成催化剂, 还可用于颜料, 防腐等工业。 该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色。已知 pH 为 5 时,+2 价铜已开始以碱式盐的形式沉淀。 某兴趣小组去一家回收含铜电缆废料的工厂做社会调查,技术人员向他们展示了处理废料的综合利用方案:
)是一种重要的化工产品,常用作有机合成催化剂, 还可用于颜料, 防腐等工业。 该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色。已知 pH 为 5 时,+2 价铜已开始以碱式盐的形式沉淀。 某兴趣小组去一家回收含铜电缆废料的工厂做社会调查,技术人员向他们展示了处理废料的综合利用方案:
![]()
(1)反应①符合绿色化学思想,且 A 为难挥发性酸,B 为气体,则加入的 A 是_______,通入的 B是______________。 (均写名称)
(2)反应②的离子方程式是___________。 为提高![]() 的产率,常在反应②的溶液中加入适量稀碱溶液但体积不能偏大,往往控制PH为3.5.这样做的目的是_________________。
的产率,常在反应②的溶液中加入适量稀碱溶液但体积不能偏大,往往控制PH为3.5.这样做的目的是_________________。
(3) 最后得到的氯化亚铜需要_______________保存。
Ⅱ.回收利用炼铜工业产生的排放物,既能节约资源,又能保护环境。
(4)烟灰中金属元素以硫酸盐和氧化物形态存在,其中锌、铅的含量最大,其次为铜、铁等。 烟灰的回收利用工艺如下:

①“一次浸取”铜浸出率较低,原因是烟灰中部分铜元素以________(填化学式)残留在浸
出渣中,“沉铜”可得到单质铜,该步骤应加入的试剂是__________________________。
② 从贵金属阳极泥中可提取粗银。 电解法精炼粗银时采用![]() 和
和![]() 的混合液作电解液,阴极的主要电极反应式为_______。 阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,该副反应的电极反应式为_______________________________。
的混合液作电解液,阴极的主要电极反应式为_______。 阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,该副反应的电极反应式为_______________________________。
【答案】 稀硫酸 空气 2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H+ OH-中和了反应生成的H+,有利于反应向右进行,提高CuCl的产率;所加碱液偏大时会生成Cu(OH)2沉淀,降低CuCl产率,且造成产物不纯 隔绝空气、密闭保存 CuO 锌粉(或铁粉) Ag++e-=Ag NO3-+4H++3e-=NO+2H2O
【解析】(1)反应①符合绿色化学思想,且 A 为难挥发性酸,A是稀硫酸。稀硫酸不能溶解铜,所以B具有氧化性,则B为空气。(2)反应②是铜离子氧化亚硫酸钠,反应的离子方程式是2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H+。 为提高CuCl的产率,常在反应②的溶液中加入适量稀碱溶液但体积不能偏大,往往控制pH为3.5,适量的碱能中和氢离子促进反应向右进行,所以这样做的目的是OH-中和了反应生成的H+,有利于反应向右进行,提高CuCl的产率;所加碱液偏大时会生成Cu(OH)2沉淀,降低CuCl产率,且造成产物不纯。(3)CuCl露置于空气中易被氧化为绿色的高价铜盐,因此最后得到的氯化亚铜需要隔绝空气、密闭保存保存。(4)①氧化铜不溶于水,因此烟灰中部分铜元素以CuO残留在浸出渣中。“沉铜”可得到单质铜,由于后续要除铁,所以该步骤应加入的试剂是锌粉(或铁粉)。②银离子氧化性强于铜离子,所以阴极的主要电极反应式为Ag++e-=Ag。阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,气体是NO,该副反应的电极反应式为NO3-+4H++3e-=NO↑+2H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大。A、D同主族;B、D、E三种元素原子的最外层电子数之和为10;E的单质可做半导体材料;C与E两元素形成的化合物可与A、C、D形成的化合物Y发生反应;B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M。1molM中含有42mol电子。回答下列问题:
(1)E元素在周期表中的位置________;化合物M中含有的化学键类型有________________
(2)比较B、C、E形成的气态氢化物的稳定性由强到弱的顺序是(用化学式表示):______;写出C与A形成的18e-化合物的结构式_____________;
(3)用电子式表示A2C的形成过程:________________________________________
(4)写出题中生成M的化学方程式_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种医药中间体,其结构简式如图所示。下列有关化合物X的说法正确的是

A.分子中两个苯环一定处于同一平面
B.不能与饱和Na2CO3溶液反应
C.在酸性条件下水解,水解产物只有一种
D.1 mol化合物X最多能与2 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨主要用于制造硬质或耐高温的合金。自然界中黑钨矿的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含少量Si、P、As的化合物。黑钨矿冶炼钨的工艺流程如下:
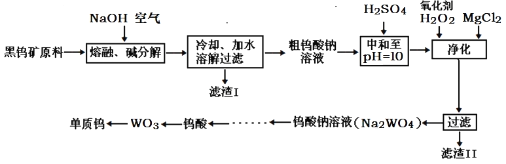
已知:①滤渣I的主要成份是Fe2O3、MnO2;
②上述流程中,除最后一步外,其余步骤中钨的化合价未变;
③常温下钨酸难溶于水。
回答下列问题:
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为__________,请写出MnWO4在熔融条件下发生碱分解反应生成MnO2的化学方程式____________。
(2)上述流程中向粗钨酸钠溶液中加硫酸调pH=10后,溶液中的杂质阴离子为SiO32-、HAsO32-、HAsO42-、HPO42-等,“净化”过程中,加入H2O2的目的是__________,滤渣Ⅱ的主要成分是__________。
(3)高温下密闭容器中用H2还原WO3可得到金属钨,其反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表。
温度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
主要成分 | WO3 W2O5 WO2 W |
已知:温度过高时,WO2(s)可转变为WO2(g)。
WO2(s)+2H2(g) ![]() W(s)+2H2O(g) △H =+66.0 kJ·mol-1
W(s)+2H2O(g) △H =+66.0 kJ·mol-1
WO2(s) ![]() WO2(g) △H =+203.9 kJ·mol-1
WO2(g) △H =+203.9 kJ·mol-1
则在700℃时,WO2(g)与H2(g)反应生成固体W(s)的热化学方程式为_____________。
(4)已知氢氧化钙和钨酸钙(CaWO4)都是微溶性的电解质,两者的溶解度均随温度升高而减小。不同温度下两种物质的沉淀溶解平衡曲线如右图,则T1时Ksp(CaWO4) =________。
在钨酸钠溶液中加入石灰乳得到大量钨酸钙,则T2时该反应的平衡常数为________。
(5)利用电解法可以从碳化钨(WC)废料中回收钨。电解时,用碳化钨做阳极,不锈钢做阴极,盐酸为电解液,阳极析出钨酸并放出CO2,该阳极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同物质的量的下列有机物,充分燃烧,消耗氧气的量相同的是
A. C3H4和C2H6
B. C3H6和C3H8O
C. C3H6O2和C3H8O
D. C3H8O和C4H8O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学要研究如何合理、高效地进行金属矿物的开发利用。
(1)以下方法可用于工业冶炼金属的是(_______)
a.电解熔融AlCl3获取金属铝 b.电解MgCl2溶液获取金属镁
c.用CO还原铁矿石来获取金属铁 d.电解饱和食盐水来获取金属钠
(2)按图所示装置进行实验。

【实验现象】反应剧烈,火星四射,漏斗下方有红热熔融物流出。
由此判断该反应是________(填“吸热”或“放热”)反应,其反应的化学方程式是___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
胡椒醛衍生物在香料、农药、医药等领域有着广泛用途,以香草醛(A)为原料合成 5-三氟甲基胡椒醛(E)的路线如图所示:

已知:Ⅰ.酚羟基能与 CH2I2 发生反应③,而醇羟基则不能。

(1)反应③的类型是__________。
(2)香草醛中含氧官能团的名称为醚键、______和______香草醛分子中最多有_____个碳原子共平面。
(3)写出香草醛在加热的条件下与新制的氢氧化铜反应的化学方程式___________。
(4)满足下列条件的香草醛的芳香族类同分异构体共有________种(不含立体结构):
①不能与氯化铁溶液发生显色反应 ②能与碳酸氢钠溶液反应放出气体
③1mol 该化合物与足量钠反应产生 2g 氢气。
其中核磁共振氢谱显示其有 5 种不同化学环境的氢原子的结构简式为:________________________。
(5)以香草醛和 2-氯丙烷为原料,用四个步骤合成香草醛缩丙二醇(![]() )
)
写出合成流程图(无机试剂和溶剂任用)。 合成流程图示例如下:
![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛对体液无毒且有惰性,能与肌肉和骨骼生长在一起,因而有“生物金属”之称。下列有关![]() Ti和
Ti和![]() Ti的说法中,正确的是( )
Ti的说法中,正确的是( )
A. ![]() Ti和
Ti和![]() Ti是中子数不同质子数相同的同种核素
Ti是中子数不同质子数相同的同种核素
B. 分别由![]() Ti和
Ti和![]() Ti组成的金属钛单质互称为同分异构体
Ti组成的金属钛单质互称为同分异构体
C. ![]() Ti和
Ti和![]() Ti互为同素异形体
Ti互为同素异形体
D. ![]() Ti和
Ti和![]() Ti原子的核外电子排布相同
Ti原子的核外电子排布相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将一定量的N2和H2充入固定体积的密闭容器中进行反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
(1)下列描述能说明该可逆反应达到化学平衡状态的有 。
A.容器内的压强不变
B.容器内气体的密度不变
C.相同时间内有3 mol H-H键断裂,有6 mol N-H键形成
D.消耗0.1molN2的同时消耗0.2molNH3
(2)若起始时向容器中充入10 mol·L-1 的N2和15 mol·L-1的H2 ,10 min时测得容器内NH3的浓度为1.5mol·L-1。
列式计算:
①10min内N2表示的反应速率;
②此时H2的转化率。(转化率是指某时刻某物质已经转化的量与该物质起始量之比)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com