
【题目】太阳能电池板材料除单晶硅外,还有氮、硼、硒、钛、钴、钙等元素组成的化学物质。
⑴钙原子基态时的电子排布式为____________________,金属钴堆积方式与镁相似,都属于六方最密堆积,其配位数是____。
⑵氮元素的第一电离能在同周期中(稀有气体除外)从大到小排第___位;写出与NO3-互为等电子体的一种非极性分子的化学式__________。
⑶晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图),其中有两个原子为10B,其余为11B,则该结构单元有_____________种不同的结构类型。己知硼酸(H3BO3)为一元弱酸,解释其为一元弱酸的原因______________。硼酸的结构与石墨相似,层内的分子以氢键相连,含1 mol硼酸的晶体中有___mol氢键。

⑷硒是动物体必需的营养元素。SeO2是硒的重要化合物,SeO2的价层电子对互斥模型是_______________。
⑸在浓的TiCl3的盐酸溶液中加入乙醚,并通入HC1至饱和,可得到配位数为6,组成为 TiCl36H2O的晶体,该晶体中两种配体的物质的量之比为1:5,则该配离子的化学式为:__________________。
⑹钴晶体的一种晶胞是一种体心立方结构(如图所示),若该晶胞的边长为a nm,密度为ρ gcm-3,NA表示阿伏加德罗常数的值,则钴的相对原子质量可表示为_________________。

【答案】1s22s22p63s23p64s2 12 2 SO3等 3 H3BO3与一个水分子可形成配位键,电离产生[B(OH)4]-和一个H+ 3 平面三角形 [TiCl(H2O)5]2+ ![]()
【解析】
⑴钙为20号元素,其核外有20个电子,金属钴堆积方式与镁相似。
⑵同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于同周期相邻元素的,S = O = N-,容易写出与NO3-互为等电子体的一种非极性分子。
⑶两个10B有3位置,为上下顶点位置,其中一个处于上顶点,另外的一个处于上层阴影中顶点,或者下层阴影中顶点,有3种结构,H3BO3与一个水分子可形成配位键,电离产生[B(OH)4]-和一个H+,则硼酸一元弱酸;1个硼酸分子形成了6个氢键,但每个氢键是2个硼酸分子共用的,所以平均含3个氢键,则含有1 mol H3BO3的晶体中有3mol氢键。
⑷ SeO2分子中价层电子对个数= δ键个数![]() 孤电子对个数。
孤电子对个数。
⑸在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl36H2O的绿色晶体,该晶体中两配体的物质的量之比为1:5,则配体中有1个![]() 、5个H2O,2个氯离子位于外界。
、5个H2O,2个氯离子位于外界。
⑹先计算晶胞中钴原子的数目,根据密度公式,得出钴的相对原子质量。
⑴钙为20号元素,其核外有20个电子,则钙原子基态时的核外电子排布式为1s22s22p63s23p64s2,金属钴堆积方式与镁相似,都属于六方最密堆积,其配位数是12,
故答案为:1s22s22p63s23p64s2;12。
⑵同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于同周期相邻元素的,故第二周期第一电离能:F > N > O > C > Be > B > Li,原子数目相等、价电子总数也相等的微粒互为等电子体,与NO3-互为等电子体的一种非极性分子为SO3等;故答案为:2;SO3等。
⑶两个10B有3位置,为图中 上下顶点位置,其中一个处于上顶点,另外的一个处于上层阴影中顶点,或者下层阴影中顶点,有3种结构,H3BO3与一个水分子可形成配位键,电离产生[B(OH)4]-和一个H+,则硼酸一元弱酸;1个硼酸分子形成了6个氢键,但每个氢键是2个硼酸分子共用的,所以平均含3个氢键,则含有1 mol H3BO3的晶体中有3mol氢键;故答案为:3;H3BO3与一个水分子可形成配位键,电离产生[B(OH)4]-和一个H+;3。
上下顶点位置,其中一个处于上顶点,另外的一个处于上层阴影中顶点,或者下层阴影中顶点,有3种结构,H3BO3与一个水分子可形成配位键,电离产生[B(OH)4]-和一个H+,则硼酸一元弱酸;1个硼酸分子形成了6个氢键,但每个氢键是2个硼酸分子共用的,所以平均含3个氢键,则含有1 mol H3BO3的晶体中有3mol氢键;故答案为:3;H3BO3与一个水分子可形成配位键,电离产生[B(OH)4]-和一个H+;3。
⑷ SeO2分子中价层电子对个数= δ键个数![]() 孤电子对个数=
孤电子对个数= ![]() ,则其价层电子对互斥模型为平面三角形,故答案为:平面三角形。
,则其价层电子对互斥模型为平面三角形,故答案为:平面三角形。
⑸在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl36H2O的绿色晶体,该晶体中两配体的物质的量之比为1:5,则配体中有1个![]() 、5个H2O,2个氯离子位于外界,则该配离子的化学式为[TiCl(H2O)5]2+;故答案为:[TiCl(H2O)5]2+。
、5个H2O,2个氯离子位于外界,则该配离子的化学式为[TiCl(H2O)5]2+;故答案为:[TiCl(H2O)5]2+。
⑹晶胞中钴原子的数目为![]() ,根据密度
,根据密度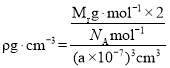 ,得出钴的相对原子质量为
,得出钴的相对原子质量为![]() ;故答案为:
;故答案为:![]() 。
。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为___,3d能级上的未成对电子数为___。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是___。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为___,提供孤电子对的成键原子是___。
③氨的沸点___(填“高于”或“低于”)膦(PH3),原因是___。
(3)单质铜及镍都是由___键形成的晶体;元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是___。
(4)某镍白铜合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图,关闭活塞K,向A中充入1 molX、1 molY,向B中充入2 molX、2molY, 此时A、B的容积都是a L。在相同温度和催化剂存在的条件下,使两容器中各自发生下述反应:X(g)+Y(g)![]() 2Z(g)+W(g);△H<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4a L。下列说法正确的是
2Z(g)+W(g);△H<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4a L。下列说法正确的是
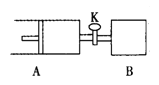
A.反应速率:v(B)<v(A)
B.平衡时Y的体积分数:A>B
C.打开K后达平衡时A的体积为2.4a L
D.A容器中X的转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮族元素包括N、P、As、Sb和Bi五种元素。
(1)下列关于氮族元素的说法正确的是___。
a.N2可用于填充霓虹灯。其发光原理是电子从能量较低的轨道跃迁到能量较高的轨道,以光的形式释放能量
b.P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na
c.基态As原子中,电子占据的最高能级为4d
d.Bi原子中最外层有5个能量相同的电子
(2)NH3在水中的溶解度比PH3大得多,其原因是___![]() 向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有___和___。
向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有___和___。
(3)PCl3分子中,Cl-P-Cl键的键角___109°28'(填“>”“<”或“2”![]() 。
。
(4)白磷(P4)是磷的一种单质,它属于分子晶体,其晶胞结构如图。已知该晶体的密度为ρg·cm-3,晶胞的边长为acm,则阿伏加德罗常数为___mol-1(用含p、a的式子表示![]() 。
。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
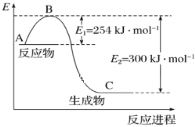
(1)上图是![]() 和
和![]() 反应生成
反应生成![]() 过程中能量的变化示意图,下列有关说法正确的是_______。
过程中能量的变化示意图,下列有关说法正确的是_______。
a. 反应物的总能量比生成物的总能量高
b. 反应物的活化能比生成物的活化能高
c. 反应物的总键能比生成物的总键能高
d. 该反应为熵增反应
(2)请写出![]() 和
和![]() 反应的热化学方程式:_______,决定该反应进行方向的主要判据为________。
反应的热化学方程式:_______,决定该反应进行方向的主要判据为________。
(3)试根据表中及图中数据计算![]() 的键能______________ kJ/mol;
的键能______________ kJ/mol;
化学键 |
|
|
键能/ kJ/mol | 390 | 943 |
(4)用![]() 催化还原
催化还原![]() 还可以消除氮氧化物的污染。已知:
还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=-akJ/mol
N2(g)+O2(g)=2NO(g);△H2=-bkJ/mol
若1molNH3还原NO至N2,则该反应过程中的反应热△H3=_____________kJ/mol(用含a、b的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究![]() 、NO、
、NO、![]() 、CO等大气污染气体的处理具有重要意义。
、CO等大气污染气体的处理具有重要意义。
(1)已知:CO可将部分氮的氧化物还原为![]() 。
。
反应I:![]()
反应II:![]()
则反应![]() 的
的![]() =___________kJ·mol-1。
=___________kJ·mol-1。
(2)一定条件下,将![]() 与CO以体积比1∶2置于恒容密闭容器中发生反应II,下列能说明反应达到平衡状态的是________________。
与CO以体积比1∶2置于恒容密闭容器中发生反应II,下列能说明反应达到平衡状态的是________________。
a. 体系压强保持不变 b. 容器中气体密度保持不变
c. 混合气体颜色保持不变d. 每消耗![]() 的同时生成
的同时生成![]()
(3)温度为T 容积为10L的恒容密闭容器中,充入1molCO和0.5mol![]() 发生反应:
发生反应:
![]() 实验测得生成的
实验测得生成的![]() 体积分数
体积分数![]() 随着时间的变化曲线如图1所示:
随着时间的变化曲线如图1所示:

①达到平衡状态时,![]() 的转化率为______,该温度下反应的平衡常数
的转化率为______,该温度下反应的平衡常数![]() _________。
_________。
②其它条件保持不变,再向上述平衡体系中充入![]() 、
、![]() 、
、![]() 、
、![]() 各
各![]() ,此时V(正)__________ V(逆)填“﹥”“ <”或“=”。
,此时V(正)__________ V(逆)填“﹥”“ <”或“=”。
4)![]() 法是工业上消除氮氧化物的常用方法,反应原理为
法是工业上消除氮氧化物的常用方法,反应原理为![]() ,在催化剂作用下,NO转化率与温度的关系如图2所示:图中A点处NO的转化率____________填“可能是”、“一定是”或“一定不是”该温度下的平衡转化率;B点之后,NO转化率降低的原因可能是______。
,在催化剂作用下,NO转化率与温度的关系如图2所示:图中A点处NO的转化率____________填“可能是”、“一定是”或“一定不是”该温度下的平衡转化率;B点之后,NO转化率降低的原因可能是______。
A. 平衡常数变大 B. 副反应增多
C. 催化剂活性降低 D. 反应活化能增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1,Na2O2(s)+CO2(g)===Na2CO3(s)+![]() O2(g) ΔH=-226 kJ·mol-1,根据以上热化学方程式判断,下列说法正确的是( )。
O2(g) ΔH=-226 kJ·mol-1,根据以上热化学方程式判断,下列说法正确的是( )。
A. CO的燃烧热为283 kJ
B. 下图可表示由CO生成CO2的反应过程和能量关系

C. 2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-452 kJ·mol-1
D. CO(g)与Na2O2(s)反应放出509 kJ热量时,转移电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、T均为短周期元素,X、Y、T原子最外层电子数之和为18。下列说法正确的是
![]()
A.X、Y、T三种元素最低价氢化物的沸点依次升高
B.X、Y和氢三种元素可共同形成离子化合物或共价化合物
C.物质WY2、ZY2一定都有熔点高、硬度大的特性
D.元素X、Y、T的最高正价的顺序为:T>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物![]() (甲)、
(甲)、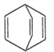 (乙)、
(乙)、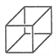 (丙)的分子式均为C8H8,下列说法不正确的是
(丙)的分子式均为C8H8,下列说法不正确的是
A. 甲、乙、丙在空气口燃烧时均产生明亮并带有浓烟的火焰
B. 甲、乙、丙中只有甲的所有原子可能处于同一平面
C. 等量的甲和乙分别与足量的溴水反应,消耗Br2的量:甲>乙
D. 甲、乙、丙的二氯代物数目最少的是丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com