
 ���ζ���������ʧ
���ζ���������ʧ| �ζ����� | ����NaOH��Һ����� | 0.1000mol/L��������/mL | ||
| �ζ�ǰ�̶� | �ζ���̶� | ��Һ���/mL | ||
| ��һ�� | 25.00 | 0.00 | 26.11 | 26.11 |
| �ڶ��� | 25.00 | 1.56 | 30.30 | 28.74 |
| ������ | 25.00 | 0.22 | 26.31 | 26.09 |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ܹ�ʹ���ȳ��ֻ�ɫ | B����Һ��pH>7 |
| C����Һ�У�c(H��)<c(OH��) | D����Һ�У�c(H��)>1��10��7mol��L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��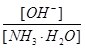 | B��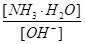 |
| C��[H+]�ͺ�[OH-]�ij˻� | D��OH-�����ʵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ��ֻ������HX��NaHCO3����NaY��Һ��ͨ��CO2������HY��Na2CO3���й�������ȷ����
��ֻ������HX��NaHCO3����NaY��Һ��ͨ��CO2������HY��Na2CO3���й�������ȷ����| A�����H����������Y�D>CO32�D>X�D>HCO3�D |
| B��������ǿ������HX>HY>H2CO3 |
C����Һ���ʵ���Ũ�� ��ͬʱ���ԣ�NaX>Na2CO3>NaY>NaHCO3 ��ͬʱ���ԣ�NaX>Na2CO3>NaY>NaHCO3 |
| D��NaX��Һ��ͨ������CO2�������Ũ�ȣ�c(X�D)��c(Na��)��c(HCO3�D)��c(OH�D) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��V1=10V2 | B��V1��10V2 | C��V1��10V2 | D��V2��10V1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A������Һ��pHһ����9 | B������ҺpHһ��Ϊ5 |
| C������Һ��pH������9��5 | D����������������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ��B. H2O2 ���� C. Cl2ˮ ���� D. HNO3
��B. H2O2 ���� C. Cl2ˮ ���� D. HNO3  ___��
___�� ͨ������ȷ����������________������С������С�����
ͨ������ȷ����������________������С������С������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com