
【题目】红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的ΔH表示生成1 mol产物的数据)。
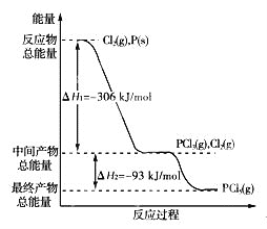
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是________________________________________;
(2)PCl5分解成PCl3和Cl2的热化学方程式是_________________________。
(3)P和Cl2分两步反应生成1 mol PCl5的反应热ΔH3= ___________,P和Cl2一步反应生成1 mol PCl5的ΔH4 ____________ΔH3(填“大于”、“小于”或“等于”);
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是____________________。
【答案】3/2Cl2(g)+P(s)===PCl3(g) ΔH=-306 kJ/mol PCl5(g)===PCl3(g)+Cl2(g) ΔH=+93 kJ/mol -399 kJ/mol 等于 PCl5+4H2O===H3PO4+5HCl
【解析】
根据反应过程与能量的关系图写出热化学方程式以及利用盖斯定律求反应热。
(1)P和Cl2反应生成PCl3的热化学方程式,根据图象,生成气态的PCl3,△H=-306kJ·mol-1。P为固体,Cl2为气体,则热化学方程式为![]() ;
;
(2)从图象来看,PCl3(g)和Cl2(g)生成PCl5(g),△H=-93kJ·mol-1。现在要求PCl5(g)分解成PCl3(g)和Cl2(g),△H应为+93kJ·mol-1。则热化学方程式为PCl5(g)=PCl3(g)+Cl2(g) ΔH=+93 kJ/mol;
(3)P和Cl2分两步反应生成1 mol PCl5的反应热,从图象来看,ΔH3=ΔH1+ΔH2=-306 kJ/mol+(-93 kJ/mol)=-399 kJ/mol。化学反应热△H只和反应物、生成物的能量有关,与反应路径无关,只要反应物和生成物一样,不管是经过一步还是二步反应,反应热相同,因此ΔH4 等于ΔH3。
(4) PCl5与足量水充分反应,最终生成两种酸,为水解反应,P和Cl的化合价都不变,P为+5价,得到的酸为磷酸,Cl为-1价,得到的酸为HCl。方程式为PCl5+4H2O=H3PO4+5HCl。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】在水中加入等物质的量的 Ag+、Ba2+、Na+、SO42-、NO3-、Cl-。该溶液放在用惰性材料做电极的电解槽中,通电片刻,则氧化产物与还原产物的质量为 ( )
A. 35.5∶10.8B. 16∶207C. 8∶1D. 108∶35.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语的表示方法中正确的是
A. ![]()
B. M2+离子核外有a个电子,b个中子,M原子符号为![]()
C. 用电子式表示MgCl2的形成过程为![]()
D. 次氯酸的电子式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿(主要成分是Cu2S)含铜量高,是最重要的炼铜矿石。请回答下列问题:
Ⅰ.已知:①2Cu2S(s)+3O2(g) ![]() 2Cu2O(s)+2SO2(g) ΔH=768.2kJ·mol1
2Cu2O(s)+2SO2(g) ΔH=768.2kJ·mol1
②Cu2S(s)+O2(g)![]() 2Cu(s)+SO2(g) ΔH=217.4 kJ·mol1
2Cu(s)+SO2(g) ΔH=217.4 kJ·mol1
(1)Cu2S与Cu2O反应生成Cu和SO2的热化学方程式为____________,该反应中Cu2O作_________(填“氧化剂”或“还原剂”)。
Ⅱ.Cu2O可催化二甲醚合成乙醇。
反应①:CH3OCH3(g)+CO(g)![]() CH3COOCH3(g) ΔH1
CH3COOCH3(g) ΔH1
反应②:CH3COOCH3(g)+2H2(g)![]() CH3OH(g)+C2H5OH(g) ΔH2
CH3OH(g)+C2H5OH(g) ΔH2
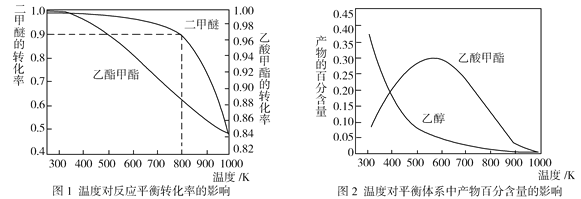
(2)压强为p kPa时,同一体系中发生反应①和反应②,温度对二甲醚(CH3OCH3)和乙酸甲酯(CH3COOCH3)平衡转化率的影响如图1所示,则ΔH1______0(填“>”或“<”,下同)、ΔH2______0。温度对平衡体系中乙酸甲酯的百分含量和乙醇的百分含量的影响如图2所示。在300~600 K范围内,乙酸甲酯的百分含量逐渐增大,而乙醇的百分含量逐渐减小的原因是____________。
(3)若压强为p kPa、温度为800 K时,向2 L恒容密闭容器中充入1 mol CH3OCH3和1 mol CO发生反应①,2min时达到平衡,则前2min内CH3COOCH3的平均生成速率为_________,该条件下平衡常数K=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次增大,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层龟子数是次外层电子数的3倍。
(1)试推断它们各是什么元素? 按要求写出合适的化学用语:A的元素符号:______,C单质的电子式:_________________,用电子式表示D的简单氢化物的形成过程________。
(2)甲、乙、丙、丁是由以上四种元素中的几种组成的10 电子微粒;
①甲为分子,且为天然气的主要成分,则甲的化学式为______
②乙为气体,且遇到无色酚酞溶液变成红色,则乙的电子式为_______
③丙为阳离子,丁为阴离子,且丙和丁在加热条件下生成的两种物质也是10电子微粒,请写出该反应的离子方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.实验室应将钠保存在煤油中B.分液漏斗和容量瓶在使用前都要检漏
C.液氯不可以储存在钢瓶中D.金属钠失火不可用水来灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 |
|
|
|
|
部分实验现象 | a极质量减小 b极质量增加 | b极有气体产生 c极无变化 | d极溶解 c极有气体产生 | 电流计指示在导线中 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是
A a>b>c>d B b>c>d>a C d>a>b>c D a>b>d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某儿童微量元素体检报告单的部分数据:
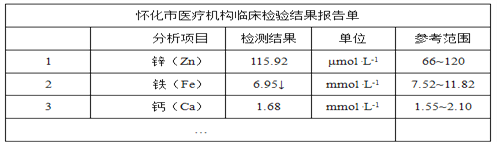
根据上表的数据,回答下列问题:
(1)该儿童__元素含量偏低。
(2)报告单中“μmol·L-1”是__(填“质量” “体积”或“浓度”)的单位。
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C表现出__________(填“氧化性”或“还原性”)。
(4)硫酸亚铁晶体(FeSO47H2O)在医疗上可作补血剂。某课外小组测定该补血剂(每片b克)中铁元素的含量。实验步骤如图:
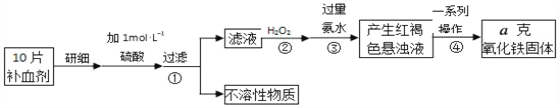
请回答下列问题:
a.②中H2O2的作用是__。
b.④中一系列处理的操作步骤为过滤、______、灼烧、冷却、称量。
c. 下列操作会导致所测定的铁元素含量偏高的是__。
A.步骤③所加氨水量不足 B.步骤④洗涤不充分 C.步骤④灼烧不充分
d. 写出步骤③中发生的离子方程式_____________________________________
e、简述滤液中存在Fe3+的检验方法是:_______________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com