
����Ŀ���������������������ܽ�Ȳ�ͬ����˿���������һ���ʣ�������Һ��pH���ﵽ����������ӵ�Ŀ�ġ����ܽ��������������ڲ�ͬpH�µ��ܽ��(S/mol/L)��ͼ��ʾ��

��1����pH��3ʱ����Һ��ͭԪ�ص���Ҫ������ʽ��__________��
��2����Ҫ��ȥCuCl2��Һ�е�����Fe3����Ӧ�ÿ�����Һ��pHֵΪ______ (�����)��
A����1����B��4���ҡ� C��8��PH��6 D����9
��3����Ni(NO3)2��Һ�к���������Co2�����ʣ�________(������������������)ͨ��������ҺpH�ķ�������ȥ��������_____________________________________________��
��4����֪һЩ���ܵ���ʵ��ܶȻ����������±���
���� | FeS | MnS | PbS | HgS | ZnS | CuS |
Ksp | 6.3��10��18 | 2.5��10��13 | 3.4��10��28 | 6.4��10��33 | 1.6��10��24 | 1.3��10��35 |
Ϊ��ȥij��ҵ��ˮ�к��е�Cu2����Pb2����Hg2�����ʣ���������˹�ҵ��ˮ�м��������___________(�����)��
A��NaOH�� ��B��FeS���� ��C��Na2S D��NH4Cl
���𰸡� Cu2�� B ���� Co2����Ni2���������ӳ���ʱ��pH��Χ���ƻ����̫С B
����������1��ͼ�п���pH��3��ʱ��Cu2+��δ����������ͭԪ�ص���Ҫ������ʽ��Cu2+��
��2����Ҫ��ȥCuCl2��Һ�е�����Fe3����Ӧ�ÿ�����Һ��pHʹ��������ȫ������ͬʱ��������Һ�е�ͭ���ӡ�����ѡ��ΪB��
��3����Ni(NO3)2��Һ�к���������Co2�����ʣ�����ͨ��������ҺpH�ķ�������ȥ����Ϊ��ͼ�п����жϳ�����Ni2+��Co2+�й�ͬ������pH��Χ�������pH��Χ���������ӻ�ͬʱ����Һ�����������������롣
��4��������Ŀ���������ܵ���ʵ��ܶȻ���������Щ�������Ksp������FeS������������ˮ�м��������FeS����������ת����Ӧ���پ����˽����ʳ�ȥ���������ʶ�������ˮ�������ĸ�����Ҳ�����ʡ�����ѡ��B��ȷ��


 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(��6��)������(Si3N4)��һ�������մɲ��ϣ�������ʯӢ�뽹̿�ڸ��µĵ������У�ͨ�����·�Ӧ�Ƶã�3SiO2(s)+6C(s)+ 2N2(g)![]() Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
��1���÷�Ӧ���������� ��2molN2�μӷ�Ӧת�Ƶ�����Ϊ ��
��2���ﵽƽ��ı�ijһ������������ı�N2��CO����������Ӧ����v��ʱ��t�Ĺ�ϵ��ͼ��

ͼ��t4ʱ����ƽ���ƶ������������� ��ͼ�б�ʾƽ��������CO�ĺ�����ߵ�һ��ʱ���� ��
��3�����÷�Ӧ��ƽ�ⳣ��Ϊ K��729������ͬ�¶���1L�ܱ������У�������SiO2��C��2mol N2��ַ�Ӧ����N2��ת������
(��ʾ��272 = 729)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪298Kʱ������Ӧ���й����ݣ�C��s��+ ![]() O2��g��=CO��g����H1=-110.5kJmol-1��C��s��+O2��g��=CO2��g����H2=-393.5kJmol-1����C��s��+CO2��g��=2CO��g���ġ�HΪ�� ��
O2��g��=CO��g����H1=-110.5kJmol-1��C��s��+O2��g��=CO2��g����H2=-393.5kJmol-1����C��s��+CO2��g��=2CO��g���ġ�HΪ�� ��
A. +283.0kJ/mol B. +172.5 kJ/mol C. -172.5 kJ/mol D. -504 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ȼ�ϵ����CsHSO4����Ϊ����ʴ���H+��������ṹ����ͼ������ܷ�Ӧ�ɱ�ʾΪ2H2+O2==2H2O�������й�˵����ȷ��������

A. ����ͨ�����·��b������a��
B. b���ϵĵ缫��ӦʽΪ��O2��2H2O��4e-��4OH-
C. ÿת��0.1 mol���ӣ�������1.12 ����H2
D. H+��a��ͨ�����������ʴ��ݵ�b��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��R��M��ԭ������������������ֻ��R���ڽ���Ԫ�أ���X��Y��R�����һ�ֻ�����Q����298Kʱ��0.1mol��L��1 Q��Һ��AG(���)��lg![]() ����12����X��M��ɵĻ�����XM��ǿ����ʡ�����˵����ȷ����
����12����X��M��ɵĻ�����XM��ǿ����ʡ�����˵����ȷ����
A. Y��R��M����Ԫ���γɵļ����Ӱ뾶��r(M)>r(R)>r(Y)
B. M���������Ӧ��ˮ����һ����ǿ��
C. R�ֱ���X��Y��M��ɵĶ�Ԫ�������ж��������Ӽ�
D. ������RYX��RMY��������ˮ�ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ�������������0.100molCO�����0.080molCuO���壬800��ʱ�������·�Ӧ��2CuO��s��+CO��g��![]() Cu2O��s��+CO2��g����n��CuO����ʱ��ı仯�����
Cu2O��s��+CO2��g����n��CuO����ʱ��ı仯�����
ʱ����min�� | 0 | 1 | 2 | 3 | 4 | 5 |
n��CuO����mol�� | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
��1����CO��ʾǰ2min�ڵĻ�ѧ��Ӧ����=
��2������˷�Ӧ��800Cʱ�Ļ�ѧƽ�ⳣ��k=
��3������ƽ������ϵ�м���CO��CO2��0.05mol�����ʱV������ V������
��4��������ԭCuO��CO������C��ˮ������Ӧ�Ƶá�
��֪��![]() H=-393.5kJ/mol
H=-393.5kJ/mol
![]() H=-566kJ/mol
H=-566kJ/mol
![]() H=-571.6kJ/mol
H=-571.6kJ/mol
��C��s��+H2O��g��![]() CO��g��+H2��g�� H= ��
CO��g��+H2��g�� H= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У�������ʵ��Ļ�ԭ��������ɵ���
A. KI��I2 B. FeCl2�� FeCl3 C. CuO ��Cu D. CO2�� Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���һ��2L���ܱ������У�����4 mol A��2 mol B�������·�Ӧ��3A(g����2B(g��![]() 4C(s����D(g������Ӧ2 min��ﵽƽ�⣬�������1��6 mol C������˵����ȷ����( ��
4C(s����D(g������Ӧ2 min��ﵽƽ�⣬�������1��6 mol C������˵����ȷ����( ��
A. ǰ2 min��D��ƽ����Ӧ����Ϊ0.2 mol��(L��min��
B. ��ʱ��B��ƽ��ת������40��
C. �������ϵ��ѹǿ��ƽ�ⲻ�ƶ�
D. ����B��ƽ�������ƶ���B��ƽ��ת��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ͭ����ȼ�ϵ�أ���ͼ�������ߡ��ɱ������õ��ͨ��һ�ָ��ӵ�ͭ��ʴ���������������������зŵ����Ϊ��2Li��Cu2O��H2O��2Cu��2Li+��2OH-������˵���������
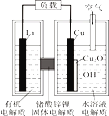
A. ������Ӧ�����У�������ΪO2
B. �ŵ�ʱ�������ĵ缫��ӦʽΪ��Cu2O��H2O��2e-��2Cu��2OH-
C. �ŵ�ʱ������·��ͨ��0.1 mol���ӵĵ���ʱ����0.1 mol Li+������������Cu���ƶ����б�״����1.12 L�������뷴Ӧ
D. ͨ����ʱ��ͭ����ʴ���������Cu2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com