
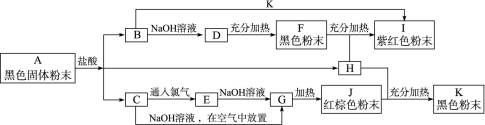
科目:高中化学 来源:不详 题型:填空题
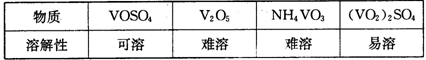
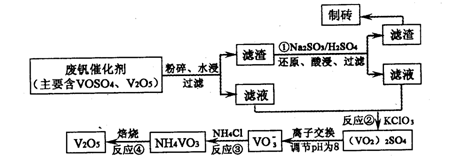
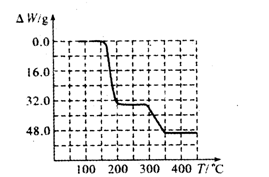
| A.先分解失去H2O,再分解失去NH3 | B.先分解失去NH3,再分解失去H2O |
| C.同时分解失去H2O和NH3 | D.同时分解失去H2、N2和H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.研究物质的性质时,常用到观察、实验、分类、比较等方法 |
| B.制陶、冶金、酿酒等生产过程中,肯定发生了化学反应 |
| C.1869年俄国化学家门捷列夫提出了原子学说,为近代化学的发展奠定了基础 |
| D.我国化学家在1965年第一次人工合成了具有生命活性的蛋白质,为世界生命科学的研究和发展作出了贡献 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
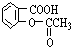 若将阿司匹灵溶于过量的氢氧化钠溶液,其反应的化学方程式为:_________________________
若将阿司匹灵溶于过量的氢氧化钠溶液,其反应的化学方程式为:_________________________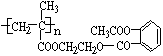

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
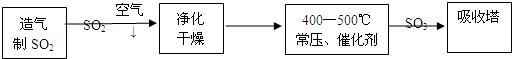
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.+6 | B.+4 | C.+3 | D.+2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
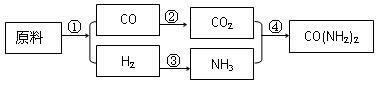
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com