
| ��ѧ�� | ���ܣ�kJ/mol�� | ��ѧ�� | ���ܣ�kJ/mol�� |
| N��N | 942 | H��O | 460 |
| N��H | 391 | O��O | 499 |
| H��H | 437 | | |
 2NH3 ��H��a kJ��mol��1���Ը��ݱ������м������ݹ���a����ֵ �� ��
2NH3 ��H��a kJ��mol��1���Ը��ݱ������м������ݹ���a����ֵ �� �� �������Ͽ��㱾ϵ�д�
�������Ͽ��㱾ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������44kJ | B������2.44KJ |
| C������44kJ | D������2.44KJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����������������Һ����кͷ�Ӧ | B���Ҵ���ȼ�� |
| C��̼������ȷֽ� | D�����������ᷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����Ƿ��ȷ�Ӧ�������ӵķ�Ӧ�������Է����� |
| B������ͬһ�����ڲ�ͬ״̬ʱ����ֵ�ǣ���̬>Һ̬>��̬ |
| C��ƽ�ⳣ��KֵԽ������淴Ӧ����Խ��ȫ����Ӧ���ת����ҲԽ�� |
| D�����������ﵽ��ܵķ��ӷ�������ײ��Ϊ��Ч��ײ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na+(g)+Cl��(g) | B��Na(s)+ Cl2(g) Cl2(g) |
| C��Na(s) | D��Na(g)��e�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Pa�£�ʯī�����ʯȼ�յĻ�ѧ����ʽ�ֱ�Ϊ��C(ʯī) + O2(g) = CO2(g)��1 moL C(ʯī) ��ȫȼ�շ���393.51 kJ��C(���ʯ) + O2(g) = CO2(g)��1 moL C(���ʯ) ��ȫȼ�շ��� 395.41 kJ���ݴ��������õ������н����У���ȷ���ǣ� ����
Pa�£�ʯī�����ʯȼ�յĻ�ѧ����ʽ�ֱ�Ϊ��C(ʯī) + O2(g) = CO2(g)��1 moL C(ʯī) ��ȫȼ�շ���393.51 kJ��C(���ʯ) + O2(g) = CO2(g)��1 moL C(���ʯ) ��ȫȼ�շ��� 395.41 kJ���ݴ��������õ������н����У���ȷ���ǣ� ����| A�����ʯ��ʯī�ȶ� | B����ʯī�Ʊ����ʯһ�������ȷ�Ӧ |
| C��ʯī�������Ƚ��ʯ�������� | D��ʯīת��Ϊ���ʯ�������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ȼúΪ���ġ��������硱�ǽ���ѧ��ֱ��ת��Ϊ���� |
| B��ȼ�ϵ�ص�����ת���ʿ��Դﵽ100% |
| C����س���ǽ�����ת��Ϊ��ѧ�ܵĹ��� |
| D��������������ȼ�գ���ѧ��ȫ��ת��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
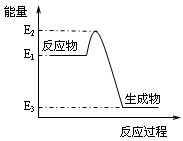
| A���÷�Ӧ�����ȷ�Ӧ |
| B���÷�Ӧ��������ȷ�Ӧ���ȶ� |
| C���÷�Ӧһ��������Ƴ�Ϊԭ��� |
| D���÷�Ӧ�����ų�������ΪE2-E3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��һ������92.0 kJ | B��һ������92.0 kJ | C��һ��С��92.0 kJ | D������ȷ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com