
【题目】钛矿工业中的硫酸酸性废水富含Ti、Fe等元素,其综合利用如下:
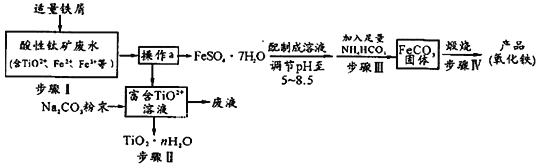
已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)TiO2+钛的化合价为________________。
(2)步骤Ⅰ中加入铁屑的作用是________________________。(以离子方程式表示)
(3)操作a是_________ 、__________、过滤、洗涤、干燥 。
(4)步骤Ⅲ中发生反应的化学方程式为________________________;反应温度一般需控制在35℃以下,其目的是____________________________________。
(5)已知Ksp=[Fe(OH)2] = 8×10-16。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5,所得的FeCO3中没有Fe(OH)2。则溶液中c(Fe2+)小于________ mol/L。步骤Ⅳ中,为了得到较为纯净的Fe2O3,除了适当的温度外,还需要采取的措施是___________。
(6)向“富含TiO2+溶液”中加入Na2CO3粉末易得到固体TiO2 nH2O。请结合平衡移动原理和化学用语解释其原因_________________________________。
【答案】+4 Fe + 2Fe3+ = 3Fe2+ 蒸发浓缩 冷却结晶 FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+H2O+CO2↑ 避免温度过高碳酸氢铵分解,减少Fe2+的水解或氧化 8×10-5 向反应容器中补充适量的空气 溶液中存在水解平衡TiO2++(n+1)H2OTiO2nH2O+2H+,加入的Na2CO3粉末与H+反应,降低了溶液中c(H+),促进水解平衡向生成TiO2nH2O的方向移动
【解析】
钛矿工业中的酸性废水富含Ti、Fe等元素,含有TiO2+、Fe2+、Fe3+等离子,加入铁粉还原铁离子得到亚铁离子,通过蒸发浓缩、冷却结晶过滤洗涤、干燥得到硫酸亚铁晶体,配制成溶液调节溶液PH5-5.8范围内,加入足量碳酸氢铵,过滤得到碳酸亚铁沉淀,在坩埚中灼烧得到氧化铁,过滤后得到富含的TiO2+溶液,加入Na2CO3粉末与H+反应,降低了溶液中c(H+),使平衡TiO2++(n+1)H2O![]() TiO2·n H2O+2H+向生成TiO2·n H2O的方向移动,可得到TiO2粗产品。
TiO2·n H2O+2H+向生成TiO2·n H2O的方向移动,可得到TiO2粗产品。
(1)离子中各元素化合价代数和等于离子所带电荷数,元素为-2价,则TiO2+钛的化合价为+4价。
(2)加入铁粉,首先发生Fe+2Fe3+=3Fe2+,其次发生Fe+2H+=Fe2++H2;
(3)操作a是溶液中得到溶质固体,方法是蒸发浓缩、冷却结晶过滤洗涤、干燥;
(4)步骤Ⅲ中发生反应是硫酸亚铁和碳酸氢铵反应生成碳酸亚铁沉淀、硫酸铵、二氧化碳和水,反应的化学方程式为:FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+H2O+CO2↑,反应温度一般需控制在35℃以下,是为了避免温度过高碳酸氢铵分解,减少铁离子的水解程度;
(5)室温下测得溶液的pH为8.5,c(OH-)=10-14/10-8.5=1×10-5.5,由题中数据可知,溶液中c(Fe2+)·c(OH-)2=1×10-6×(1×10-5.5)2=1×10-17<Ksp[Fe(OH)2]=8×10-16,故无Fe(OH)2沉淀生成;
(6)富含的TiO2+溶液,加入Na2CO3粉末与H+反应,降低了溶液中c(H+),使平衡TiO2++(n+1)H2OTiO2nH2O+2H+向生成TiO2·n H2O的方向移动,可得到TiO2粗产品.


科目:高中化学 来源: 题型:
【题目】下列溶液中溶质的物质的量浓度为1mol·L-1的是( )
A.将0.1mol胆矾固体溶于100mL水中
B.将22.4LHCl气体溶于水配成1L溶液
C.将1L10mol·L-1的浓盐酸与9L水混合
D.10gNaOH固体溶解在水中配成250mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,部分物质的电离常数如表所示:
化学式 | CH3COOH | H2CO3 |
电离常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 |
请回答下列问题:
(1)相同pH的CH3COONa、NaHCO3、Na2CO3浓度由大到小的顺序为__________
(2)常温下0.1mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填字母,下同)。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-) D.c(H+)/c(OH-)
(3)现有10mLpH=2的盐酸溶液,进行以下操作:
a.与pH=5的盐酸等体积混合,则pH=_____________;
b.向该盐酸溶液中加入10mL0.02mol/LCH3COONa溶液,则该混合溶液中存在的物料守恒式为__________________;
c.向该盐酸溶液中加入等体积等浓度的Na2CO3溶液,则混合溶液中存在的电荷守恒式为_______________________;
d. 下列关于体积都为10mL,pH=2的A(盐酸)和B(CH3COOH)溶液说法正确的是_____ (填写序号)。
①与等量的锌反应开始反应时的速率A=B
②与等量的锌反应(锌完全溶解,没有剩余)所需要的时间A>B
③加水稀释100倍,pH大小比较:4=A>B>2
④物质的量浓度大小比较:A>B
⑤分别与10mLpH=12的NaOH溶液充分反应后的溶液pH大小比较:A<B
e. 现用标准HCl溶液滴定氨水,应选用________指示剂,下列操作会导致测定结果偏高的是___。
A.未用HCl标准溶液润洗滴定管
B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.观察读数时,滴定前仰视,滴定后俯视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是
A. 原子半径:Na>Mg>O
B. 13C和14C属于同位素
C. 0族元素是同周期中非金属性最强的元素
D. N和P属于第ⅤA族元素,HNO3酸性比H3PO4的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.1mol H2O的质量为18g/mol
B.40gNaOH溶解在1L水中,形成溶液溶质的物质的量浓度为1mol/L
C.3.01×1023个SO2分子质量为32 g
D.标准状况下,1mol任何物质体积均为22.4L/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X____。
(2)上述实验流程中①②③步均要进行的实验操作是____(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是____________。
(4)按此实验方案得到的溶液3中肯定含有杂质。为了解决这个问题,可以向溶液3中加入适量的________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 1molH2和1molI2在加热条件下充分反应,生成HI的分子数为2NA
B. 10g质量分数为46%的乙醇溶液含有的氢原子数目为0.6NA
C. 20mL0.1 mol/LAlCl3溶液中,水解形成Al(OH)3胶体粒子数为0.002NA
D. 0.1molNa2O2和Na2O的混合物中含有的离子总数等于0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是

A. X、Y、Z三种元素最低价氢化物的沸点依次升高
B. 由X、Y和氢三种元素形成的化合物中只有共价键
C. T的氢化物的沸点一定高于同主族元素形成的其他氢化物
D. T元素单质具有半导体的特性,T与Z元素可形成化合物TZ4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com