
����Ŀ��(NH4)2SO4�dz����Ļ��ʺͻ���ԭ�ϣ������ֽ⡣ij��ȤС����̽����ֽ���
[��������](NH4)2SO4��260���400��ʱ�ֽ���ﲻͬ��
[ʵ��̽��]��С����ѡ����ͼ��ʾװ�ý���ʵ�飨�гֺͼ���װ���ԣ�
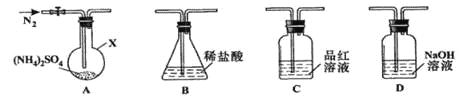
ʵ��1������װ��A-B-C-D����������ԣ���ͼʾ�����Լ���װ��Bʢ0.5000mol/L����70.00mL����ͨ��N2�ž���������260�����װ��Aһ��ʱ�䣬ֹͣ���ȣ���ȴ��ֹͣͨ��N2��Ʒ����Һ����ɫ��ȡ��װ��B������ָʾ������0.2000mol/L NaOH��Һ�ζ�ʣ�����ᣬ�յ�ʱ����NaOH��Һ25.00 mL��������ζ������Һ����SO42-��
��1������X��������________________��
��2���ζ�ǰ�����в�������ȷ˳����_________(����ĸ���)��
a��ʢװ0.2000mol/L NaOH��Һ
b����0.2000mol/L NaOH��Һ��ϴ
c����������¼
d����©����ϴ
e���ž��ζ��ܼ�������ݲ�����Һ��
��3��װ��B����Һ������������ʵ�����__________mol��
ʵ��2������װ��A-D-B����������ԣ���ͼʾ���¼����Լ���ͨ��N2�ž���������400�����װ��A��(NH4)2SO4��ȫ�ֽ������ֹͣ���ȣ���ȴ��ֹͣͨ��N2���۲쵽װ��A��D֮��ĵ���������������ɫ���塣�����飬�ð�ɫ�����װ��D����Һ����SO32-����SO42-����һ���о����֣�����������������
��4������װ��D����Һ����SO32-����SO42-��ʵ�������������__________��
��5��װ��B����Һ���յ�������____________��
��6��(NH4)2SO4��400��ֽ�Ļ�ѧ����ʽ��______________________��
���𰸡�Բ����ƿ dbaec 0.03 mol ȡ����װ��D����Һ���Թ��У��μ�BaCl2��Һ�����ɰ�ɫ��������������ϡ����������ȫ�ܽ⣬�ų���ɫ�̼������� NH3 3(NH4)2SO4![]() 4NH3��+ N2��+3SO2�� + 6H2O��
4NH3��+ N2��+3SO2�� + 6H2O��
��������
��1������XΪԲ����ƿ��
��2���ζ�ǰ���ȼ��ζ����Ƿ�©ˮ���ٽ�����ϴ��Ȼ���ñ�Һ��ϴ����ע���Һ���ž��ζ���������ݲ�����Һ�棬��������¼���ζ�ǰ����ɣ�
��3�����������������Ƽ���Bװ����ʣ���HCl���μӷ�Ӧ��HCl���շֽ����ɵ�NH3��������Ӧ��NH3+HCl=NH4Cl��������������NH3�����ʵ�����
��4��ȡD��Һ���Թ��У���������BaCl2��Һ���ټ������ᣬ��ɫ������ȫ�ܽ������ɴ̼�����ζ�����壬˵��D����Һ����SO32-����SO42-��
��5��װ��D����Һ����SO32-��˵���ֽ�����SO2��װ��A��D֮��ĵ���������������ɫ���壬��ɫ����Ӧ�Ƕ�����������ˮ�γɵ��Σ�װ��B����Һ���յ������ǰ�����
��6���ɣ�5���з�����֪����NH4��2SO4��400��ֽ�ʱ����NH3��SO2��H2O���ɣ�SԪ�ػ��ϼ۽��ͣ����ݵ���ת���غ㣬ֻ��ΪNԪ�ػ��ϼ����ߣ�����������������˵������N2����ƽ��д����ʽ��
��1�����������ṹ��֪����X��������Բ����ƿ��
��2���ζ��IJ�������Ϊ�����Ȳ�©��ˮϴ��Ȼ���ô�װ��Һ����ϴ����װ��Һ�����ž��ζ��ܼ�������ݲ��ҵ���Һ�棬�����������м�¼�������ȷ�IJ���˳����dbaec��
��3��Ʒ����Һû����ɫ��֤����SO2���ɣ�������ζ������Һ����SO2��4��֤��������Һ��û������SO3����װ��B�����յ�����ΪNH3����������к͵ζ���ԭ����n(HCl)��n(NH3)+n(NaOH)����n(NH3)��0.5mol/L��0.07L��0.2mol/L��0.025L��0.03mol��
��4�������ᱵ�������ᷴӦ����SO2�����ᱵ���������ᣬ�����װ��D����Һ����SO32������SO42����ʵ������������ǣ�ȡ����װ��D����Һ���Թ��У��μ�BaCl2��Һ�����ɰ�ɫ��������������ϡ����������ȫ�ܽ⣬�ų���ɫ�̼������壬֤��װ��D����Һ����SO2�� 3���� SO42����
��5��ʵ��2֤����(NH4)2SO4��400���ֽ�õ��IJ�������NH3��SO2���ܱ�װ��B�е�������Һ���յ�����ΪNH3��
��6��(NH4)2SO4��400���ֽ�õ��IJ�������NH3��SO2������������������������˸��ݵ�ʧ�����غ��֪��Ӧ�л��е������ɣ����Է�Ӧ�Ļ�ѧ����ʽΪ3(NH4)2SO4![]() 4NH3��+ N2��+3SO2�� + 6H2O����
4NH3��+ N2��+3SO2�� + 6H2O����


 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������100mL1.0 mol/L Na2SO4��Һ����ȷ�ķ�����( )
�ٽ�14.2 g Na2SO4������100mLˮ��
�ڽ�32.2g Na2SO410H2O��������ˮ�У�����ˮϡ����100 mL
�۽�20 mL 5.0 mol/L Na2SO4��Һ��ˮϡ����100 mL
A.�٢�B.�ڢ�C.�٢�D.�٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£�m g����A��n g����B�ķ�������ͬ������˵���в���ȷ����
A. ��������A��B����Է�������֮��Ϊm��n
B. ͬ��������A��B�ķ�����֮��Ϊn��m
C. ͬ��ͬѹ�£�A��B��������ܶ�֮��Ϊn��m
D. ��ͬ״���£�ͬ���A��B�����������֮��Ϊm��n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڸ�ʵ��װ��ͼ����������ȷ����
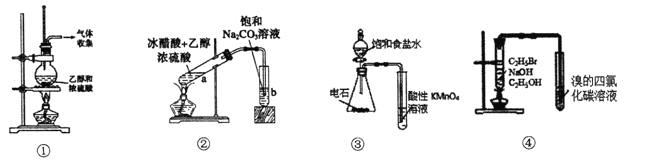
A. װ�â٣�ʵ������ȡ��ϩ
B. װ�âڣ�ʵ������ȡ��������
C. װ�âۣ���֤��Ȳ�Ļ�ԭ��
D. װ�âܣ���֤�����鷢����ȥ��Ӧ������ϩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�IJ����У��е���ͬ���칹�壬�е�û��ͬ���칹�壬����һ��������ͬ���칹��ķ�Ӧ��
A. �����ϩ(![]() )������ʵ�����Br2�ӳ�
)������ʵ�����Br2�ӳ�
B. 2-�ȱ�����NaOH���Ҵ���Һ���ȷ�����ȥ��Ӧ
C. �ױ���һ�������·���������Ӧ����һ�����ױ�
D. ��Ȳ���������Ȼ�����һ���������ɶ��ȴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�������A�����ϣ���������̼����������Ϊ70.59%�������������Ϊ 5.88%������Ϊ�����������з����ⶨ���л����������Է��������ͷ��ӽṹ��A������ͼ���˴Ź������ס��������ͼ�ֱ��ʾ���£�
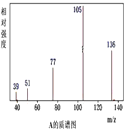
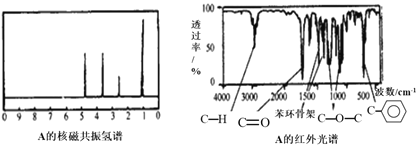
��ش��������⣺
��1��A��ʵ��ʽΪ__________��
��2��A�Ľṹ��ʽΪ__________��
��3��������������һ���л���____________��
��4��1molA��һ�������¿���___________molH2�����ӳɷ�Ӧ��
��5��A�ж���ͬ���칹�壬ͬʱ��������������ͬ���칹��M��______�֡������ڷ����廯������������ࣻ�۷��ӽṹ�к���һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������M�Ƕ�����Ȳ��Һ�����ϵ�һ�֣���Ķ�����Ȳ�������![]() ���Ի�Ϊͬϵ��ĵ�ȡ������A��GΪԭ�Ϻϳ�M��һ��·�ߣ����ַ�Ӧ������ȥ�����£�
���Ի�Ϊͬϵ��ĵ�ȡ������A��GΪԭ�Ϻϳ�M��һ��·�ߣ����ַ�Ӧ������ȥ�����£�

�ش��������⣺
��1��A�ķ���ʽΪ________��
��2��D�к��еĹ�������________�������������________��̼ԭ�ӹ�ƽ�棻
��3���ٵķ�Ӧ������________���۵ķ�Ӧ������________��
��4���ݵĻ�ѧ����ʽΪ________��
��5��B��ͬ���칹������ͬʱ��������������a��������������ȡ������b���ܷ���������Ӧ������______�֣������������칹�������к˴Ź�������Ϊ5��壬�ҷ������Ϊ6��2��2��1��1����________��д�ṹ��ʽ����
��6�����������ϳ�·�ߣ����һ���ɱ���ϩ�ͼױ�Ϊ��ʼԭ���Ʊ�![]() �ĺϳ�·�ߣ�___���������Լ����ã�(�ϳ�·�߳��õı�ʾ��������ʼԭ��A
�ĺϳ�·�ߣ�___���������Լ����ã�(�ϳ�·�߳��õı�ʾ��������ʼԭ��A![]() B����
B����![]() Ŀ�����)��
Ŀ�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С��Ϊ��̽��һ����������X(��������Ԫ��)����ɺ����ʣ���Ʋ��������ʵ�飺

��ȡ10.80gX�ڶ��������м�������ȫ�ֽ⣬�õ�6.40g����1.��ش��������⣺
��1��������ɫ����1�н���Ԫ�ص�ԭ�ӽṹʾ��ͼ_______��д������ĵ���ʽ_______��
��2��X�Ļ�ѧʽ��______���ڶ��������м���X����ȫ�ֽ�Ļ�ѧ��Ӧ����ʽΪ_______��
��3����ɫ����2�ڿ����б�ɺ��ɫ������ԭ����_______(�û�ѧ��Ӧ����ʽ��ʾ)��
��4��һ�������£�����������1�е�ij�ֳɷֿ��ܷ���������ԭ��Ӧ��д��һ�����ܵĻ�ѧ��Ӧ����ʽ_______�������ʵ�鷽����֤�÷�Ӧ�IJ���_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ���ڼӳɷ�Ӧ���ǣ� ��
A. CH3CH==CH2��Br2��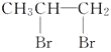
B. ![]() ��HNO3
��HNO3![]()
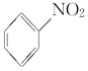 ��H2O
��H2O
C. 2CH3CH2OH��O2![]() 2CH3CHO��2H2O
2CH3CHO��2H2O
D. CH3COOH��CH3CH2OH![]() CH3COOCH2CH3��H2O
CH3COOCH2CH3��H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com