
| A. | 混合溶液pH>7 | |
| B. | 对混合溶液进行微热,K1增大、K2减小 | |
| C. | 调节混合溶液的pH至中性,则此时溶液中c(Na+)=c(CH3COO-) | |
| D. | 温度不变,若在混合溶液中加入少量NaOH固体,c(CH3COO-)减小 |
分析 A.根据题干知,醋酸电离程度大于醋酸根离子水解程度,所以常温下,等体积、等物质的量浓度的醋酸和醋酸钠溶液混合呈酸性;
B.弱电解质的电离和盐类水解都是吸热反应,升高温度促进醋酸电离、醋酸根离子水解;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
D.温度不变,在混合溶液中加入少量NaOH固体,OH-和H+反应促进醋酸电离.
解答 解:A.根据题干知,醋酸电离程度大于醋酸根离子水解程度,所以常温下,等体积、等物质的量浓度的醋酸和醋酸钠溶液混合后,溶液中存在c(OH-)<c(H+),呈酸性,所以混合溶液pH<7,故A错误;
B.醋酸电离和醋酸根离子水解都是吸热反应,升高温度促进醋酸电离、醋酸根离子水解,所以对混合溶液进行微热,K1增大、K2增大,故B错误;
C.溶液呈中性,则c(OH-)=c(H+),任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)═c(CH3COO-),故C正确;
D.温度不变,在混合溶液中加入少量NaOH固体,OH-和H+反应促进醋酸电离,则溶液中c(CH3COO-)增大,故D错误;
故选C.
点评 本题考查弱电解质电离,明确醋酸电离和醋酸根离子水解程度相对大小与溶液酸碱性关系是解本题关键,知道任何电解质溶液中都存在电荷守恒和物料守恒,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 酸 | 碱 | 盐 | 混合物 | |
| A | H2SO3 | 纯碱 | 明矾 | 盐酸 |
| B | HClO4 | 熟石灰 | 石灰石 | 液氯 |
| C | HI | 烧碱 | 小苏打 | 氯水 |
| D | NaHSO4 | 一水合氨 | 食盐 | 漂白粉 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含ClO-的溶液中:H+、K+、Br-、I- | |
| B. | pH=1的溶液中:NH4+、Ba2+、CO32-、NO3- | |
| C. | 在与Al反应能放出H2的溶液中:Mg2+、HCO3-、SO42-、Cl- | |
| D. | 在pH=10的溶液中:Na+、K+、CH3COO-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 浓硫酸能加快酯化反应速率 | B. | 不断蒸出酯,会降低其产率 | ||
| C. | 装置b比装置a原料损失的少 | D. | 可用分液的方法分离出乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用钠可以检验某无水酒精中是否含有水 | |
| B. | 除去甲烷中混有的少量乙烯,可以将混合气体通过酸性KMnO4溶液 | |
| C. | 制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入浓硫酸,最后加入乙酸 | |
| D. | 在蔗糖溶液中加入少量稀硫酸,水浴加热后,再加入少量新制的氢氧化铜悬浊液,加热至沸腾,没有砖红色沉淀生成,说明蔗糖没有水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 2 | D. | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
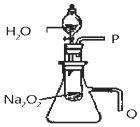 实验法是化学重要的研究物质性质的基本方法.某化学研究小组进行了如下实验,请回答问题.
实验法是化学重要的研究物质性质的基本方法.某化学研究小组进行了如下实验,请回答问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com