
1L某溶液中含有的离子如下表:
离子 | Cu2+ | Al3+ | NO3- | Cl- |
物质的量浓度(mol/L) | 1 | 1 | a | 1 |
用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是
A.电解后溶液呈酸性 B.a=3
C.阳极生成1.5molCl2 D.阴极析出的金属是铜与铝
科目:高中化学 来源:2017届海南省高三上10月月考化学试卷(解析版) 题型:实验题
某化学小组采用类似制乙酸乙酯的装置(图1),用环己醇制备环己烯:

已知: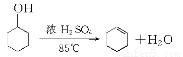
密度(g· cm-3) | 熔点(℃) | 沸点℃ | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品:将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是__________________。
②试管C置于冰水浴中的目的是___________________。
(2)制备精品:
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在________层(填“上”或“下”),分液后用____________(填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图2装置蒸馏,冷却水从________口进入。蒸馏时加入生石灰,目的是__________。
③收集产品时,控制的温度应在__________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是___________(填选项符号)
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是____________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:填空题
己知某溶液中只存在OH-、H+、NH4+、CL-四种离子,某同学推测其离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(NH4+)>c(OH-)>c(Cl-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
⑴若溶液中只有一种溶质,则该溶质是_________________。
⑵若四种离子的关系符合③,则溶质为___________;若四种离子的关系符合④,则溶质为________。
⑶将pH相同的NH4Cl溶液稀释相同的倍数,下面图像正确的是(填图像序号)______________。
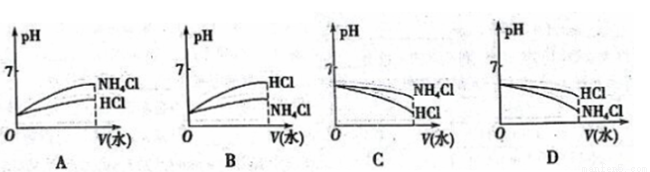
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:选择题
在恒温恒容的密闭容器中可逆反应2NO2(g) 2NO(g)+O2(g),达到平衡状态的标志是
2NO(g)+O2(g),达到平衡状态的标志是
①单位时间内生成n molO2的同时生成2n mol NO2
②单位时间内生成n molO2的同时生成2n mol NO
③混合气体的颜色不再改变的状态
④用NO2、NO、O2表示的反应速率的比为2:2:1的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
⑧2V正(NO2)=2V逆(O2)
A.①③⑥⑦ B.②⑤⑥⑦ C.①③④⑤⑧ D.①②③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上月考二化学卷(解析版) 题型:填空题
常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
实验编号 | HA物质的量浓度/ | NaOH物质的量浓度/ | 混合后溶液的pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.12 | 0.1 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?____________.
(2)乙组混合溶液中粒子浓度c(A-)和c(Na+)的大小关系____________.
A.前者大 B.后者大 C.两者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是____________.
(4)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=_________mol•L-1.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上月考二化学卷(解析版) 题型:选择题
某酸的酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度,有关叙述正确的是
A.H2Y在电离时:H2Y+H2O HY-+H3O+
HY-+H3O+
B.在该盐的溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C.在该盐的溶液中,离子浓度为:c(Na+)>c(HY-)>c(Y2-)>c(OH-)>c(H+)
D.HY-水解方程式为:HY-+H2O Y2-+H3O+
Y2-+H3O+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上月考二化学卷(解析版) 题型:选择题
在体积均为1.0L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 CO2和0.2molCO2,在不同温度下反应CO2(g)+c(s) 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
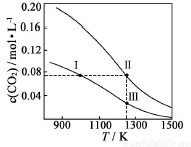
A.反应CO2(g)+c(s) 2CO(g) △S>0、△H<0
2CO(g) △S>0、△H<0
B.体系的总压强P总:P总(状态Ⅱ)>2P总(状态Ⅰ)
C.体系中c(CO):c(CO,状态Ⅱ)>2c(CO,状态Ⅲ)
D.逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
下列溶液中粒子的物质的量浓度关系正确的是
A.0.1mol·L-1NaHCO3溶液与0.1 mol·L-1NaOH溶液等体积混合,所得溶液中:
c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
B.20mL0.1 mol·L-1CH3COONa溶液与10mL0.1 mol·L-1HCl溶液混合后呈酸性,所得溶液中:
c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:
c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.0.1 mol·L-1CH3COOH溶液与0.1 mol·L-1NaOH溶液等体积混合,所得溶液中:
c(OH-)>c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
一定温度下,水存在H 2 O H++OH- ΔH=Q(Q>0)的平衡,下列叙述一定正确的是
H++OH- ΔH=Q(Q>0)的平衡,下列叙述一定正确的是
A.向水中滴入少量稀盐酸,平衡逆向移动,Kw 减小
B.将水加热,Kw 增大,pH增大
C.向水中加入少量固体HCl气体,平衡逆向移动,c(H+ )降低
D.向水中加入少量固体硫酸钠,c(H+ )和Kw 均不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com