
| A、品红溶液 | B、酸性高锰酸钾溶液 |
| C、澄清石灰水 | D、溴水 |
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
A、 用装置来做SO2的喷泉实验 |
B、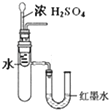 用装置来验证浓H2SO4与水混合的热量变化 |
C、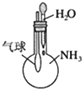 用装置来验证NH3易溶于水 |
D、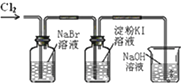 用装置来验证氧化性:Cl2>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、X均为中学化学常见物质,一定条件下它们有如图转化关系(其他产物已略去),回答下列问题:
A、B、C、X均为中学化学常见物质,一定条件下它们有如图转化关系(其他产物已略去),回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 物质A~D为CH3COOH、NaOH、HCl、NH3?H2O中的各一种,常温下将各种物质的溶液从1mL稀释到1000mL,pH 的变化关系如图所示,请回答下列问题:
物质A~D为CH3COOH、NaOH、HCl、NH3?H2O中的各一种,常温下将各种物质的溶液从1mL稀释到1000mL,pH 的变化关系如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、因铝对人体有害,故不能使用铝锅等炊具 |
| B、一种治疗胃酸过多的药物的主要成分为Al(OH)3,该药应禁止使用 |
| C、膨化食品中的铝元素超标可能是发酵剂明矾造成的 |
| D、用铝箔包装的茶叶不能食用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、I-、CO32-、SO42- |
| B、Fe2+、H+、K+、NO3- |
| C、Mg2+、Na+、SCN-、Cl- |
| D、Cu2+、Ba2+、Na+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:


 (g)
(g)| FeSO4/Al2O3 |
| 高温 |
 (g)+)+3H2(g)
(g)+)+3H2(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三氯化铁溶液中加入铁粉2Fe3++Fe=3Fe2+ |
| B、Ba(OH)2溶液和稀H2SO4的反应H++OH-=H2O |
| C、过量氯气通入氯化亚铁溶液中2Fe2++Cl2=2Fe3++2Cl- |
| D、氢氧化镁溶于稀硫酸中Mg(OH)2+2H+=Mg2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、燃烧产物中硫元素都是SO2 |
| B、燃烧产物中的SO2和S的物质的量之比为5:3 |
| C、燃烧产物中硫元素都是S |
| D、燃烧产物中的SO2和S的物质的量之比为1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com