
| A、混合气体一定没有甲烷 |
| B、混合气体中一定是甲烷和乙烯 |
| C、混合气体中一定没有乙烷 |
| D、混合气体中一定有乙烯 |
| 3.6g |
| 18g/mol |
| 3.6g |
| 18g/mol |


科目:高中化学 来源: 题型:
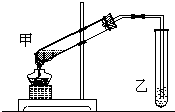 如图是某学生设计的制取乙酸乙酯的实验装置图,并采取了以下主要实验操作:
如图是某学生设计的制取乙酸乙酯的实验装置图,并采取了以下主要实验操作:查看答案和解析>>
科目:高中化学 来源: 题型:
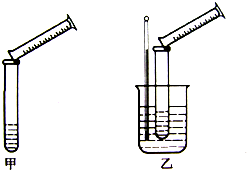 硫代硫酸钠与稀硫酸的反应为:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)
硫代硫酸钠与稀硫酸的反应为:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略) | 实验组号 | 温度 | Na2S2O3 | H2SO4 | 加入H2O 的体积 | 出现沉淀 所需时间 | ||
| 体积 | 浓度 | 体积 | 浓度 | ||||
| Ⅰ | 0℃ | 5mL | 0.1mol/L | 10mL | 0.1mol/L | 5mL | 8s |
| Ⅱ | 0℃ | 5mL | 0.1mol/L | 5mL | 0.1mol/L | 10mL | 12s |
| Ⅲ | 30℃ | 5mL | 0.1mol/L | 5mL | 0.1mol/L | 10mL | 4s |
| Ⅳ | 30℃ | 5mL | 0.2mol/L | 5mL | 0.2mol/L | 10mL | 2s |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2s22p2 和2s22p4 |
| B、3s23p4 和2s22p4 |
| C、3s2 和2s22p5 |
| D、3s1 和3s23p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
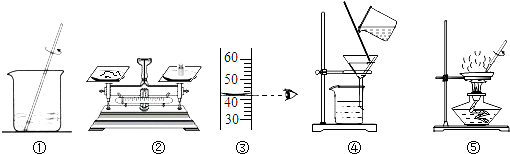
| A、甲实验的步骤是①④⑤,其中去除杂质的关键步骤是蒸发 |
| B、甲实验各步操作中,玻璃棒的作用都是相同的 |
| C、乙实验若按照②③①的步骤进行操作,砝码为5g(游码读数0),则配制的溶液浓度偏大(p水=1g/cm3) |
| D、乙实验中,若①所用的烧杯内壁沾有水,对配制的溶液浓度无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用大米酿造的酒在一定条件下密封保存,时间越长越香醇 |
| B、欲将蛋白质从溶液中析出而又不改变它的性质,可加CuSO4溶液 |
| C、乙烯使溴水褪色与苯使溴水褪色的原因相同 |
| D、纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④⑤ | B、②③ | C、①③ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
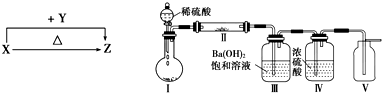
查看答案和解析>>
科目:高中化学 来源: 题型:
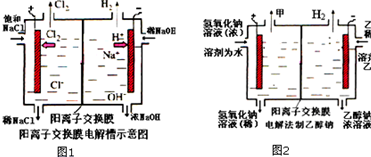 工业上生产氯气,常用电解槽电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.如图1为电解槽的示意图.
工业上生产氯气,常用电解槽电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.如图1为电解槽的示意图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com