
| A. | K2SO4•2Cr2(SO4)3 | B. | 2K2SO4•Cr2(SO4)3 | C. | K2SO4•Cr2(SO4)3 | D. | K2SO4•$\frac{1}{2}$Cr2(SO4)3 |
分析 3.81gI2的物质的量为0.015mol,根据电子转移守恒计算Cr2O72-的物质的量,根据Cr元素守恒可知n(Cr3+)=2n(Cr2O72-);溶液中加入过量的BaCl2溶液,得到4.66g白色沉淀为硫酸钡,硫酸钡的物质的量为0.02mol,根据硫酸根守恒可知,溶液中n(SO42-)=0.02mol;溶液为电中性,所以n(K+)+3n(Cr3+)=2n(SO42-),计算n(K+),根据K+、Cr3+、SO42-的物质的量之比判断X的化学式.
解答 解:3.81gI2的物质的量为:$\frac{3.81g}{254g/mol}$=0.015mol,根据电子转移守恒可知:n(Cr2O72-)×2×(6-3)=0.015mol×2,解得:n(Cr2O72-)=0.005mol,根据Cr元素守恒可知:n(Cr3+)=2n(Cr2O72-)=0.005mol×2=0.01mol;
溶液中加入过量的BaCl2溶液,得到4.66g白色沉淀为硫酸钡,硫酸钡的物质的量为:$\frac{4.66g}{233g/mol}$=0.02mol,根据硫酸根守恒可知,溶液中n(SO42-)=0.02mol;
根据溶液为电中性可得:n(K+)+3n(Cr3+)=2n(SO42-),则:n(K+)=2n(SO42-)-3n(Cr3+)=0.02mol×2-0.01mol×3=0.01mol,
故化合物X中K+、Cr3+、SO42-的物质的量之比为:0.01mol:0.01mol:0.02mol=1:1:2,
所以化合物X的化学式为:K2SO4•Cr2(SO4)3,
故选C.
点评 本题考查了复杂化学式的计算,题目难度中等,注意质量守恒定律、电荷守恒在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题

| 序号 | 烧瓶中的物质 | 实验记录 | 实验结论 |
| 实验一 | 足量MnO2 | a.充分反应后未见黑色固体物质减少 b.收集到112mL气体 | ①催化剂 |
| 实验二 | 足量MnO2和稀硫酸 | c.充分反应后黑色粉末部分溶解 d.收集到112mL气体 | ②氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
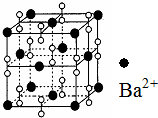 钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如图所示,有关说法正确的是( )
钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如图所示,有关说法正确的是( )| A. | 该晶体为分子晶体 | |
| B. | 晶体的化学式为Ba2O2 | |
| C. | 该氧化物的电子式为 | |
| D. | 与每个Ba2+距离相等且最近的Ba2+共有6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池的电解液为碱性溶液,负极为Fe | |
| B. | 电池放电过程中,正极附近溶液的pH增大 | |
| C. | 电池放电时,电解质溶液中OH-移向正极 | |
| D. | 电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1 mol•L-1的硫化钠溶液中:c(OH-)═c(H+)+c(HS-)+c (H2S) | |
| B. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | 在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) | |
| D. | 0.2mol•L-1HCN溶液和0.1mol•L-1的NaOH溶液等体积混合:c(HCN)+c(CN-)═2 c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
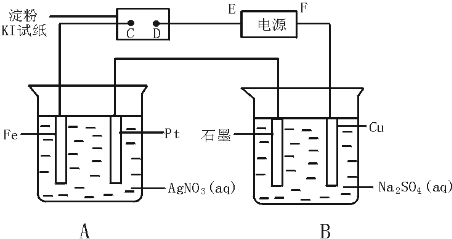
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
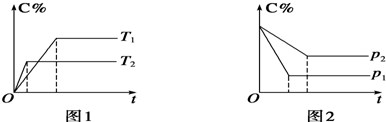
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | NaOH溶液体积/mL | 滴定消耗滤液体积/mL |
| 1 | 25.00 | 20.02 |
| 2 | 25.00 | 17.10 |
| 3 | 25.00 | 19.98 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com