
| A. | 依据分子组成中含有氢原子的数目,将酸分为一元酸、二元酸等 | |
| B. | 依据是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 依据分散质粒子直径的大小,将分散系分为溶液、胶体、浊液 | |
| D. | 依据组成元素的种类,将纯净物分为单质和化合物 |
分析 A、根据酸能电离出的氢离子的个数,酸分为一元酸、二元酸;
B、有电子得失或偏移的为氧化还原反应;
C、溶液、胶体和浊液的本质区别是分散质粒子直径的大小;
D、由一种元素构成的纯净物为单质,由两种或以上元素构成的纯净物为化合物.
解答 解:A、根据酸能电离出的氢离子的个数,酸分为一元酸、二元酸,而不是根据含有的氢原子的个数,如醋酸,含4个氢原子,但是一元酸,故A错误;
B、有电子得失或偏移的为氧化还原反应,无电子得失或偏移的为非氧化还原反应,故B正确;
C、溶液、胶体和浊液的本质区别是分散质粒子直径的大小,极根据分散质粒子直径大小,可以分为溶液、胶体和浊液,故C正确;
D、由一种元素构成的纯净物为单质,由两种或以上元素构成的纯净物为化合物,故纯净物分为单质和化合物是根据构成元素的种类,故D正确.
故选A.
点评 本题考查了常见的概念以及物质和概念的分类标准,难度不大,应注意的是酸的分类标准的掌握.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:实验题
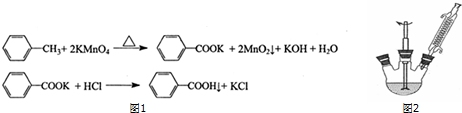
| 名称 | 相对分子质量 | 性状 | 熔点/℃ | 溶解度 | |
| 水 | 乙醇 | ||||
| 甲苯 | 92 | 无色液体易烯易挥发 | -95 | 不溶 | 易溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4(100℃升华) | 25℃0.35g 80℃2.7g | 易溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
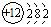 ,O2-结构示意图:
,O2-结构示意图: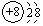 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
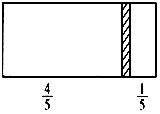 一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入1molN2,右边充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法正确的是( )
一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入1molN2,右边充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法正确的是( )| A. | 右边与左边分子数之比为4:1 | |
| B. | 右侧CO的质量为5.6 g | |
| C. | 右侧气体密度是相同条件下氢气密度的14倍 | |
| D. | 若改变右边CO的充入量而使隔板处于容器正中间,保持温度不变,则应充入0.2molCO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量 | B. | 摩尔质量 | C. | 质量分数 | D. | 物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通式相同的不同物质一定属于同系物 | |
| B. | 完全燃烧某有机物,生成CO2和H2O的物质的量之比为1:1,该有机物只可能是烯烃或环烷烃 | |
| C. | 分子式相同而结构不同的化合物一定互为同分异构体 | |
| D. | 符合通式CnH2n-2的有机物一定是炔烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com