
| A、元素Z、W的简单离子的电子层结构相同 |
| B、元素Y的简单气态氢化物的热稳定性比Z的弱 |
| C、由X、Y、Z三种元素形成化合物,其水溶液可能显碱性 |
| D、W、Z两种元素形成的化合物中肯定不含共价键 |


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案科目:高中化学 来源: 题型:
 焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①③ | B、只有①②③ |
| C、只有②③④ | D、有①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实.2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),则可推测该反应是吸热反应 | ||
B、室温下,将浓度为0.1mol?L?1HF溶液加水稀释,其电离平衡常数和
| ||
| C、电解精练铜时,阳极泥中常含有金属金、银、锌等 | ||
| D、锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后再用酸溶解去除 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正反应活化能不小于100kJ?mol-1 |
| B、正反应活化能小于100kJ?mol-1 |
| C、逆反应活化能一定小于100kJ?mol-1 |
| D、正反应活化能比逆反应活化能小100kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
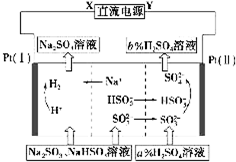 用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中正确的是( )
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中正确的是( )| A、X为直流电源的正极,Y为直流电源的负极 |
| B、阳极区pH减小 |
| C、图中的b<a |
| D、阴极的电极反应为HSO3--2e-+H2O═SO42-+3H+和SO32--2e-+2H2O═SO42-+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、MnO2与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| B、Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O | ||||
| C、双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-═I2+2H2O | ||||
| D、磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
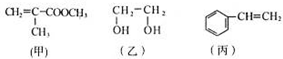 “神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料.如图甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料.下列说法中,错误的是( )
“神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料.如图甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料.下列说法中,错误的是( )| A、甲物质可以在引发剂作用下生成有机高分子化合物 |
| B、1mol乙物质可与2mol钠完全反应生成1mol氢气 |
| C、丙物质能够使酸性高锰酸钾溶液退色 |
| D、甲、乙、丙三种物质都可以发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com