
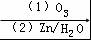 RCHO+R′CHO (R、R′代表烃基或氢)
RCHO+R′CHO (R、R′代表烃基或氢)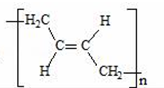 b.
b.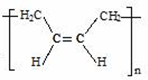 c.
c.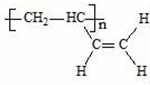
 .
. .
.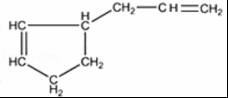 .
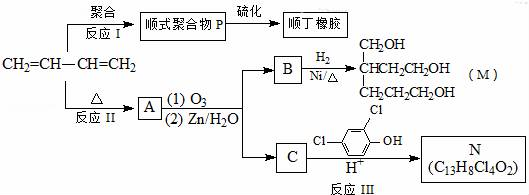
. 分析 根据转化关系知,1,3-丁二烯发生聚合反应I得到顺式聚合物P为聚顺1,3-丁二烯,则P的结构简式为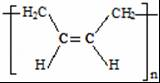 ,由信息i知,在加热条件下发生反应II生成A,A的结构简式为
,由信息i知,在加热条件下发生反应II生成A,A的结构简式为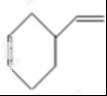 ,A发生反应生成B和C,B和氢气发生加成反应生成M,则B的结构简式为
,A发生反应生成B和C,B和氢气发生加成反应生成M,则B的结构简式为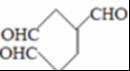 ,C和二氯苯酚发生反应生成N,C为醛,根据N中碳原子个数知,一个C分子和两个二氯苯酚分子发生反应生成N,N的结构简式为
,C和二氯苯酚发生反应生成N,C为醛,根据N中碳原子个数知,一个C分子和两个二氯苯酚分子发生反应生成N,N的结构简式为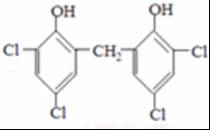 ,则C的结构简式为HCHO,以此解答该题.
,则C的结构简式为HCHO,以此解答该题.
解答 解:根据转化关系知,1,3-丁二烯发生聚合反应I得到顺式聚合物P为聚顺1,3-丁二烯,则P的结构简式为 ,由信息i知,在加热条件下发生反应II生成A,A的结构简式为
,由信息i知,在加热条件下发生反应II生成A,A的结构简式为 ,A发生反应生成B和C,B和氢气发生加成反应生成M,则B的结构简式为
,A发生反应生成B和C,B和氢气发生加成反应生成M,则B的结构简式为 ,C和二氯苯酚发生反应生成N,C为醛,根据N中碳原子个数知,一个C分子和两个二氯苯酚分子发生反应生成N,N的结构简式为
,C和二氯苯酚发生反应生成N,C为醛,根据N中碳原子个数知,一个C分子和两个二氯苯酚分子发生反应生成N,N的结构简式为 ,则C的结构简式为HCHO,
,则C的结构简式为HCHO,
(1)CH2=CH-CH=CH2的名称是1,3-丁二烯,故答案为:1,3-丁二烯;
(2)通过以上分析知,反应Ⅰ的反应类型是加聚反应,故选a;
(3)通过以上分析知,顺式聚合物P的结构式是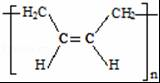 ,故选b;
,故选b;
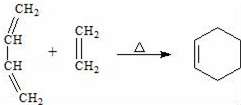
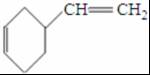
(4)①A的相对分子质量为108,1,3-丁二烯的相对分子质量是54,则A的结构简式为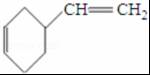 ,则
,则
反应Ⅱ的化学方程式是2CH2=CH-CH=CH2$\stackrel{△}{→}$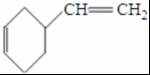 ,
,
故答案为:2CH2=CH-CH=CH2$\stackrel{△}{→}$ ;
;
②B的结构简式为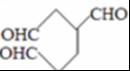 ,1mol B完全转化成M所消耗H2的物质的量是3mol,则氢气的质量是6g,故答案为:6;
,1mol B完全转化成M所消耗H2的物质的量是3mol,则氢气的质量是6g,故答案为:6;
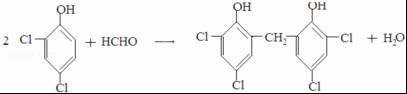
(5)C是甲醛,甲醛和二氯苯酚反应生成N,所以反应Ⅲ是C和二氯苯酚反应生成的化学方程式是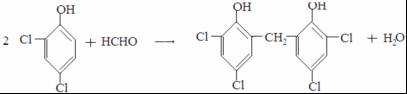 ,
,
故答案为: ;
;
(6)根据以上分析知,B是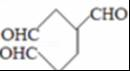 、C是HCHO,A的某些同分异构体在相同的反应条件下也能生成B和C,符合条件A的同分异构体有
、C是HCHO,A的某些同分异构体在相同的反应条件下也能生成B和C,符合条件A的同分异构体有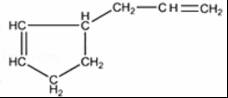 ,故答案为:
,故答案为: .
.
点评 本题考查了有机物的推断,为高考常见题型,侧重于学生的分析能力的考查,根据1,3-丁二烯为突破口结合题给信息、M和N的结构简式确定发生的反应,注意理解题给信息中有机物的断键和成键物质,难点是同分异构体结构简式的判断,题目难度中等.


科目:高中化学 来源: 题型:实验题
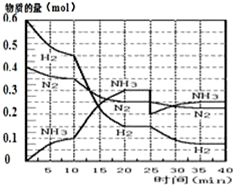 氨的合成原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.4KJ•mol-1.现在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各物质的物质的量变化如图.
氨的合成原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.4KJ•mol-1.现在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各物质的物质的量变化如图.| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
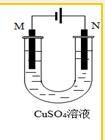
| A. | 若用于精炼粗铜,所得电解铜的纯度可达99.95%~99.98% | |
| B. | 若用于精炼粗铜,在N极附近得到阳极泥,可作为提炼金、银等贵重金属的原料 | |
| C. | 若用于精炼粗铜,则M极为粗铜 | |
| D. | 若用于铁片镀铜,则M极为铁片 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④⑤ | C. | ②④⑤ | D. | ①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com