
【题目】一定条件下存在反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,各容器中充入的物质的物质的量如下表,700℃ 条件下开始反应。达到平衡时,下列说法正确的是
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,各容器中充入的物质的物质的量如下表,700℃ 条件下开始反应。达到平衡时,下列说法正确的是
容器 | 充入容器中的物质的物质的量 |
Ⅰ | 1 mol CO和 1 mol H2O |
Ⅱ | 1 mol CO2和1 mol H2 |
Ⅲ | 2 mol CO和2 mol H2O |
A. 容器Ⅰ、Ⅱ中正反应速率相同
B. 容器Ⅰ、Ⅲ中反应的平衡常数相同
C. 容器Ⅰ中CO的物质的量比容器Ⅱ中的少
D. 容器Ⅰ中CO的转化率与容器Ⅱ中CO2 的转化率之和小于1
【答案】D
【解析】
A.在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,刚开始时,容器I中正反应速率最大,容器II中正反应速率为零,达到平衡时,容器I温度大于700℃,容器II温度小于700℃,所以容器Ⅰ中的正反应速率大于容器Ⅱ中正反应速率,A错误;
B.容器III可看成容器I体积压缩一半,各物质浓度增加一倍,若温度恒定,则平衡不移动;但恒容绝热的情况下,容器III中温度比容器I高,更有利于平衡向逆反应方向移动,升高温度,平衡向吸热的逆反应方向移动,所以化学平衡常数K(I)>K(III),B错误;
C.容器Ⅰ从正反应方向开始,容器III从逆反应方向开始,由于该反应的正反应为放热反应,所以反应达到平衡时,容器Ⅰ的温度高于容器II,升高温度,化学平衡逆向移动,因此I中CO的物质的量比容器Ⅱ中的多,C错误;
D.根据选项C可知容器I、II的温度不相同,容器I的温度高于700℃,容器II温度低于700℃。若容器II的温度也是700℃,一个从正反应方向开始,一个从逆反应方向开始,I中CO的转化率与容器Ⅱ中CO2 的转化率之和等于1,但容器II温度低于700℃,降低温度,平衡正向移动,使CO2的转化率降低,因此容器Ⅰ中CO的转化率与容器Ⅱ中CO2 的转化率之和小于1,D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
Ⅰ.分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得生成7.2gH2O和13.2gCO2,消耗氧气10.08L(标准状况),则该物质中各元素的原子个数之比是____________________。
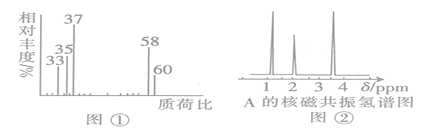
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为________,该物质的分子式是_______________。
(3)根据价键理论,预测A可能的结构简式: _________________________。
Ⅱ.结构式的确定:
(4)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值可以确定分子中氢原子的种类和数目。经测定,有机物A的核磁共振氢谱如图②,则A的结构简式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、Q是原子序数依次增大的前四周期元素,W是宇宙中最丰富的元素;X、Z元素原子基态时,核外电子均排布在3个能级上,且它们的价电子层上均有2个未成对电子;向含有 QSO4的溶液中滴加氨水,生成蓝色沉淀,继续滴加氨水,沉淀溶解,得深蓝色溶液。请回答下列问题:
(1)Y元素在周期表中的位置为___________, Z原子的价电子排布图为___________________
(2)W可分别与X、Y形成多种化合物,其中,最简单化合物的稳定性由强到弱的顺序为_____(用分子式表示);Y的一种氢化物能在卫星发射时作燃料,写出该氢化物的结构式_______________。
(3)继续滴加氨水,沉淀溶解时反应:____________________________(用离子方程式表示),向深蓝色溶液中再加乙醇,会析出深蓝色的[Q(NH3)4]SO4·H2O晶体,该晶体中含有的化学键____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化学方程式及反应类型均正确的是( )
A. CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 脂化反应
CH3COOCH2CH3+H2O 脂化反应
B. CH2=CH2+HOCl → HOCH2—CH2Cl 加聚反应
C. 2CH3CH2OH+O2![]() 2CH3CHO+H2O 氧化反应
2CH3CHO+H2O 氧化反应
D. CH3Cl+Cl2![]() CH2Cl2+HCl 取代反应
CH2Cl2+HCl 取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化不可能通过一步反应直接完成的是
A. Al(OH)3 → Al2O3 B. Al2O3 → Al(OH)3
C. Al → AlO2- D. Al3+ → Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应式:mX(g)+nY(?)![]() pQ(s)+2mZ(g),已知反应已达平衡,此时c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的
pQ(s)+2mZ(g),已知反应已达平衡,此时c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的![]() ,c(X)=0.5mol/L,下列说法正确的是( )
,c(X)=0.5mol/L,下列说法正确的是( )
A.反应向逆方向移动B.Y可能是固体或液体
C.系数n>mD.Z的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学为了探究铜与浓硫酸的反应,进行了一系列实验。在反应过程中会发生一些副反应,生成不溶于水和酸的CuS、Cu2S。
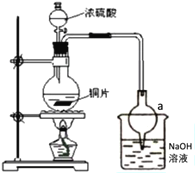
(1)处于安全和绿色化学考虑,在制取硫酸铜时,可选用下列的物质是____。
a.Cu b.CuO c.CuS d.CuSO4·Cu(OH)2H2O
(2)装置a的作用是___。反应过程中,因为浓硫酸的吸水作用,烧瓶中出现白色固体物质,如何简便检验反应后圆底烧瓶里有Cu2+存在?___。在实际反应中,由于条件控制不好,容易产生CuS和Cu2S固体:2CuS![]() Cu2S+S。
Cu2S+S。
(3)已知样品质量为ag,得到Cu2S是bg,则样品中CuS质量分数是___。如果Cu2S高温下转化为Cu,则实验测得的值会___(填“偏大”、“偏小”或“不变”)
(4)根据以上信息,说明铜与浓硫酸反应需要控制哪些条件?___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式如图所示。该物质具有下列的结构和性质,不正确的是( )
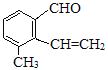
A.最多可以和5molH2发生加成反应
B.所有原子有可能在同一平面内
C.能与Br2在光照下发生取代
D.能与Ag(NH3)2OH溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成气的主要组分为CO和H2;以天然气为原料生产的合成气有多种方法,其中Sparg工艺的原理为CH4(g)+CO2(g)2CO(g)+2H2(g)。在特定温度下,向甲、乙、丙三个密闭容器中充入相同量的CH4(g)和CO2(g),改变容器体积,测得平衡时容器内气体的浓度如下表所示:
实验编号 | 容器温度/℃ | 容器体积 | 物质浓度/(mol·L-1) | ||
CH4 | CO2 | CO | |||
甲 | 300 | V1 | 0.02 | 0.02 | 0.10 |
乙 | 300 | V2 | x | x | 0.05 |
丙 | 350 | V1 | y | y | 0.12 |
下列说法正确的是( )
A.该反应在低温条件下不能自发进行
B.300 ℃时反应的平衡常数为25
C.V1∶V2=3∶7
D.保持温度和容器体积不变,开始时向甲容器中充入0.28 mol CO和0.28 mol H2,CO转化率一定大于2/7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com