
 物质A在一定条件下反应制得新型纤维酸类降脂药克利贝特,其结构简式如图所示,下列有关叙述正确的是( )
物质A在一定条件下反应制得新型纤维酸类降脂药克利贝特,其结构简式如图所示,下列有关叙述正确的是( )| A. | 物质A分子中含有2个手性碳原子 | |
| B. | 物质A分子中所有碳原子可能位于同一平面内 | |
| C. | 1 mol物质A最多可以与含4molBr2的溴水反应 | |
| D. | 物质A可以发生加成反应、氧化反应、水解反应 |
科目:高中化学 来源: 题型:解答题
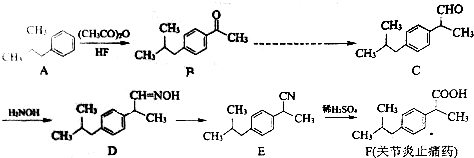
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .P元素属于p区元素,
.P元素属于p区元素,
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
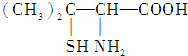
| A. | 青霉氨基酸分子中所有碳原子均在同一直线上 | |
| B. | 青霉氨基酸具有两性并能发生酯化反应 | |
| C. | 青霉氨基酸分子间不能发生缩合反应 | |
| D. | 1 mol青霉氨基酸与足量的金属钠反应生成0.5 mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 (用元素符号表示)
(用元素符号表示)查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com