
����Ŀ������������Ȼ���е������٣���;�dz��㷺��ͨ���Ի����Ϊԭ����ȡ�����飬����������ͼ��ʾ��
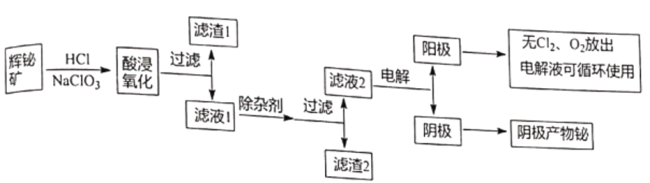
��֪���ٻ������Ҫ�ɷ���Bi2S3����������Bi2O3��SiO2�����������������ȡ�
��Bi2O3�������ᣬNaBiO3������ˮ��
�۳����£�Ksp[Fe(OH)3]=4��10-38,Ksp[Bi (OH)3]=4��10-30��Ksp[Fe(OH)2]=8.0��10-16��
�ش��������⣺
��1��д���������ʱBi2S3�����������ʵĻ�ѧ����ʽ_______________��
��2������1�ijɷ�Ϊ_______________��
��3�����Ӽ�������a.������ҺpH,b_______________��д��һ������߲�������ij��Ӽ�_______________��
��4����Һ2���������Ʊ�NaBiO3,������Һ2�м���NaOH��NaClO��Һ��ȡNaBiO3,д���÷�Ӧ�����ӷ���ʽ_______________��
��5����Һ2���õ�ⷨ��ȡ�����鵥�ʣ��������ﴦ����ɼ���ѭ��ʹ�ã����װ����ͼ��ʾ��
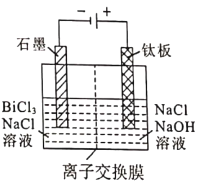
�ٽ���Ĥ����Ϊ_______________���Cl-����OH-��)����Ĥ��
�������缫��ӦʽΪ_______________��
���𰸡�Bi2S3+6HCl+NaClO3=2BiCl3+NaCl+3S��+3H2O S��SiO2 ��ȥ����Fe3+ Bi2O3��Bi(OH)3 Na++Bi3++C1O-+4OH-=NaBiO3��+Cl-+2H2O Cl- Cl-+6OH--6e-=ClO3-+3H2O
��������
����������������ˣ��õ�����1Ϊ��������Ķ��������Bi2S3�����������ɵ����ʣ���Һ1�к���BiCl3��NaCl��FeCl3�ȣ�Ϊ�˱������������ʣ������ij����Լ�������Bi2O3��Bi(OH)3��Ŀ���ǵ���pHʹ������ת��������������ȥ����Һ2�е���Ҫ�ɷ�Ϊ�Ȼ��ƺ�BiCl3�������õ��鵥�ʡ�
��1���������ʱBi2S3�����������ʵĻ�ѧ����ʽΪBi2S3+6HCl+NaClO3=2BiCl3+NaCl+3S��+3H2O���ʴ�Ϊ��Bi2S3+6HCl+NaClO3=2BiCl3+NaCl+3S��+3H2O��
��2���ɷ���֪������1�ijɷ�ΪS��SiO2���ʴ�Ϊ��S��SiO2��
��3���ɷ���֪������Bi2O3��Bi(OH)3����pHʹ������ת������������������ȥ���ʴ�Ϊ����ȥ����Fe3+��Bi2O3��Bi(OH)3��
��4����Һ2�е���Ҫ�ɷ�Ϊ�Ȼ��ƺ�BiCl3������NaOH��NaClO��Һ��ȡNaBiO3ʱ������Ӧ�����ӷ���ʽΪNa++Bi3++C1O-+4OH-=NaBiO3��+Cl-+2H2O���ʴ�Ϊ��Na++Bi3++C1O-+4OH-=NaBiO3��+Cl-+2H2O��
��5����������Ϊ�����ӣ����ʱ���������������ŵ磬������������������Ĥ����ΪCl-����Ĥ���ʴ�Ϊ��Cl-��
�������缫���������ӷŵ�ת��Ϊ��������缫��ӦʽΪCl-+6OH--6e-=ClO3-+3H2O���ʴ�Ϊ��Cl-+6OH--6e-=ClO3-+3H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾ�ķ�Ӧ�ж�����˵���д������
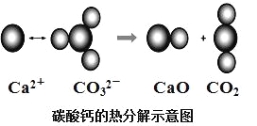
A. CO2(g)��CaO(s)������������CaCO3(s)��������
B. �÷�Ӧ���ʱ������
C. �÷�Ӧ�������Ӽ�����Ҳ�й��ۼ����ѣ���ѧ������������������ѧ�����ɷų�����
D. �ɸ÷�Ӧ���Ƴ�������Ҫ���Ȳŷ����ķ�Ӧ��Ϊ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹ�õ���(CuSO45H2O)����0.1mol/L������ͭ��Һ����ȷ�IJ�����_______
A.���������ȳ�ȥ�ᾧˮ��ȡ16g�ܽ���1Lˮ��
B.��ȡ25g��������ˮ��Ȼ����Һϡ����1L
C.��ȡ25g�����ܽ���1Lˮ��
D.��16g��������ˮ��Ȼ����Һϡ����1L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���о���Ч����úȼ���ͷų�����SO2�������ڼ�С������Ⱦ����T��ʱ������CO����SO2�ķ�ӦΪ��2CO(g)+SO2(g)![]() 2CO2(g)+S(l) ��H=akJ/mol��
2CO2(g)+S(l) ��H=akJ/mol��
��1����֪T��ʱ��C(s)+![]() O2(g)=CO(g) ��H1=-110.5kJ/mol
O2(g)=CO(g) ��H1=-110.5kJ/mol
S(l)+O2(g)=SO2(g) ��H2=-290.0kJ/mol
C(s)+O2(g)=CO2(g) ��H3=-390.0kJ/mol
��T��ʱ��a=___��
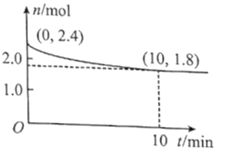
��2����T���£���1.4molCO��1molSO2ͨ��2L���������з���������Ӧ����Ӧ��ϵ���������ʵ�����ʱ��仯��ͼ����0~10min����Ӧ��ƽ������v(CO)=___��SO2��ƽ��ת����![]() (SO2)=___%����T��ʱ�÷�Ӧ��ƽ�ⳣ��Kc=___L/mol��
(SO2)=___%����T��ʱ�÷�Ӧ��ƽ�ⳣ��Kc=___L/mol��
��3��ʵ���ã�v��=v(CO)����=k��c(CO)c(SO2)��v��=v(CO2)����=k��![]() ��k����k��Ϊֻ���¶�Ӱ������ʳ�����������2���������ڵ��¶����ߣ���������ʵ�״̬�������仯����
��k����k��Ϊֻ���¶�Ӱ������ʳ�����������2���������ڵ��¶����ߣ���������ʵ�״̬�������仯����![]() ��ֵ��___������������������С������������)��
��ֵ��___������������������С������������)��
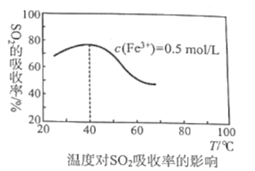
��4��ij�����Ŷ��о���Fe2(SO4)3(aq)����SO2��Fe3+��Һ����SO2���������ӷ�Ӧ����ʽΪ___������������������£�����ͬʱ�����¶ȶ�SO2�����ʵ�Ӱ������ͼ����40��ǰ��SO2�����������¶ȱ仯�Ŀ���ԭ����___����40���SO2�������ʷ����ı仯���¶����߸÷�Ӧ�����ƶ��Ľ�������·�Ӧ�����ƶ���ԭ��һ�Ǹ÷�ӦΪ���ȷ�Ӧ������___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС����������ʾװ����ȡ����ء��������ƺ���ˮ������̽��ʵ�顣
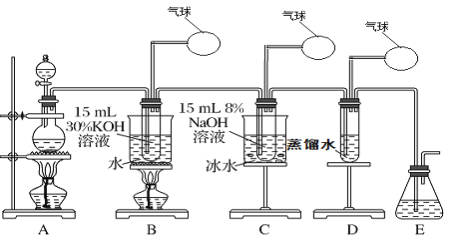
ʵ����.��ȡ����أ�KClO3�����������ơ���ˮ
��1��д��װ��Aʵ������ȡCl2�Ļ�ѧ��Ӧ����ʽ_________________________
��2����ȡʵ�������ȡ��װ��B�е��Թܣ���ȴ�ᾧ�����ˡ�ϴ�ӣ���ʵ�����������Ҫ�IJ��������н�ͷ�ιܡ��ձ���________��________��
��3��д��B���Ʊ�����أ�KClO3���ķ���ʽ____________________
��4��װ��C�з�Ӧ��Ҫ�ڱ�ˮԡ�н��У���ԭ����_____________________________
���ϣ�SO2��һ�������������CO2���ƣ�2NaOH(����)+SO2=Na2SO3+H2O ,SO32-�ǻ�ԭ�Ժ�ǿ�����ӣ�����Һ����������ǿ�����Ӳ��ܴ������棬�ױ�������SO42����
ʵ����.β������
ʵ��С�����ø����չ�����SO2��NaOH��Һ����β���������մ�����
��5������β��һ��ʱ�������Һ(ǿ����)�п϶�����Cl����OH����![]()
�����ʵ�飬̽��������Һ�п��ܴ��ڵ�����������(�����ǿ����е�CO2��Ӱ��)��
������������裺
����1��ֻ����![]() ��
��
����2���Ȳ�����![]() Ҳ������ClO����
Ҳ������ClO����
����3��______________________________��
�����ʵ�鷽��������ʵ�顣���ڱ���д��ʵ�鲽���Լ�Ԥ������ͽ��ۡ�
��ѡʵ���Լ���3mol��L��1 H2SO4��1mol��L��1 NaOH��Һ��0.01mol��L��1����KMnO4��Һ�����ۡ�KI��Һ��
ʵ�鲽�� | Ԥ������ͽ��� |
����1��ȡ��������Һ������A��B�Թ��� | |
����2����A�Թ��еμ�0.01 mol��L��1����KMnO4��Һ | (1)����Һ��ɫ�������1���� (2)����Һ����ɫ�������2��3���� |
����3��____________________________________ | __________________________________ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���Ʊ����跴Ӧ���Ȼ�ѧ����ʽ���£�SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g) ����=+QkJ/mol(Q>0)��ij�¶ȡ�ѹǿ�£���һ������Ӧ��ͨ���ܱ������������Ϸ�Ӧ������������ȷ���ǣ� ��
Si(s)+4HCl(g) ����=+QkJ/mol(Q>0)��ij�¶ȡ�ѹǿ�£���һ������Ӧ��ͨ���ܱ������������Ϸ�Ӧ������������ȷ���ǣ� ��
A.��Ӧ�����У�������ѹǿ�����SiCl4��ת����
B.����Ӧ��ʼʱSiCl4Ϊ1mol�����ƽ��ʱ����������ΪQkJ
C.��Ӧ��2minʱ����HClŨ��Ϊ0.12mol/L����H2�ķ�Ӧ����0.03mol/(L��min)
D.����Ӧ��������0.25QkJʱ�����ɵ�HClͨ�뺬0.1mol NaOH����Һǡ�÷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С������Ǧ����Ϊֱ����Դ�����е�������ˮ��ʵ��̽������Ƶ�ʵ��װ����ͼ��ʾ������˵����ȷ����
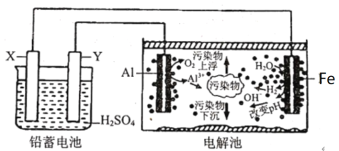
A.Y�缫��ӦΪPb+SO42--2e-=PbSO4
B.ÿ����103.5gPb, �����ϵ�����������1molH2����
C.�õ��ص��ܷ�ӦΪ2Al+6H2O![]() 2Al(OH)3+3H2��
2Al(OH)3+3H2��
D.����ˮΪ����Cr2O72-��ҵ���Է�ˮ��Ϊ����ת��ΪCr3+��ȥ���������缫����Ǧ���ص�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С����100mL0.50mol/LNaOH��Һ��60mL0.50mol/L��������к��ȵIJⶨ��װ����ͼ��ʾ���ش��������⣺
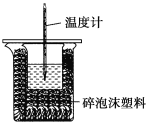
��1����ʵ�鹲��Ҫ400mLNaOH��Һ��ʵ���������Ƹ���Һʱ������Ҫ����NaOH����____g��
��2��ͼ��װ��ȱ�ٵ�������____��
��3�������Թ�����ԭ����____��
��4������д�±��е�ƽ���¶Ȳ
ʵ�� ���� | ��ʼ�¶�T1/�� | ��ֹ�¶� T2/�� | ƽ���¶Ȳ� (T2��T1)/�� | ||
HCl | NaOH | ƽ��ֵ | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ____ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
��5��������Ϊ0.50 mol/L NaOH��Һ��0.50 mol/L������Һ���ܶȶ���1 g/cm3���кͺ�������Һ�ı�����Ϊc=4.18J/(g��)������ʵ���к�����H=___��ȡС�����һλ��
��6������ʵ������57.3kJ/mol��ƫ�����ƫ���ԭ�������____
A����ȡNaOH��Һʱ���Ӷ���
B��Ϊ��ʹ��Ӧ��֣����������зִμ����
C��ʵ��װ�ñ��¸���Ч����
D����ͭ˿���沣��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ת����ϵ���ش����⣺

��֪������CH3Br![]() CH3��HBr��
CH3��HBr��
��C���ʱ�����һ±����ֻ�����֡�
(1)д��B���ʵ�����__________��D���ʵĽṹ��ʽ________��
(2)д����Ӧ��������________����Ӧ��������________��
(3)д����Ӧ���Ļ�ѧ����ʽ��________________________________��
(4)д��D��E��Ӧ�Ļ�ѧ����ʽ��_______________��
(5)��Ӧ�����п�������һ��C16H18���л���䱽����һ±����Ҳֻ�����֣�д�����Ľṹ��ʽ��_______________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com