
分析 根据实验(1)现象:溶液呈强酸性,说明溶液中肯定含有H+,与H+发生反应的不能共存;
根据实验(2)现象:CCl4层呈紫红色,说明有I2,说明原溶液中含有I-,而I-与Fe3+、NO3-和H+发生反应而不能共存;
根据实验(3)现象:溶液从酸性逐渐变为碱性,溶液均无沉淀产生,而Mg2+、Al3+能与碱反应产生沉淀,说明溶液中肯定不含有Mg2+、Al3+;
根据实验(4)现象:取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,说明溶液中肯定含有Ba2+,而Ba2+能与SO42-产生沉淀,说明溶液中不含SO42-再结合问题分析回答.
解答 解:(1)溶液呈强酸性,说明溶液中肯定含有H+,而H+与CO32-发生反应而不能共存,说明溶液中肯定不含有CO32-,
故答案为:CO32-;
(2)CCl4层呈紫红色,说明有I2,这是由于I-被氯气氧化所产生的,从而说明溶液中含有I-,而I-与Fe3+、NO3-和H+发生反应而不能共存,说明溶液中肯定不含有Fe3+、NO3-,
故答案为:I-;Fe3+、NO3-;
(3)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀产生,说明原溶液一定不存在的离子是Al3+、Mg2+、Fe3+,
故答案为:Al3+、Mg2+、Fe3+;
(4)取出(3)所得溶液加Na2CO3溶液后,有白色沉淀生成,说明溶液中肯定含有Ba2+,而Ba2+能与SO42-产生沉淀,说明溶液中不含SO42-,
故答案为:Ba2+;SO42-;
(5)根据以上分析可知,还不能确定的离子为:K+、Cl-,故答案为:K+、Cl-.
点评 本题考查根据实验现象判断离子共存,题目难度不大,明确常见离子的性质及检验方法为解答关键,要掌握根据实验现象判断存在的离子,排除与该离子反应的离子.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③⑤ | C. | ④⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
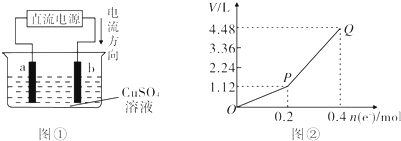
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl NaBr | B. | NaCl NaBr Na2SO4 | ||
| C. | NaCl | D. | Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1000 mL | B. | 500 mL | C. | 100 mL | D. | 1500 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚与氢氧化钠溶液反应 | |
| B. | 溴乙烷与NaOH溶液混和共热CH3CH2Br+NaOH$→_{△}^{水}$CH2═CH2↑+H2O+NaBr | |
| C. | 乙醛与银氨溶液反应 CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O | |
| D. | 乙醇的消去反应 CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;NH4+的空间构型是正四面体.
;NH4+的空间构型是正四面体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>Z>Y>X>M | |
| B. | YM2、Y2X2、W2M2均为直线型的共价化合物 | |
| C. | 元素Z和元素M的最高正价的数值之和等于11 | |
| D. | 由X、Y、Z、M四种元素形成的化合物中可能含有离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com