
下列表示对应化学反应的离子方程式正确的是( )
A.将过量SO2通入少量氨水中:SO2+2NH3·H2O==2NH4++SO32-
B.实验室用Cu和稀HNO3反应制取少量NO气体:
Cu+4H++NO3- ==Cu2++NO↑+2H2O
C.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O
D.KIO3与KI在酸性溶液中反应:5I-+IO3-+3H2O==3I2+6OH-
科目:高中化学 来源: 题型:
A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):
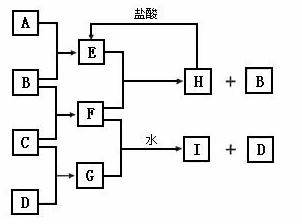
请填写下列空白:
(1)A是 ,C是 。
(2)H与盐酸反应生成E的化学方程式是 。
(3)E与F反应的化学方程式是 。
(4)F与G的水溶液的反应生成I和D的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学知识概括合理的是( )
A.酸性氧化物都是非金属氧化物
B.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C.丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
D.熔融状态能导电的物质一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Al3+、
Fe3+、SO42―、CO32―、Cl―和I―。你取该溶液进行了以下实验:
(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入CCl4及数滴氯水,经振荡后CCl4层呈紫红色;
(3)另取部分溶液,加入稀NaOH 溶液使其变为碱性,溶液中最终无沉淀;
(4)取部分上述碱性溶液,通入过量CO2气体有白色沉淀生成;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝;根据上述实验事实,你可知道该溶液中:
① 肯定含有的离子是 ;
② 肯定不存在的离子是 ;
查看答案和解析>>
科目:高中化学 来源: 题型:
以下物质间的转化,不能通过一步反应实现的是( )
A.S→SO3→H2SO4 B.Al(OH)3→Al2O3→Al
C.Cu→CuCl2→Cu(OH)2 D.Na→Na2O2→Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有NH 、Mg2+、Fe2+、Al3+和SO
、Mg2+、Fe2+、Al3+和SO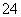 五种离子,若向其中加入过量的Ba(OH)2溶液,微热并搅拌,再加入过量的氢碘酸,溶液中大量减少的离子有( )
五种离子,若向其中加入过量的Ba(OH)2溶液,微热并搅拌,再加入过量的氢碘酸,溶液中大量减少的离子有( )
A.4种 B.3种 C.2种 D.1种
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.无水氯化铝是有机化工常用催化剂,其外观为白色固体,178℃时升华,极易潮解,遇水后会发热并产生白雾。实验室用如下装置制备少量无水氯化铝,其反应原理为:2Al + 6HCl(g) = 2AlCl3 + 3H2
完成下列填空:
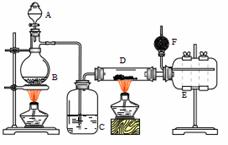
A为浓硫酸,B为NaCl固体
(1)进行实验时应先点燃 (选填“B”或“D”)处酒精灯。
(2)用粗短导管连接D、E的目的是________(选填序号)。
a. 防堵塞 b. 防倒吸 c. 平衡气压 d. 冷凝回流
(3)F中盛有碱石灰,其目的是 (选填序号)。
a. 吸收多余HCl b. 吸收Cl2 c. 吸收CO2 d. 防止空气中H2O进入E瓶
(4)将D中固体改为氯化铝晶体(AlCl3·6H2O)也能进行无水氯化铝的制备,此时通入HCl气体的目的是 。若实验条件控制不当,最终得到的物质是碱式氯化铝[化学式为Al2(OH)nCl(6-n)],且质量是原氯化铝晶体(AlCl3·6H2O)的40%,则可推算n的值为 。
Ⅱ.焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。Na2S2O5溶于水即生成NaHSO3。
(1)证明NaHSO3溶液中HSO3—的电离程度大于水解程度,可采用的实验方法是 (填序号)。
| a.测定溶液的pH | b.加入Ba(OH)2溶液 | c.加入盐酸 |
| d.加入品红溶液 | e.用蓝色石蕊试纸检测 |
(2)检验Na2S2O5晶体在空气中已被氧化的实验方案是________ ______。
(3)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量的方案如下:

(已知:滴定时反应的化学方程式为SO2 + I2 + 2 H2O = H2SO4 + 2 HI)
按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g/L。在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,如图所示,最先观察到变为红色的区域为( )

A.Ⅰ和Ⅱ B.Ⅰ和Ⅳ C.Ⅱ和Ⅲ D.Ⅱ和Ⅳ
查看答案和解析>>
科目:高中化学 来源: 题型:
农业技术人员向农民建议:在塑料大棚中种植植物时,可向大棚中通人适量的C02。
这是因为( )
A.C02可使害虫窒息死亡,从而防治病虫害
B.施用二氧化碳能促进植物进行光合作用,提高产量
C. C02可产生温室效应,从而提高大棚内的温度
D. CO2可灭火,施用后防止火灾
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com