
今有aX、bY、cZ三种元素。已知:①各原子序数a、b、c均小于20,且a+b+c=25; ②元素Y的原子价电子构型为ns2npn+2; ③X和Y在不同条件下可形成X2Y和X2Y2两种化合物,Y和Z在不同条件下可形成ZY和ZY2两种化合物; ④Z的硫化物的相对分子质量与Z氯化物的相对分子质量之比为38︰77。回答下列问题:
(1)X: (写元素名称);Z的价电子排布图为: 。
(2)X2Y2的电子式 ,属于 化合物(填“离子”或“共价”)。
(3)Z的硫化物的VSEPR模型为 ,分子空间构型为 ;Z的氯化物的VSEPR模型和分子空间构型分别是 、 ,其中Z原子分别以 杂化轨道成键,根据原子轨道成键方式分,Z的硫化物分子中含有的键的种类及数目是 、 。
科目:高中化学 来源:2016届甘肃省高三上第三次模拟考试化学试卷(解析版) 题型:选择题
右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化氢溶液,各加入生铁块,放置一段时间。下列有关描述错误的是

A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中负极电极反应相同
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:选择题
在一个绝热的体积一定的密闭容器中发生可逆反应:N2(g) + 3H2(g) 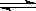 2NH3(g) , △H<0,下列各项中不能说明该反应已经达到平衡状态的是
2NH3(g) , △H<0,下列各项中不能说明该反应已经达到平衡状态的是
A.体系的压强不再改变
B.体系的温度不再改变
C.断裂1mol N≡N键的同时,也断裂6molN—H键
D.反应消耗的N2、H2与产生的NH3的速率υ(N2) : υ(H2) : υ(NH3) == 1∶3 ∶2
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上月考化学试卷(解析版) 题型:选择题
下列事实对应的离子方程式正确的是( )
A.金属钠加入滴有酚酞的水中,溶液变红:Na+2H2O===Na++2OH-+H2↑
B.用NaOH溶液吸收多余的氯气:Cl2+2OH-===Cl-+ClO-+H2O
C.将NaHCO3溶液和过量Ca(OH)2溶液混合有白色沉淀:
2HCO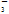 +Ca2++2OH-===CaCO3↓+2H2O+CO
+Ca2++2OH-===CaCO3↓+2H2O+CO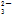
D.将醋酸溶液滴到大理石上有气泡产生:2H++CaCO3===CO2↑+Ca2++H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:填空题
甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。
(1)CO2可用于合成二甲醚(CH3OCH3),有关反应的热化学方程式如下:
CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) ΔH = -49.0kJ·mol-1,
2CH3OH(g) = CH3OCH3(g)+ H2O(g) ΔH =-23.5kJ·mol-1,
则CO2与H2反应合成二甲醚的热化学方程式为 。
(2)若反应2CH3OH(g)  CH3OCH3(g) + H2O(g)在某温度下的化学平衡常数为400,此温度下,在密闭容器中加入一定量甲醇,反应进行到某时刻,测得各物质的浓度如表所示:
CH3OCH3(g) + H2O(g)在某温度下的化学平衡常数为400,此温度下,在密闭容器中加入一定量甲醇,反应进行到某时刻,测得各物质的浓度如表所示:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
浓度(mol·L-1) | 0.44 | 0.60 | 0.60 |
①写出该反应的平衡常数表达式:K= 。
②比较该时刻正、逆反应速率的大小:v(正) v(逆)(填“>”、“<”或“=”)
③若加入甲醇后经 10 min 反应达到平衡,则平衡后c(CH3OH)= ,该时间内反应速率v(CH3OCH3)= 。
(3)工业上合成甲醇的反应:CO(g)+2H2(g) CH3OH(g) ΔH =-90.8kJ·mol-1,若在温度相同、容积均为2L的3个容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时如下:
CH3OH(g) ΔH =-90.8kJ·mol-1,若在温度相同、容积均为2L的3个容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molCO、2 mol H2 | 1 mol CH3OH | 2 mol CO、4 mol H2 |
CH3OH的浓度(mol/L) | c1=0.25 | c2 | c3 |
反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
平衡常数 | K1 | K2 | K3 |
反应物转化率 | α1 | α2 | α3 |
①下列不能说明该反应在恒温恒容条件下已达化学平衡状态的是 。
A. v正(H2)= 2v逆(CH3OH) B. n(CO)﹕n(H2)﹕n(CH3OH)=1﹕2 : 1
C. 混合气体的密度不变 D. 混合气体的平均相对分子质量不变
E. 容器的压强不变
②下列说法正确的是 。
A. c1= c2 B. Q1= Q2 C. K1= K2 D. α2+α3 < 100%
③如图表示该反应的反应速率v和时间t的关系图:
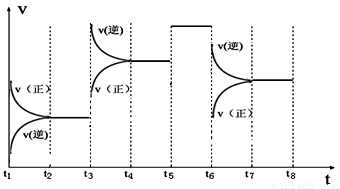
各阶段的平衡常数如下表所示:
t2~t3 | t4~t5 | t5~t6 | t7~t8 |
K4 | K5 | K6 | K7 |
K4、K5、K6、K7之间的关系为 (填“>”、“<”或“=”)。反应物的转化率最大的一段时间是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州市高一上学期期中测试化学试卷(解析版) 题型:填空题
现有部分元素的原子结构特点如下表:
X | 其单质之一是空气中主要成分,最常见的助燃剂 |
Y | 其某种核素不含中子 |
Z | 失去一个电子后,形成Ne原子电子层结构 |
W | 最外层电子数是次外层电子数的2倍 |
(1)写出各元素的元素符号:X_______,Y________,
(2)画出下列微粒的结构示意图Z+________,W原子__________。
(3)写出两种由上述任意三种元素组成的水溶液呈碱性的物质_____________、___________。(填化学式)
查看答案和解析>>
科目:高中化学 来源:2016届浙江省深化课程改革协作校高三上学期11月期中联考化学试卷(解析版) 题型:选择题
我国科学家最新研发的固体透氧膜提取金属钛工艺,其电解装置如右图所示:将TiO2熔于NaCl-NaF融盐体系,以石墨为阴极,覆盖氧渗透膜的多孔金属陶瓷涂层为阳极,固体透氧膜把阳极和熔融电解质隔开,只有O2-可以通过。下列说法不正确的是

A.a 极是电源的正极,O2-在熔融盐中从右往左迁移
B.阳极电极反应式为2O2--4e- = O2↑
C.阳极每产生4.48L的O2,理论上能生成0.2mol钛
D.NaCl-NaF融盐的作用是降低熔化TiO2需要的温度
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期月考化学试卷(解析版) 题型:选择题
已知5KCl+KClO3+3H2SO4===3Cl2↑+3K2SO4+3H2O,下列说法不正确的是
A.KClO3是氧化剂
B.被氧化与被还原的氯元素的质量比为5:1
C.H2SO4既不是氧化剂又不是还原剂
D.1molKClO3参加反应时有10mol电子转移
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省益阳市高一12月月考化学试卷(解析版) 题型:选择题
把NaHCO3和Na2CO3·10H2O混和物6.56g溶于水制成100mL溶液,其中c(Na+)=0.5mol/L。在该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量为
A.2.93 g B.5.85 g C.6.56g D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com