
| 族 周 期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
 _.
_.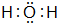 (填该物质的电子式).
(填该物质的电子式).分析 由元素在周期表中的位置可知,①为C,②为N,③为O,④为F,⑤为Mg,⑥为Al,⑦为Si,⑧为S,⑨为Cl,⑩为Ar.
(1)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,稀有气体化学性质最不活泼;元素⑨对应的离子为Cl-,核外电子数为18,各层电子数为2、8、8;
(2)同周期自左而右原子半径减小;
(3)非金属性越强,对应氢氧化物越稳定,H2O比硫化氢稳定;
(4)金属性越强,最高价氧化物对应水化物的碱性越强;
(5)③与⑦形成的化合物为二氧化碳等,碳原子与氧原子之间形成共价键,属于分子晶体.
解答 解:由元素在周期表中的位置可知,①为C,②为N,③为O,④为F,⑤为Mg,⑥为Al,⑦为Si,⑧为S,⑨为Cl,⑩为Ar.
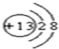
(1)稀有气体Ar的化学性质最不活泼,同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,故上述元素中,金属性最强的元素是镁,最活泼的非金属单质是F2,元素⑨对应的离子为Cl-,核外电子数为18,离子结构示意图为 ,
,
故答案为:Ar;镁;F2; ;
;
(2)同周期自左而右原子半径减小,故第二周上述元素中F原子半径最小,
故答案为:F;
(3)非金属性O>S,非金属性越强,对应氢氧化物越稳定,故H2O比硫化氢稳定,H2O的电子式为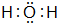 ,
,
故答案为: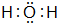 ;
;
(4)金属性Mg>Al,金属性越强,最高价氧化物对应水化物的碱性越强,故Mg(OH)2的碱性更强,
故答案为:Mg(OH)2;
(5)③与⑦形成的化合物为二氧化碳等,碳原子与氧原子之间形成共价键,属于分子晶体,
故答案为:共价;分子.
点评 本题考查元素周期表与元素周期律综合应用,侧重对元素周期律与化学用语的考查,注意掌握金属性、非金属强弱比较实验事实.


科目:高中化学 来源: 题型:解答题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | O | ||||||
| 3 | Na | Mg | Al | Si | S | |||
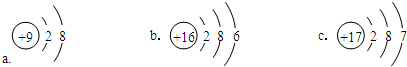
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | |
| D |
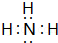 ,Y的结构式为
,Y的结构式为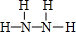
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
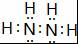 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
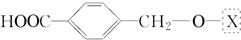 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.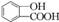 .
. 任意2种.
任意2种.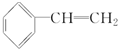 为主要原料制备
为主要原料制备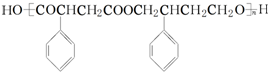 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).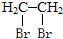
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
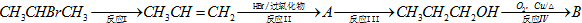 请回答下列问题:
请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:F2>C12>Br2 | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 熔沸点:SiO2>NaCl>CO2 | D. | 热稳定性:SiH4>PH3>H2S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com